Номенклатура и классификация ферментов
Вначале ферментам давали название по случайному признаку. Например, название пепсин происходит от слова peptis (пищеварение). Затем рабочее название фермента начали составлять из названия субстрата, типа катализируемой реакции и окончания «аза»: лактатдегидрогеназа. В 1961 году на Международном биохимическом съезде в Москве приняли систематическую классификацию ферментов. Их названия составляют из названия субстрата, класса реакции и окончания «аза». Если происходит перенос химической группы от донора к акцептору, то это включается в название: лактат:НАД-оксидоредуктаза.
Описано более 1900 ферментов, которые по типу катализируемой реакции деля на 6 классов: 1) оксидоредуктазы; 2) трансферазы; 3) гидролазы; 4) лиазы; 5) изомеразы; 6) лигазы (синтетазы). Каждый класс делится на подкласс, подкласс – на подподкласс. В последнем фермент имеет свой порядковый номер. Поэтому каждый фермент имеет свой шифр, состоящий из четырех чисел: номеров класса, подкласса, подподкласса и порядкового номера. Например, у лактат:НАД-оксидоредуктазы шифр 1.1.1.27.
1. Оксидоредуктазы катализируют окислительно-восстановительные реакции. Существует их 17 поклассов. Ферменты первого подкласса окисляют атомы водорода группы = СН - ОН:
СН3 СН3
1 1
СН-ОН + НАД Лактатдегидрогеназа С=О + НАД-Н2
1 1
СООН СООН .
Молочная кислота Пировиноградная килота.
У первого подподкласса акцептором ионов водорода является НАД, у второго – НАДФ, у третьего – цитохромы.
Ферменты второго класса окисляют альдегидную группу, третьего – группу
-СН2-СН2- и т.д. Ферменты, переносящие ионы водорода, называют дегидрогеназами. Если акцептором оксидоредуктазы служит кислород, ее называют оксидазой. Если при окислении кислорода он включается прямо в субстрат, то это – оксигеназы.
2. Трансферазы переносят различные функциональные группы от одного субстрата к другому. Аминотрансферазы перенося аминогруппы, метилтрансферазы – группы –СН3, ацилтрансферазы – радикалы кислот и т.д.
СООН СООН
1 1
СН2 CН3 СН2 СН3
1 1 1 1
СН2 + С=О Аланинамино- СН2 + СН-NH2
1 1 ←трансфераза→ 1 1
СН-NH2 СООН Пиридоксаль- С=О CООН
1 фосфат 1
COOH СООН
Глутамино- Пировиноград- α-кетоглутаро- Аланин
вая кислота ная кислота вая кислота
3. Гидролазы расщепляют вещества с присоединением к месту разрыва молекулы воды. Широко распространены. Гидролазы подкласса 3.1, эстеразы, расщепляют сложноэфирные связи эфиров фосфорной, карбоновых кислот, тиолов и т.д:
СН2 -О-СО-С17Н35 СН2 -ОН
1 1 С17Н35 –CO-О-СН Липаза НО-СН + 3 С17Н35 - СООН
1 1
СН2-О-СО-С17Н35 + 3 Н2О СН2-ОН Стеариновая кислота
Тристеарин Глицерол.
Гидролазы подкласса 3.1, гликозидазы, расщепляют О-, N- и S-гликозильные связи у различных соединений, например, у углеводов:
Гидролазы подкласса 3.4, пептидазы, расщепляют пептидные связи:
H2N-CH-CO-NH-CH-COOH Дипептидаза H2N-CH-COОН + H2N -CH-COOH
1 1 + Н2О 1 1
CH3 CH2 –OH СН3 CH2 –OH
Аланилсерин Аланин серин
4. Лиазы катализируют реакции расщепления веществ без присоединения к месту разрыва молекул воды или обратные им реакции –
соединение двух веществ в одно без затраты энергии в виде АТФ или других макроэргических соединений.

5. Изомеразы катализируют превращения, происходящих в пределах одной молекулы.

6. Лигазы (синтетазы) катализируют реакции соединения молекул двух веществ в одну с использованием энергии АТФ или другого макроэргического соединения. При этом образуются –С-О-, -C-S- и –С-N-cвязи.
СООН
СН3 СН2
1 1
СО2 + СН-ОН + АТФ Пируваткарбоксилаза С=О + АДФ + Н3РО4.
1 Биотин 1
СООН СООН
Пировиноградная Щавелевоуксусная
кислота кислота
Ферменты в сельском хозяйстве.
Ферменты широко используются в связанных с сельским хозяйством технологических процессах: производстве молочных продуктов, напитков, переработке пера, костей и др. Все чаще используются ферменты, иммобилизованные на гранулах стекла, полимерах и помещенные в колонки, через которые пропускают перерабатываемое вещество.
Распространены заболевания людей и животных, связанные с нарушением синтеза или повреждением некоторых ферментов (фенилкетонурия, галактоземия, гликогенозы и др.). Своевременная диагностика их позволяет проводить лечебно-профилактические мероприятия, направленные на снижение ущерба, наносимого этой патологией.
При патологии печени, поджелудочной железы, миокарда и других заболеваниях животных из поврежденных органов в кровь поступают ферменты. Определяя их активность, можно не только выявить пораженный орган, но и оценить тяжесть заболевания, эффективность проводимой терапии.
Ферменты широко используются в современных клинических биохимических исследования в качестве реагентов. Применение их позволяет повысить точность и облегчить проведение анализа.
Ферменты применяют для лечения животных с патологией органов пищеварительной системы, хирургическими заболеваниями и др.
Лекция №4
ОБМЕН ВЕЩЕСТВ
План
- Понятие об обмене веществ.
- Биологическое окисление.
- Обмен энергии. АТФ. Митохондрии.
- Цикл трикарбоновых кислот.
Обмен веществ – совокупность химических превращений, которым подвергаются вещества с момента поступления в организм до выделения их в виде конечных продуктов. Включает два взаимосвязанные между собой процессы: ассимиляцию и диссимиляцию. Ассимиляция – образование характерных для организма веществ, сопряженное с потреблением АТФ. Диссимиляция – процесс распада веществ в организме.
Этапы обмена веществ
- Пищеварение – гидролитическое расщепление ферментами веществ,
поступивших с пищей, до простых веществ- мономеров: белки расщепляются до аминокислот, жиры – до глицерина и жирных кислот, олиго- и полисахахариды – до моносахаридов.
- Всасывание мономеров в кровь в стенке кишечника.
- Межуточный (тканевой) обмен – химические превращения веществ в
тканях или метаболизм. Вещества, участвующие в этих превращениях – метаболиты. Одновременно в организме протекают процессы образования (анаболизм) и распада веществ (катаболизм).
4. Образование конечных продуктов -процесс, позволяющий высвободить около 80% энергии. Конечными продуктами метаболизма белков, углеводов и липидов являются углекислый газ и вода. При окислении белков образуется также аммиак, обезвреживающийся в мочевину.
Биологическое окисление – совокупность процессов окисления (отщепления и присоединения электронов), протекающих в клетках. Согласно теории В.И. Палладина оно заключается в отщеплении от окисляемого субстрата ионов водорода и электронов и переносе их на активированный кислород с образованием воды:
S-H2 2Н+ + 2е- ½ О2 → Н2О + энергия (210 кДж).
Реакция 2Н+ + ½ О2 → Н2О + энергия является основным источником энергии в организме. Вне организма она протекает быстро, с выделением большого количества энергии, с взрывом, а в организме – ступенчато. Энергия при этом выделяется порциями, что предотвращает перегревание клетки. Часть ее выделяется в виде тепла, часть запасается в макроэргических связях аденозинтрифосфата (АТФ):
Аденозиндифосфат (АДФ) + Н3РО4 + энергия → АТФ.
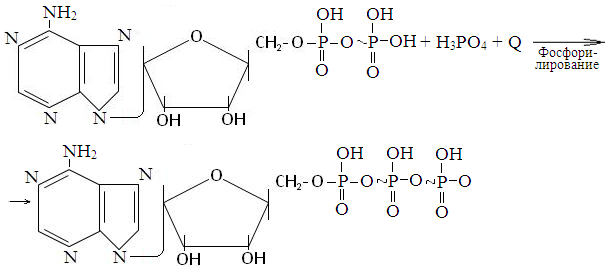
Синтез АТФ из АДФ и Н3РО4 называется фосфорилированием. Различают две разнолвидности его: субстратное и окислительное фосфорилирование. Первое из них (субстратное фосфорилирование) протекает за счет энергии, освобождающейся при расщеплении макроэргических (богатых энергией) химических связей некоторых веществ- субстратов: 1,3-дифосфоглицериновой, фосфоенолпировиноградной кислот (в реакциях окисления глюкозы ) и активной формы янтарной кислоты (в реакциях окисления активной формы уксусной кислоты в цикле Кребса); 2) за счет энергии освобождающейся при окислении кислородом ионов водорода ферментами дыхательной цепи, расположенной на внутренней мембране митохондрий (окислительное фосфорилирование).
Строение дыхательной цепи митохондрий
На внутренней мембране этих органоидов локализовано 8 оксидоредуктаз, коферменты которых располагаются последовательно в следующем порядке:
Ц и т о х р о м ы
S-H2 2е- НАД 2е- ФМН 2е- убихинон 2е- Ц.b 2е- Ц.c1 2е- Ц.c 2е- Ц.a 2е- Ц.a3 2е-
2Н+ 2Н+ 2Н+ 2Н+
Н2О ½ О2
-------------------- ----------------- -----------------
АТФ АТФ АТФ
Первый кофермент – НАД. Он принимает ионы водорода и электроны от субстрата S-H2, находящегося за пределами дыхательной цепи. Акцептором их является атом углерода никотинамида, находящийся в 4-м положении. Образовавшийся НАД-Н2 передает ионы водорода и электроны ФМН, где они присоединяются к атомам азота изоалаксозинового цикла. От ФМН-Н2 ионы водорода и электроны переходят на убихинон. Первые из них временно остаются на убихиноне и в дальнейшем, соединяясь с атомом активированного кислорода, образуют молекулу воды.
От убихинона електроны передаются на цитохром b, присоединяясь к атому железа гема, который меняет свою валентность с 3 на 2.. От цитохром b они перемещаются последовательно на цитохромы с1, с, а и а3. При каждом таком переходе электрона от одного фермента дыхательной цепи митохондрий к другом происходит постепенная потеря энергии и на цитохром а3 (цитохромоксидазу) переходит лишь остаток ее. Последний передается на молекулу кислорода, поступившую в клетку через кровь из легких, активируя ее. Активированный кислород после этого соединяется с ионами водорода, отщепившимися от убихинона и образуется вода, конечный продукт биологического окисления.
Генерации АТФ ферментами дыхательной цепи митохондрий
Каждые два фермента дыхательной цепи митохондрий образуют редокс-пару. Между ними имеются определенный окислительно-восстановительный потенциал (ОВП), э.д.с., выражающаяся в вольтах. В процессе переноса электронов происходит постепенное увеличение ОВП. У НАД он равен -0,32 в, у кислорода - +0,81 в. Генерация АТФ в дыхательной цепи митохондрий происходит на тех участках ее, где различие в ОВП между компонентами редокс-пары составляет не менее 0,2 в. Таких участков 3: 1) между НАД и ФМН; 2) между цитохромами b и c1; 3) между цитохромами а и а3.Поэтому при окислении ферментами дыхательной цепи митохондрий одной молекулы НАД-Н2 генерируется 3 молекулы АТФ. Если же окисляется ФАД-Н2, то ионы водорода и электроны передаются от него на ФМН, минуя первый пункт генерации АТФ, между НАД и ФМН. Поэтому произойдет генерация только двух молекул АТФ.
Согласно теории П. Митчелла, энергия, отдаваемая электронами при прохождении через эти участки дыхательной цепи, используется для перемещения положительно заряженных ионов водорода из внутреннего пространства митохондрий (матрикса) в пространство между внутренней и наружной мембранами их, т.е. на наружную поверхность внутренней мембраны этих органоидов (ВММ). Вследствие этого на последней накапливается избыток ионов водорода. При этом на внутренней поверхности ВММ содержится избыток отрицательно заряженных электронов. Поэтому создается разница потенциалов между наружной и внутренней поверхностями ВММ (мембранный потенциал).
Из-за наличия этого потенциала ионы водорода стремятся вернуться обратно в матрикс. Для этого они использую специальный канал, расположенный внутри фермента протонная АТФ-аза, расположенная на ВММ. Во время прохождения через этот канал ионов водорода выделяется энергия, которая используется для генерации из АДФ и фосфорной кислоты АТФ (окислительного фосфорилирования). Следовательно протонная АТФ-аза функционирует как АТФ- синтетаза.
Креатинкиназная реакция – «челночный» механизм, осуществляющий перенос энергии АТФ от места выработки его (митохондрий, расположенных на поверхности мышечных волокон) до места потребления (саркомеров мышечных волокон). Прямо поступать АТФ в саркомеры не может, т.к. расщепляется по пути ферментами.
Микросомальное окисление, протекающее с участие специальной цепи переноса электронов (ЦПЭ), расположенной на мембранах эндоплазматической цепи печени, надпочечников и других органов, также сопряжено с потреблением кислорода. При этом последний не только превращается в воду, но и используется для гидроксилирования (присоединения НО-группы) ряда веществ: стероидных гормонов, ядов лекарственных и других веществ, происходящее на первой стадии их инактивации. Микросомальная ЦПЭ состоит из четырех ферментов, коферментами которых являются НАДФ, ФАД, ион железа и цитохром Р450:
О R-H
2Н+
НАДФ-Н2 2Н+ флавопртеин---Fe-cодержащий белок--цит. Р450--О R-OH
2е- 2е- 2е- 2е-
Источники ионов водорода в клетках.
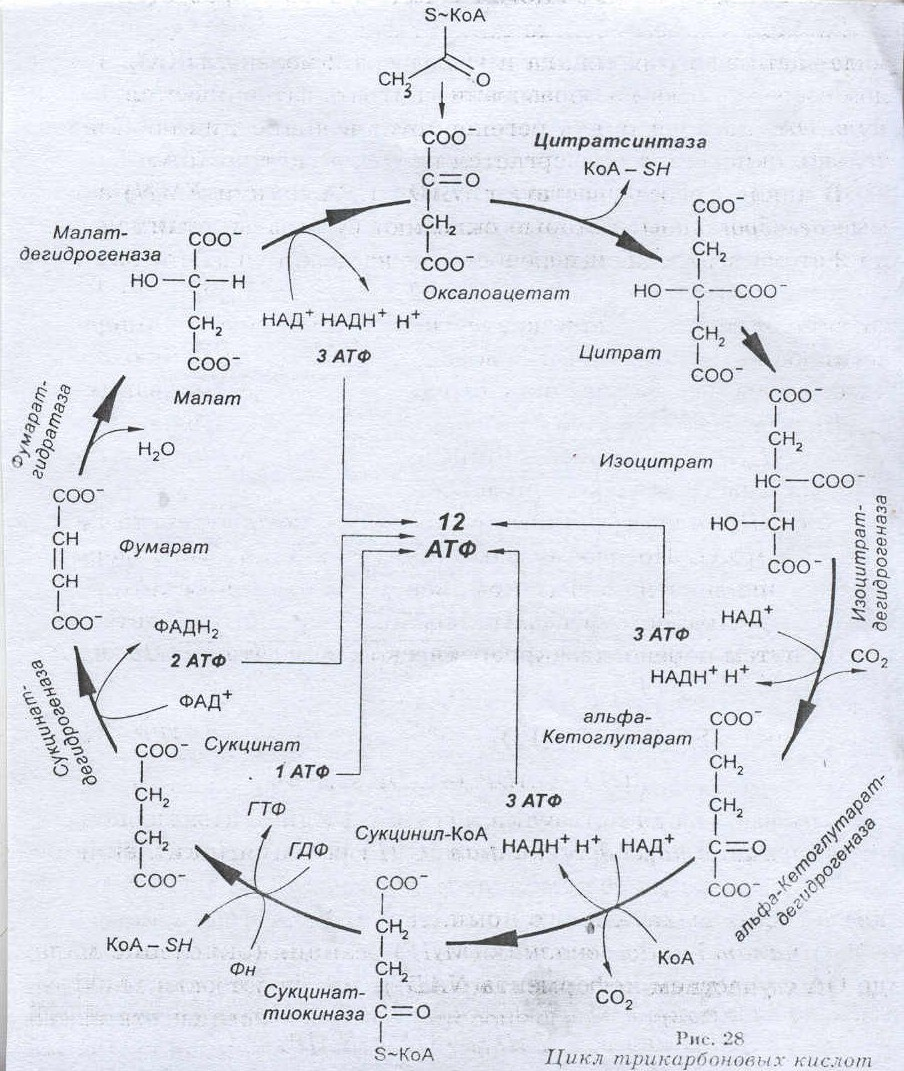
Большое количество ионов водорода генерируются в реакциях отщепления их от 3-фосфоглицеринового альдегида, молочной, пировиноградной кислот (окисление глюкозы), активированных жирных кислот (окисление липидов), глутаминовой кислоты (обмен белков). Основная масса их высвобождается при окислении в цикле трикарбоновых кислот, описанном Г. Кребсом, активированной уксусной кислоты (ацетил-КоА). Источником последнего является главным образом окисление пировиногроадной, жирных кислот и некоторых аминокислот.
Лекция №5
Цикл Кребса
План.
1. Реакции цикла трикарбоновых кислот.
2. Биологическая роль цикла Кребса.
Цикл Кребса – 10 последовательно протекающих реакций, начинающихся с вовлечения в процесс шавелевоуксусной кислоты и заканчивающихся высвобождением ее.