Функциональные дефекты лейкоцитов
Нарушения функциональных свойств лейкоцитов могут быть наследственными и приобретенными. Они связаны, главным об-
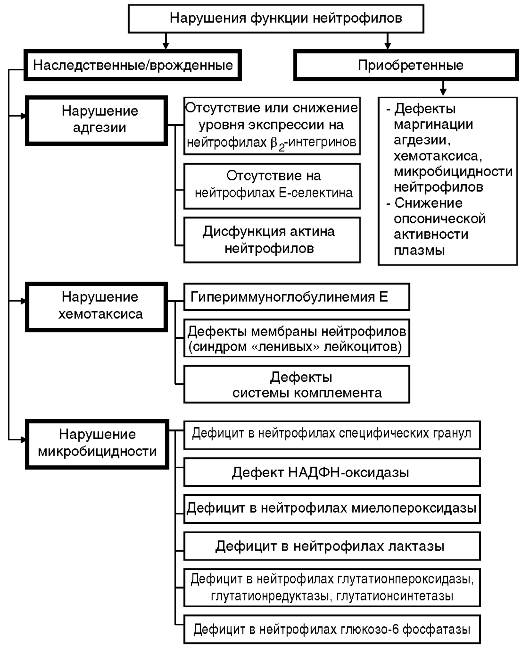 Рис. 14-11.Патогенетические факторы дисфункции нейтрофилов
Рис. 14-11.Патогенетические факторы дисфункции нейтрофилов
разом, с дефектами нейтрофильных гранулоцитов вследствие нарушения их маргинации, адгезии, миграции и микробицидных свойств (рис. 14-11).
Лейкоцитозы
Лейкоцитоз- увеличение общего количества лейкоцитов (более 9,0-109/л) или числа их отдельных морфологических форм.Лейкоцитоз носит временный характер и исчезает вместе с причиной,
его обусловившей; это не самостоятельное заболевание, а реакция крови на соответствующие этиологические факторы. В зависимости от природы этих факторов различают физиологические и патологические лейкоцитозы.
К физиологическим лейкоцитозамотносят алиментарный (пищеварительный), развивающийся через 2-3 ч после приема пищи; миогенный - при мышечном напряжении; эмоциональный - вследствие психического возбуждения, а также лейкоцитоз новорожденных (в течение первых двух дней жизни), беременных (развивающийся с 5-6-го мес беременности) и рожениц (отмечающийся ко второй неделе после родов). Кратковременный физиологический лейкоцитоз имеет перераспределительный характер и связан с мобилизацией в кровяное русло резерва зрелых лейкоцитов из органов-депо; длительный (новорожденных, беременных) - обусловлен активацией процессов образования лейкоцитов в костном мозгу.
Среди патологических лейкоцитозовразличают: инфекционный - при пневмонии, менингите, скарлатине и ряде других инфекционных заболеваний; воспалительный (особенно при гнойных воспалительных процессах) - при различного рода травмах: повреждении электрическим током, действии высокой и низкой температуры и т.д.; токсогенный - при действии вредных веществ как экзогенного (бензол, мышьяковистый водород, анилин и др.), так и эндогенного происхождения (при уремии, диабетической коме); постгеморрагический - наступающий после острых кровопотерь; новообразовательный - при распаде опухолей; лейкемический - при острых и хронических лейкозах. Механизм их возникновения связан с повышением лейкопоэтической функции костного мозга, и лишь один вид патологического лейкоцитоза - центрогенный (при шоковых состояниях, эпилепсии, агонии; послеоперационный) имеет перераспределительный характер.
В зависимости от увеличения содержания тех или иных видов лейкоцитов в крови различают нейтрофильный лейкоцитоз, эозинофилию, базофилию, лимфоцитоз и моноцитоз.
Нейтрофильный лейкоцитоз (нейтрофилия)- увеличение содержания нейтрофилов свыше 70% в гемограмме. Отмечается при острых инфекционных заболеваниях, гнойных воспалительных процессах, инфаркте миокарда, укусах ядовитых насекомых, после острой кровопотери, а также при алиментарном и эмоциональном физиологических лейкоцитозах. Важное практическое значение имеет определение степени ядерного сдвига в лейкоцитарной фор-
муле.По этому признаку различают шесть видов нейтрофильного лейкоцитоза (табл. 14-8):
1) без ядерного сдвига - при острой кровопотере, стрессреакции;
2) с гипорегенеративным ядерным сдвигом влево - при легком течении ряда инфекций и воспалений;
3) с регенеративным ядерным сдвигом влево - при гнойносептических процессах;
4) с гиперрегенеративным ядерным сдвигом влево - признак неблагоприятного течения инфекционных и гнойно-септических заболеваний;
5) с дегенеративным ядерным сдвигом влево - показатель угнетения функциональной активности костного мозга, может иметь место при тяжелом течении инфекционных заболеваний, при эндогенной интоксикации и т.д.;
6) с дегенеративным ядерным сдвигом вправо - при лучевой болезни, злокачественной анемии Аддисона-Бирмера; в ряде случаев у практически здоровых людей.
Таблица 14-8.Классификация нейтрофилий в зависимости от характера и
| степени ядерного сдвига Варианты нейтрофилии Характеристика | |
| Без сдвига | Увеличение общего числа нейтрофилов (>70%) за счет сегментно-ядерных форм клеток (>65%) |
| Со сдвигом влево: | |
| гипорегенераторным | Увеличение общего числа нейтрофилов (>70%) за счет сегментно-ядерных (>65%) и палочкоядерных (>5%) форм клеток |
| регенераторным | Увеличение общего числа нейтрофилов (>70%) за счет сегментно-ядерных (>65%), палочкоядерных (>5%) форм клеток и метамиелоцитов (>0,5%) |
| гиперрегенераторным | Увеличение общего числа нейтрофилов (>70%) за счет сегментно-ядерных (>65%), палочкоядерных (>5%) форм клеток, метамиелоцитов (>0,5%) и более молодых клеток (миелоцитов, промиелоцитов, миелобластов). Анэозинофилия |
Окончание табл. 14-8
| дегенеративным | Увеличение общего числа нейтрофилов (>70%) за счет сегментно-ядерных (>65%) и палочкоядерных (>5%) форм клеток, появление в крови нейтрофилов с признаками дегенерации (вакуолизация ядра и цитоплазмы, токсогенная зернистость, кариорексис и др.) |
| Со сдвигом вправо | Увеличение общего числа нейтрофилов (>70%) за счет сегментно-ядерных форм клеток (>65%) на фоне повышенного (>5%) содержания в крови гиперсегментно-ядерных нейтрофилов (более 5 ядерных сегментов) |
Эозинофилия- увеличение содержания эозинофилов свыше 5% в гемограмме. По современным представлениям эозинофилия является своеобразной реакцией организма на чужеродные белки, гистамин, инвазию паразитами и связана с антитоксической, антигистаминной (посредством гистаминазы - фермента гранул эозинофилов), фагоцитарной (фагоцитоз иммунных комплексов) и противогельминтной (экзоцитоз личинок, разрушение миелина нервных волокон паразитов) функцией эозинофилов.
Развитие эозинофилии имеет место при различных аллергических заболеваниях и синдромах (бронхиальная астма, отек Квинке, крапивница и др.); при паразитарных заболеваниях (описторхоз, аскаридоз, лямблиоз и др.), некоторых кожных болезнях (псориаз, экзема), коллагенозах (ревматизм, дерматомиозит), гемобластозах (хронический миелолейкоз, лимфогранулематоз), некоторых эндокринопатиях (гипофизарная кахексия, микседема и др.), ряде инфекционных заболеваний (скарлатина, сифилис, туберкулез), при применении некоторых лекарственных препаратов (антибиотики, сульфаниламиды и др.); описаны также наследственные формы эозинофилии.
Базофилия(более 1% базофилов в гемограмме) - редкая форма лейкоцитоза, встречающаяся при анафилактических и реагиновых аллергических реакциях (крапивница, отек Квинке, пищевая и лекарственная аллергия и др.), что обусловливается способностью базофилов фиксировать IgE и IgG, высвобождать медиаторы гранул (факторы хемотаксиса нейтрофилов и эозинофилов, гепарин, гистамин, серотонин и др.). Базофилия обнаруживается также при
вакцинации, гемолитических анемиях, гемофилии, эндокринопатиях (сахарный диабет, микседема и др.), хроническом миелолейкозе.
Лимфоцитоз- увеличение содержания лимфоцитов свыше 45% в гемограмме. Физиологический лимфоцитоз характерен для детей первых 10 лет жизни, а также отмечается у вегетарианцев и после физических нагрузок (миогенный). В условиях патологии лимфоцитоз развивается при ряде инфекционных заболеваний (брюшной тиф, свинка, коклюш, малярия, бруцеллез, инфекционный мононуклеоз, туберкулез, сифилис и др.), что связано с формированием противоинфекционного иммунитета, а также при алиментарной дистрофии, бронхиальной астме и некоторых эндокринных расстройствах (евнухоидизм, микседема, акромегалия).
Моноцитоз- увеличение содержания моноцитов свыше 9% в гемограмме. Обнаруживается при персистентных бактериальных и вирусных инфекциях (туберкулез, инфекционный мононуклеоз, корь, краснуха и др.), воспалительных заболеваниях (неспецифический язвенный колит, спру, коллагенозах и др.), гемобластозах, раке молочной железы и яичников, после спленэктомии и др.
Лейкемоидные реакции
Лейкемоидные реакции - патологические реакции системы крови, характеризующиеся изменениями в периферической крови (увеличением общего количества лейкоцитов до 30-109/л и выше, появлением незрелых форм лейкоцитов), сходными с таковыми при лейкозах и исчезающими после купирования вызвавшего их первичного процесса.При этом клеточный состав костного мозга (в отличие от лейкозов) остается нормальным. Выделяют две большие группы лейкемоидных реакций: миелоидного и лимфатического (моноцитарно-лимфатического) типов (см. табл. 14-9). В свою очередь, лейкемоидные реакции миелоидного типа подразделяют на нейтрофильные лейкемоидные реакции (при инфекционновоспалительных заболеваниях, интоксикациях, опухолях) и так называемые большие эозинофилии крови (при паразитарных инвазиях, аллергических заболеваниях, коллагенозах и др.). Среди лейкемоидных реакций моноцитарно-лимфатического типа наиболее важной в практическом отношении является лейкемоидная реакция с картиной острого лимфобластного лейкоза при инфекционном мононуклеозе, при которой в периферической
крови обнаруживаются «атипичные мононуклеары» - трансформированные вирусом Эпштейна-Барр или другими инфекционными возбудителями (вирус простого герпеса, цитомегаловирус, Toxoplasma gondii и др.) мононуклеарные лейкоциты (лимфоциты, моноциты), сходные по морфологии с бластными клетками.
Лейкопении
Лейкопения- уменьшение общего количества лейкоцитов ниже 4,0-109/л.Наиболее часто развитие лейкопении связано с уменьшением абсолютного числа нейтрофилов (нейтропения).Лимфоцитопения может иметь место при лимфогранулематозе, пневмонии, сепсисе, коллагенозах и некоторых других заболеваниях, но редко является причиной лейкопении. Моноцитопения, эозинопения, хотя и имеют существенное диагностическое значение, но не отражаются на общем количестве лейкоцитов.
В основе патогенеза лейкопении (нейтропении) лежат три механизма: 1) угнетение лейкопоэтической функции костного мозга; 2) повышенное разрушение нейтрофилов; 3) перераспределение нейтрофилов.
Нейтропении, обусловленные угнетением лейкопоэтической функции костного мозга.Развитие их в основном связано:
1) с нарушением пролиферации и дифференцировки стволовых гемопоэтических клеток при «внутреннем» дефекте клетокпредшественниц грануломоноцитопоэза - потере способности их к дифференцировке в клетки нейтрофильного ряда при сохраняющейся способности к нормальной дифференцировке в эозинофильные, базофильные и моноцитарные клетки, при дефиците веществ, необходимых для деления и созревания кроветворных клеток (белки, аминокислоты, витамины В12, фолиевая кислота и др.), а также вследствие аутоиммунных механизмов, связанных с образованием антиКОЕ-ГМ антител и аутореактивных Т-лимфоцитов;
2) с разрушением клеток-предшественниц нейтрофилов в костном мозгу при действии токсических веществ и лекарственных препаратов;
3) с патологией гемопоэзиндуцирующего микроокружения, в том числе в случаях выпадения стимулирующей дифференцировку стволовых клеток функции Т-лимфоцитов (при аплазии тимуса), гипосекреции клетками ГИМ факторов роста (ГМ-КСФ, Г-КСФ, IL-3, М-КСФ и др.;
4) с уменьшением площади гранулоцитопоэза в результате замещения кроветворной ткани костного мозга опухолевой (при лейкозах и карцинозах - метастазах рака в костный мозг), фиброзной, костной, жировой тканью.
Кроме того, формирование данного рода нейтропений может быть обусловлено наследственным дефектом механизма обратной связи, контролирующего процесс образования, созревания нейтрофилов в костном мозгу и их элиминацию на периферию.
Нейтропении, обусловленные повышением разрушения нейтрофилов.Разрушение нейтрофилов в крови может происходить под влиянием антител типа лейкоагглютининов, которые образуются при переливании крови (особенно лейкоцитарной массы), при действии некоторых лекарственных препаратов, являющихся аллергенами-гаптенами (сульфаниламиды, амидопирин и др.), токсических факторов инфекционного происхождения (тяжелые инфекционные заболевания, обширные воспалительные процессы), при заболеваниях, сопровождающихся увеличением количества циркулирующих иммунных комплексов в крови (аутоиммунные заболевания, лимфомы, опухоли, лейкозы и др.). Причиной наследственных нейтропений этой группы может быть преждевременная гибель клеток вследствие цитогенетической аномалии (тетраплоидия). Наряду с этим нейтропения может развиваться вследствие повышенного разрушения циркулирующих нейтрофилов в селезенке при заболеваниях, сопровождающихся гиперспленизмом (коллагенозы, цирроз печени, гемолитическая анемия, болезнь Фелти и др.).
Нейтропения, связанная с перераспределением нейтрофилов,носит временный характер и, как правило, сменяется лейкоцитозом. Ее формирование отмечается при шоке, неврозах, острой малярии и некоторых других состояниях в результате скопления клеток в расширенных капиллярах органов-депо (легкие, печень, кишечник). Перераспределительная нейтропения может обусловливаться также избыточной адгезией нейтрофилов на эндотелиоцитах вследствие активации эндотелия с последующей миграцией гранулоцитов в ткани под влиянием IL-8. Данный механизм лежит в основе хронической идиопатической нейтропении, характеризующейся повышенным содержанием IL-8 и растворимых лейкоцитарных адгезивных молекул к эндотелию (sELAM, sICAM, sVCAM) в сыворотке крови.
Таблица 14-9.Варианты лейкемоидных реакций и их характеристика
| Вариант ЛР | Причины развития | Картина крови |
| 1. Миелоидного типа | ||
| Нейтрофильные: | ||
| Псевдобластная | «Выход» из иммунного агранулоцитоза Первичный туберкулез Тяжелые токсикоинфекции (дифтерия, столбняк и др.) Сепсис | Появление большого числа бластоподобных клеток |
| Промиелоцитарная | Появление большого числа типичных промиелоцитов | |
| С картиной хронического миелолейкоза | Инфекции (бактериальные, вирусные, грибковые) Воспаление (хронические васкулиты, дерматиты, подагра, миозиты и др.) Интоксикация (при эндокринных расстройствах, нарушениях метаболизма, уремии, отравлениях) Злокачественные новообразования (рак молочной железы, почек, печени, легких) Лимфогранулематоз | Нейтрофилия с гиперрегенераторным ядерным сдвигом влево при нормальном содержании эозинофилов и базофилов, дегенеративные изменения нейтрофилов (токсогенная зернистость, кариопикноз) |
| Большая эозинофилия крови | Паразитозы (филяриоз, лямблиоз, описторхоз и ДР-) Аллергические заболевания (бронхиальная астма, аллергический ринит, лекарственная аллергия при приеме антибиотиков, сульфаниламидов, ацетилсалициловой кислоты) | Увеличение числа эозинофилов (>15%) и изменение их морфологии (вакуолизация ядра, цитоплазмы) |
Продолжение табл. 14-9
| Коллагенозы (ревматоидный артрит, узелковый периартериит, системная склеродермия, системная красная волчанка) Пристеночный фибропластический эндокардит (эндокардит Леффлера) Иммунодефицитные синдромы (синдром Вискотта-Олдрича, дефицит IgA) Злокачественные новообразования (рак щитовидной железы, желудка, гипернефроидный рак почки, лимфогранулематоз, лимфома Ходжкина, хронический миелолейкоз) Выделяют также идиопатические и наследственные формы | ||
| 2. Моноцитарно-лимфатического типа | ||
| С картиной острого лимфобластного лейкоза | Инфекционный мононуклеоз (болезнь Филатова) | ОКЛ - 20-109/л и более, увеличение числа лимфоцитов и моноцитов, «атипичных мононуклеаров» (>10%), нейтропения |
| Острый инфекционный лимфоцитоз | Энтеровирусная инфекция, вызванная вирусом Коксаки Болезнь кошачьих царапин Бактериальные инфекции (коклюш, иерсиниоз, туберкулез и др.) Протозойная инвазия (токсоплазмоз, малярия) | ОКЛ - 15-100? 109/л и более, лимфоцитоз (>60%) без изменений морфологии клеток, моноцитоз |
Окончание табл. 14-9
| Стресс-лимфоцитоз | Сердечно-сосудистая патология (кардиоваскулярный коллапс, острая сердечная недостаточность, инфаркт миокарда, септический шок и др.) Реакции гиперчувствительности немедленного типа Хирургические вмешательства Травмы Эпилепсия | Кратковременный лимфоцитоз до 5-109/л и более |
| Персистирующий лимфоцитоз | Ревматоидный артрит Злокачественные новообразования (тимома) Хронические воспалительные заболевания (саркоидоз, гранулематоз Вегнера и др.) Реакции гиперчувствительности замедленного типа Гипоспленизм Курение | Длительный лимфоцитоз до 3,8-109/л и более |
| Реактивный моноцитоз | Инфекционно-воспалительные заболевания (туберкулез, хронический пиелонефрит, саркоидоз, спру) Злокачественные новообразования (рак молочной железы и яичников, лимфогранулематоз, миеломная болезнь) | Увеличение числа моноцитов (>0,8-109/л) |
Примечание. ОКЛ - общее количество лейкоцитов.
Агранулоцитоз - клинико-гематологический синдром, характеризующийся полным или почти полным отсутствием нейтрофильных гранулоцитов в крови.Условно за агранулоцитоз принимают состояние, при котором уровень гранулоцитов ниже 0,75-109/л и/или общее количество лейкоцитов менее 1-109/л. Иногда этим термином обозначают тяжелую нейтропению.
Наиболее часто развитие агранулоцитоза связано с приемом медикаментов (цитостатические препараты, амидопирин, аминазин, антитиреоидные средства, сульфаниламиды, некоторые антибиотики и др.). Во многих случаях этиологические факторы, приводящие к возникновению тяжелой гранулоцитопении, остаются неустановленными («генуинные», или идиопатические агранулоциозы).
По механизму развития агранулоцитозы подразделяют на миелотоксический и иммунный (см. табл. 14-10). В основе миелотоксическогоагранулоцитоза лежит угнетающее действие медикаментозных препаратов и других повреждающих факторов на пролиферативную активность гранулоцитарных элементов костного мозга, вследствие чего развивается гипоплазия гранулоцитопоэза; возможность возникновения тяжелой гранулоцитопении при этом определяется суммарной дозой принятого препарата. Миелотоксический агранулоцитоз обычно сочетается с анемией и тромбоцитопенией.
Ведущее значение в патогенезе иммунный(гаптеновых) агранулоцитозов имеет появление в организме антител (агглютинины, лизины и т.д.), действие которых направлено против собственных гранулоцитов периферической крови или их клеток-предшественниц в костном мозгу. Считается, что медикаментозные препараты выступают в роли гаптенов, образующих комплексные соединения с белками плазмы и мембран лейкоцитов. Вырабатываемые на образовавшийся «чужеродный» комплекс (антиген) антитела, фиксируясь на поверхности клеток, вызывают их разрушение. Как правило, при иммунном агранулоцитозе снижается содержание только лейкоцитов.
Классическим клиническим проявлением агранулоцитоза независимо от причин и механизмов его развития является язвеннонекротическая ангина(angina agranulocytotica), развивающаяся вследствие подавления защитных реакций организма (снижения резистентности к бактериальной флоре).
Лейкозы
Одной из наиболее опасных для жизни человека патологий системы крови являются лейкозы, относящиеся к группе гемобластозов - злокачественных новообразований кроветворной (миелоидной и лимфоидной) ткани. В отличие от лейкоцитозов, лейкемоидных реакций и лейкопений лейкоз является не реактивным состоянием, а болезнью системы крови.
Лейкоз - это опухоль, исходящая из кроветворных клеток костного мозга, в основе развития которой лежит неконтролируемый рост клеток с преобладанием процессов их пролиферации над дифференцировкой и образованием очагов патологического кроветворения в органах и тканях, в норме не участвующих в гемопоэзе.При этом утратившие способность к созреванию лейкозные клетки могут проходить значительно большее, чем нормальные клетки крови, число циклов деления, что и создает огромную клеточную продукцию, характеризующую лейкоз.
Этиология лейкозовдо настоящего времени точно не установлена. Об опухолевой природе лейкозов свидетельствует наличие общих закономерностей, объединяющих лейкозы и опухоли: нарушение способности клеток к дифференцировке; морфологическая и метаболическая анаплазия клеток; способность к метастазированию; общие этиологические факторы, способствующие развитию лейкозов и опухолей, и др.
К возможным этиологическим факторам, вызывающим развитие лейкозов, относят ионизирующую радиацию, ряд химических веществ, вирусы. Определенное значение в развитии лейкозов придается генетическим факторам, наследственной и приобретенной иммунной недостаточности, действию бластомогенных метаболитов триптофана и тирозина.
Соответственно существует несколько теорий происхождения лейкозов.
Радиационная теория. Роль ионизирующих излучений в возникновении лейкозов доказана в эксперименте. Как однократное (в дозе 2 Гр и выше), так и хроническое (в течение 2-3 месяцев) облучение лучами Рентгена в малых дозах может индуцировать лейкоз у лабораторных животных (крысы, мыши). Прослежено повышение заболеваемости острым и хроническим миелолейкозом у жителей Хиросимы и Нагасаки, у рентгенологов и радиологов. Приводятся данные об увеличении частоты лейкозов у больных, леченных
большими дозами лучей Рентгена, иттрия, радия по поводу злокачественных новообразований и анкилозирующего спондилоартрита, а также у детей, получавших облучение вилочковой железы в раннем возрасте, и др. Описано учащение случаев острых лейкозов среди больных эритремией после лечения их радиоактивным фосфором.
Теория химического лейкозогенеза. Экспериментально доказана возможность индуцирования лейкозов у животных введением канцерогенных веществ (диметилбензантрацен, метилхолантрен и др.). Также в эксперименте показана возможность стимуляции лейкозогенеза метаболитами триптофана и тирозина (М.Л. Раушенбах). Однако роль этих веществ в лейкозогенезе человека не доказана. В то же время накоплены данные, указывающие на увеличение риска заболевания лейкозами (как правило, острыми) у людей, имеющих длительный профессиональный контакт с бензолом и летучими органическими растворителями (шоферы, работники кожевенной и обувной промышленности и т.д.). В последние годы отмечено заметное учащение случаев острого лейкоза у больных злокачественными новообразованиями, леченных такими цитостатическими препаратами, как циклосфосфан, хлорбутин, метотрексат, миелосан, адриамицин и др. К лекарственным препаратам, способным индуцировать лейкозы, относятся также бутадион, левомицетин и некоторые другие.
Вирусная теория связывает возникновение лейкозов с активацией (под действием радиации и химических факторов) латентных лейкозогенных вирусов. Несомненно доказанным является вирусное происхождение лейкозов у многих видов животных - птиц, мышей, крыс, хомячков, кошек, крупного рогатого скота. К настоящему времени выделено и детально охарактеризовано несколько типов вирусов, вызывающих различные виды лейкозов у животных. Как правило, это РНК-содержащие вирусы, а также ДНК-содержащие вирусы, которые относятся к герпесвирусам (подробнее см. раздел 13.3).
Вопрос о роли вирусов в происхождении лейкозов у человека остается во многом спорным. Против вирусной этиологии лейкозов у человека свидетельствует, прежде всего, факт невозможности прямой перевивки лейкозов при случайном переливании крови лиц, больных лейкозом, и отсутствие убедительных доказательств контагиозности лейкозов. Не описаны также случаи передачи лейкоза от больной матери плоду и новорожденному в период вскармливания грудью.
Таблица 14-10.Дифференциальные критерии лекарственных агранулоцитозов
| Критерии | Вид агранулоцитоза | ||
| миелотоксический | иммунный | ||
| Патогенез | Вследствие прямого повреждения клетокпредшественниц гемопоэза | Вследствие иммунного разрушения циркулирующих нейтрофилов | Вследствие иммунного разрушения клетокпредшественниц гранулоцитопоэза |
| Начало | Постепенное | Острое | Постепенное |
| Клинические проявления | Лихорадка, язвеннонекротическое поражение слизистых оболочек ротоглотки и желудочнокишечного тракта, некротическая энтеропатия | Лихорадка, озноб, крапивница, отек Квинке, изъязвление слизистых оболочек ротоглотки, верхних дыхательных путей, желудочно-кишечного тракта, увеличение размеров лимфоузлов, печени и селезенки, грибковые инфекции | |
| Связь с дозой медикамента | Присутствует | Отсутствует | |
| Количество лейкоцитов | Снижение общего количества лейкоцитов, нейтропения до (0,2-0,1)-109/л, моноцитоз, лимфоцитоз, увеличение числа плазматических клеток (только при иммунном агранулоцитозе) | ||
| Количество тромбоцитов | Снижено | В норме | |
| Анемия | Определяется | Не определяется | |
| Картина костного мозга | Тотальное угнетение гемопоэза | Гиперплазия гранулоцитарного ростка | Гипоплазия гранулоцитарного ростка |
| Антилейкоцитарные антитела | Отсутствуют | Присутствуют |
Генетическая теория располагает достаточно убедительными аргументами, указывающими на возможность наследственной предрасположенности к лейкозам. Известны случаи семейных лейкозов, доказана роль этнических особенностей в развитии лимфолейкоза. К возникновению лейкозов предрасполагают болезни, характеризующиеся спонтанными разрывами хромосом и нерасхождением соматических или половых хромосом (болезнь Дауна, анемия Фанкони, синдромы Кляйнфелтера, Тернера и др.). Получены линии мышей, у которых частота спонтанных лейкозов близка к 100%.
Патогенез лейкозов.Согласно мутационно-клоновой теории, в основе происхождения лейкозов лежат мутация и опухолевая трансформация ранних клеток-предшественниц гемопоэза (клеток II и III классов) под влиянием лейкозогенного фактора (ионизирующей радиации, химических веществ, вирусов и др.). В результате происходит выход кроветворных клеток из-под контроля регулирующих систем макроорганизма с активацией их деления на фоне подавления дифференцировки. Формируется клон опухолевых (лейкозных) клеток - потомков одной первоначально мутировавшей клетки (моноклоновая опухоль),которые заселяют (инфильтрируют) костный мозг. В моноклоновой стадии опухолевые клетки чувствительны к химиотерапии. В процессе развития лейкоза (опухолевая прогрессия) происходят качественные изменения составляющих субстрат опухоли клеток, обусловленные нестабильностью их генетического аппарата, что проявляется нарушениями структуры хромосом, анэуплоидией, переходом части ранее неактивных в клетке генов в активное состояние (феномен дерепрессирования генов). Эти изменения ведут к появлению новых клонов опухолевых клеток, среди которых в процессе жизнедеятельности организма, а также под воздействием лечебных средств, применяемых в химиотерапии заболевания, «отбираются» наиболее автономные клоны. В результате моноклоновая опухоль превращается в поликлоновую злокачественную опухоль.На этой стадии развития лейкоза лейкозные клетки становятся устойчивыми к цитостатической терапии, метастазируют в органы и ткани, в норме не участвующие в гемопоэзе, образуя очаги экстрамедуллярного кроветворения (табл. 14-11).
Таблица 14-11.Основные стадии патогенеза лейкозов
| Стадия Характеристика | |
| Инициация | Лейкозогенный фактор (радиация, вирусы и др.) действует на стволовые кроветворные клетки II-III классов, вызывая их опухолевую трансформацию в результате мутационного превращения протоонкогенов в онкогены и инактивации антионкогенов |
| Промоция | Активация и гиперпролиферация лейкозных клеток при действии промотора с формированием клона лейкозных клеток, идентичных по фенотипу и генотипу (моноклоновая стадия) |
| Инфильтрация | «Расселение» лейкозных клеток в костном мозгу с угнетением нормального гемопоэза |
| Прогрессия | Формирование множества клонов лейкозных клеток, различающихся по фенотипу и генотипу (поликлоновая стадия), и естественный отбор наиболее автономных из них, что ведет к «озлокачествлению» заболевания |
| Метастазирование | Образование очагов патологического кроветворения вне костного мозга за счет способности лейкозных клеток к инвазии, интра- и экстравазации, миграции по сосудистой системе, имплантации и пролиферации в различных тканях и органах |
О клоновой природе лейкозов свидетельствуют возможность перевивки лейкоза мышам путем введения одной лейкозной клетки; продукция гомогенного иммуноглобулина при парапротеинемических гемобластозах (миеломная болезнь, макроглобулинемия Вальденстрема и др.); однотипность лейкозных клеток (несущих на поверхности иммуноглобулины одного класса и подкласса) при хроническом лимфолейкозе; наличие специфических хромосомных изменений в опухолевых клетках (транслокации, делеции). Частным подтверждением клонового происхождения лейкозов является обнаружение в 80-90% случаев хронического миелолейкоза аномальной филадельфийской (Ph') хромосомы (рис. 14-12) в миелоидных клетках, включая гранулоцитарный, эритроидный и мегакариоцитарный ростки. Этот факт служит неоспоримым доказательством происхождения хронического миелолейкоза из одного патологического клона, родоначальницей которого является
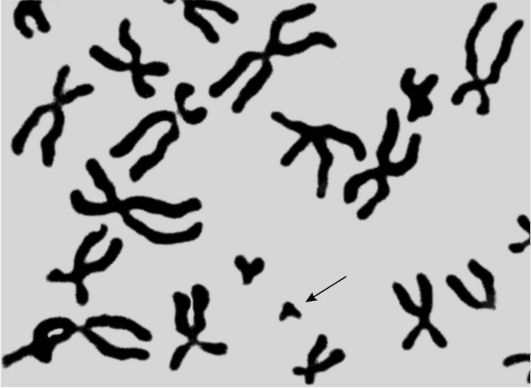 Рис. 14-12.Аномальная Ph'-хромосома в клетке больного хроническим миелолейкозом
Рис. 14-12.Аномальная Ph'-хромосома в клетке больного хроническим миелолейкозом
плюрипотентная стволовая клетка-предшественница миелопоэза (КОЕ-ГЭММ).
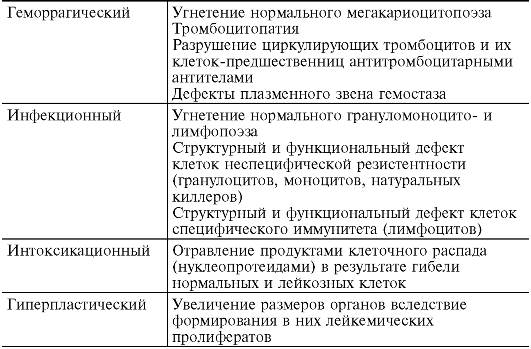
Общие нарушения в организме при лейкозахпроявляются следующими клиническими синдромами: анемическим (головокружение, слабость, повышенная утомляемость, одышка и т.д.), геморрагическим (кровотечения из десен, носа, кишечника, кровоизлияния в жизненно важные органы), инфекционным (рецидивирующие инфекции вследствие угнетения фагоцитоза, микробицидной функции лейкоцитов, синтеза антител и т.д.), интоксикационным (тошнота, рвота, снижение аппетита, уменьшение массы тела и т.д.) и гиперпластическим (увеличение размеров и нарушение функции различных органов) (табл. 14-12).
Таблица 14-12.Патогенез основных клинических синдромов лейкозов

 Причинами смерти при лейкозах являются резкое малокровие и тяжелая общая интоксикация, поражение жизненно важных органов (лейкозная инфильтрация, обширные кровоизлияния). Непосредственной причиной смерти больных могут стать инфекционные осложнения (пневмонии, сепсис, перитонит).
Причинами смерти при лейкозах являются резкое малокровие и тяжелая общая интоксикация, поражение жизненно важных органов (лейкозная инфильтрация, обширные кровоизлияния). Непосредственной причиной смерти больных могут стать инфекционные осложнения (пневмонии, сепсис, перитонит).
