Химическая кинетика. Химическое равновесие.
Химическая реакция – единичный элементарный акт взаимодействия или превращения частиц, в результате которого образуются новые частицы.
Характеристики реакции:
1) молекулярность – число частиц, участвующих в элементарном акте
2) агрегатные состояния реагентов:
· гомогенные (реакции в объеме)
· гетерогенные (реакции на поверхности)
· биохимические реакции
3) скорость реакции
· Скорость для гомогенных – определяется количеством вещества (1 моль), прореагировавшего за единицу времени (1 с) в единице объема (1 л)
· Скорость для гетерогенных – определяется количеством вещества (1 моль), прореагировавшего за единицу времени (1 с) на единицу площади (1 м куб.)
Факторы, влияющие на скорость
1) природа реагирующих веществ: полярнее вещество – выше скорость
2) температура: увеличивается температура, увеличивается число «активных частиц»
Теория энергии активации
обычные условия: молекулы не обладают энергией для преодоления энергетического барьера
Закон Вант – Гоффа: при повышении температуры на каждые 10 градусов скорость увеличивается в Ƴ раз
Энергия активации – небольшой избыток над средней энергией молекул, необходимый для превращения реагентов в продукты (зависит от природы вещества и катализатора)
Активированные комплексы – наиболее выгодный путь протекания реакции, требующий наименьших энергетических затрат.
Уравнение Аррениуса: устанавливает зависимость константы скорости {\displaystyle k}химической реакции от температуры. Согласно простой модели столкновений, химическая реакция между двумя исходными веществами может происходить только в результате столкновения молекул этих веществ. Но не каждое столкновение ведёт к химической реакции. Необходимо преодолеть определённый энергетический барьер, чтобы молекулы начали друг с другом реагировать. То есть молекулы должны обладать некой минимальной энергией{\displaystyle E_{A}}, чтобы этот барьер преодолеть.


3) катализатор:
· катализатор – вещество, ускоряющее реакцию за счет понижения энергии активации
· ингибитор – увеличивает энергию активации
· промотор – вещество, повышающее активность катализатора
· каталитический яд – снижает активность катализатора, разрушает активированные комплексы (группировка атомов в решающий момент элементарного акта химической реакции)
Теория катализа
· гомогенный катализ: реагенты и катализатор в одной фазе, катализатор образует промежуточное неустойчивое соединение с одним из реагентов
· гетерогенный катализ: реагенты и катализатор в разных фазах, реакция идет на поверхности катализатора (поверхность катализатора содержит «активные центры», молекулы адсорбируются на поверхности катализатора)
Ферментативный катализ (биокатализ) – ускорение биохимических реакций при участии белковых макромолекул. называемых ферментами (энзимами).
Особенности ферментативного катализа:
1) в организме катализаторы – ферменты
2)ферменты обладают высокой активностью и селективностью
3) в процессе катализа ферменты разрушаются
4) действие ферментов зависит от реакции среды и температуры
5) скорость ферментативной реакции зависит от концентрации фермента или субстрата только при очень небольших концентрациях
6) 1 моль каталазы при 0 градусов обеспечивает разложение 5 млн. молекул перекиси водорода за 1 минуту
Закон действующих масс: скорость реакции прямо пропорциональна произведению С реагирующих веществ, взятых в степенях равных порядку реакции
· Физический смысл константы скорости заключается в том, что она равна скорости реакции при единичных концентрациях реагирующих веществ
Для реакции с участием газов давление оказывает такое же воздействие, как и концентрация.
Порядок реакции – величина, которая показывает влияние С данного вещества на скорость реакции
Константа скорости:
1) природа веществ
2) температура
3) катализатор
4) не зависит от С
Химическое равновесие
· обратимые реакции – реакции, при которых реагенты превращаются в продукты, а продукты – в реагенты (протекают 2 противоположные реакции)
равновесие: скорость прямой реакции = скорость обратной реакции
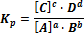
Константа равновесия:
1) природа веществ
2) температура
3) не зависит от С и катализатора
Принцип Ле Шателье
Если на находящуюся в равновесии систему оказать внешне воздействие, то равновесие сместится в сторону, уменьшающую это воздействие.
Биологическое значение:
· действие антидотов при отравлении СО основано на вытеснении СО из НвСО
НвО2 + СО = НвСО + О2
· насыщение венозной крови происходит при повышении давления на кислород (г)
