Материальный баланс процесса адсорбции
Процесс адсорбции проводится периодически или непрерывно. Материальный баланс непрерывной адсорбции: 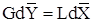 , где G – расход паро-газовой фазы (кг/с инертной части газа); L - расход адсорбента (кг/с);
, где G – расход паро-газовой фазы (кг/с инертной части газа); L - расход адсорбента (кг/с); 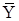 - рабочая концентрация адсорбируемого вещества в паро-газовой фазе (кг/кг ин. части газа);
- рабочая концентрация адсорбируемого вещества в паро-газовой фазе (кг/кг ин. части газа); 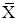 - рабочая концентрация адсорбируемого вещества в адсорбенте.
- рабочая концентрация адсорбируемого вещества в адсорбенте.
Кинетика процесса адсорбции
Экспериментально доказано, что при адсорбции диффузионные сопротивления внутри твёрдой фазы малы по сравнению с внешним диффузионным сопротивлением, поэтому при расчётах процесса адсорбции используют основное уравнение массопередачи в виде: 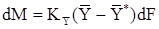 , где с некоторым допущением полагают, что
, где с некоторым допущением полагают, что 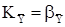 .
. 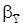 определяют по критериальным уравнениям Nu = f(Re,Pr).
определяют по критериальным уравнениям Nu = f(Re,Pr).
Адсорберы периодического действия с неподвижным слоем адсорбента
Вначале через адсорбент L пропускают паро-газовую смесь G; происходит насыщение адсорбента поглощаемым веществом. Затем пропускают вытесняющее вещество В или нагревают адсорбент (т.е. производят десорбцию – регенерацию адсорбента).
Адсорберы непрерывного действия с движущимся адсорбентом.
Адсорбент L циркулирует в замкнутой системе: насыщение его происходит в верхней зоне аппарата (адсорбционной), регенерация – в нижней (десорбционной).
Кристаллизация
 Кристаллизация – выделение твёрдой фазы в виде кристаллов из растворов или расплавов. Кристаллы – однородные твёрдые тела различной геометрии в зависимости от вида химического соединения. В химической промышленности кристаллизация применяется для получения в чистом виде веществ. Кристаллизацию обычно производят из водных растворов (понижая температуру или удаляя часть растворителя) или из растворов органических веществ, испаряя их. Из расплавов – путём охлаждения. На скорость кристаллизации влияют степень пересыщения раствора, его температура, образование центров кристаллизации, интенсивность перемешивания, наличие примесей и др.
Кристаллизация – выделение твёрдой фазы в виде кристаллов из растворов или расплавов. Кристаллы – однородные твёрдые тела различной геометрии в зависимости от вида химического соединения. В химической промышленности кристаллизация применяется для получения в чистом виде веществ. Кристаллизацию обычно производят из водных растворов (понижая температуру или удаляя часть растворителя) или из растворов органических веществ, испаряя их. Из расплавов – путём охлаждения. На скорость кристаллизации влияют степень пересыщения раствора, его температура, образование центров кристаллизации, интенсивность перемешивания, наличие примесей и др.

| |
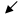
| |

 В начале скорость равна нулю (период индукции), затем максимальна и падает до 0(1) (при большой степени пересыщения). При наличии тормозящих кристаллизацию примесей период индукции возрастает, наблюдается период постоянной скорости (2).
В начале скорость равна нулю (период индукции), затем максимальна и падает до 0(1) (при большой степени пересыщения). При наличии тормозящих кристаллизацию примесей период индукции возрастает, наблюдается период постоянной скорости (2). Влияние температуры – при более высокой температуре уменьшается μ и увеличивается диффузия. Но с повышением температуры растёт число центров кристаллизации и образуются более мелкие кристаллы.
Способы кристаллизации
1) с удалением части растворителя – путём его испарения или вымораживания. Это изотермический метод. Испарение производят в выпарной установке, там же производят и кристаллизацию. Общий недостаток метода – отложение кристаллов на поверхности аппарата.
2) Кристаллизация с изменением температуры раствора - изогидрический способ, осуществляется при постоянном содержании в растворе растворителя. Процесс ведут как в аппарате периодического, так и непрерывного действия. В качестве охладителя используют воду.
3) Комбинированные способы.
а) вакуум-кристаллизация – здесь испарение происходит за счёт отдачи раствором своего физического тепла. Пары откачиваются вакуум-насосом. Процесс протекает адиабатически. Пересыщение раствора достигается его охлаждением;
б) кристаллизация с испарением части растворителя в токе носителя;
в) дробная (фракционированная) кристаллизация.
