Общие правила работы и техника безопасности в химической лаборатории
ЛАБОРАТОРНАЯ РАБОТА 1
ОБЩИЕ ПРАВИЛА РАБОТЫ И ТЕХНИКА БЕЗОПАСНОСТИ В ХИМИЧЕСКОЙ ЛАБОРАТОРИИ
Цель и содержание
Ознакомить студентов с общими правилами работы в химических лабораториях. С первых дней работы в лаборатории студент должен выработать в себе самостоятельность и серьезное отношение ко всем процессам лабораторного эксперимента, что включает теоретическую, практическую подготовку, подготовку химических реактивов, расчет данных и проведение самого опыта.
Теоретическое обоснование
1. Во время работы в химической лаборатории соблюдайте тишину, чистоту и порядок.
2. Не приступайте к работе без разрешения преподавателя.
3. Запрещается работать в лаборатории одному.
4. Работать студент должен на закрепленном за ним рабочем месте.
5. Не допускать попадания химических реактивов на кожу и одежду.
6.Во время работы надевайте халат, а длинные волосы убирайте под косынку.
7. Экономьте реактивы, газ, воду, электричество.
8. Реактивы общего пользования не уносите на свои рабочие места. Если нет указаний по дозировке реактивов для данного опыта, то брать следует их в минимальном количестве.
9. Аккуратно и осторожно обращайтесь с химической посудой, приборами и реактивами. Если посуда разбилась, сдайте ее лаборанту.
10. Для проведения опытов пользуйтесь только дистиллированной водой.
11. Не путайте пробки от склянок с разными реактивами. Сухие реактивы нужно брать только чистым шпателем. Неизрасходованные реактивы не высыпать (не выливать) в те склянки, из которых они взяты.
12. Пользоваться реактивами без этикеток или с сомнительными этикетками категорически запрещается.
13. Не работайте с грязной посудой, сами не оставляйте ее немытой.
14. Не запускайте прибор без предварительной проверки. Не оставляйте прибор без присмотра.
15. Не выносите из лаборатории приборы, реактивы, посуду.
16. Особую осторожность соблюдайте при работе с ядовитыми и вредными веществами: с концентрированными кислотами и щелочами. Работу с ними проводите только в вытяжном шкафу, окна которого должны быть открыты не более чем на одну треть.
17. Не выливайте в раковины остатки кислот, щелочей, огнеопасных жидкостей и т.д. Сливайте эти вещества в специальные склянки, помещенные в вытяжной шкаф. Не бросайте в раковину бумагу, песок , металлы и др. твердые вещества.
18. При нагревании или кипячении жидкости (особенно с осадком) на газовой горелке или спиртовке, во избежание разбрызгивания, нагревайте верхнюю часть пробирки, при этом держа ее отверстием от себя и от работающих рядом.
19. При взвешивании сухих реактивов не высыпайте их прямо на чашку весов. Взвешивайте на часовом стекле или на фильтровальной бумаге.
20. Запрещается курить и принимать пищу в химической лаборатории
21. Не следует вдыхать пахучие вещества, в том числе и выделяющиеся газы, близко наклоняясь к сосуду с этими веществами. Нужно легким движением руки направить струю воздуха от отверстия сосуда к себе и осторожно вдохнуть.
22. Уходя из лаборатории, проверьте, выключены ли газ, вода, электричество.
23. Результаты лабораторной работы оформляют в виде отчета и отдают преподавателю.
Посуда общего назначения
Пробирки.Представляют собой узкие цилиндрической формы сосуды с закругленным дном (рис. 1.1); они бывают различной величины и диаметра и из различного стекла.
Обычные лабораторные пробирки изготавливают из легкоплавкого стекла, но для особых работ, когда требуется нагревание до высоких температур, пробирки изготавливают из тугоплавкого стекла или кварца.
Кроме обычных, простых, пробирок, применяют также градуированные и центрифужные конические пробирки.
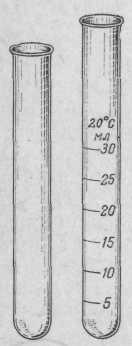
Рисунок 1.1 – Простая и градуированная пробирки
Для хранения пробирок, находящихся в работе, служат специальные деревянные, пластмассовые или металлические штативы (рис.1.2).

Рисунок1.2 – Штатив с пробирками
Пробирки применяют для проведения главным образом аналитических или микрохимических работ. При проведении реакций в пробирке реактивы не следует применять в слишком большом количестве. Совершенно недопустимо, чтобы пробирка была наполнена до краев.
Иногда в пробирку нужно ввести твердое вещество (порошки, кристаллы и т. П.), для этого применяют микрошпатель, которым отбирают нужное количество твердого вещества. Пробирку держат в левой руке, наклонив ее горизонтально, и вводят в нее микрошпатель почти до дна (рис. 1.3). Затем пробирку ставят вертикально и слегка ударяют по ней рукой. Когда все твердое вещество высыпается, микрошпатель вынимают.

Рисунок 1.3 – Внесение в пробирку порошкообразных веществ
Для перемешивания налитых реактивов пробирку держат большим и указательным пальцами левой руки за верхний конец и поддерживают ее средним пальцем, а указательным пальцем правой руки ударяют косым ударом по низу пробирки. Этого достаточно, чтобы содержимое ее было хорошо перемешано. Совершенно недопустимо закрывать пробирку пальцем и встряхивать ее в таком виде; при этом можно не только ввести что-либо постороннее в жидкость, находящуюся в пробирке, но иногда и повредить кожу пальца, получить ожог и пр. Если пробирка наполнена жидкостью больше чем на половину, содержимое перемешивают стеклянной палочкой.
Если пробирку нужно нагреть, ее следует зажать в держателе (рис. 1.4). При неумелом и сильном нагревании пробирки жидкость быстро вскипает и выплескивается из нее, поэтому нагревать нужно осторожно. Когда начнут появляться пузырьки, пробирку следует отставить и, держа ее не в пламени горелки, а около него или над ним, продолжать нагревание горячим воздухом. При нагревании открытый конец пробирки должен быть обращен в сторону от работающего и от соседей по столу.
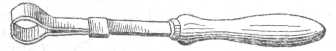
Рисунок 1.4 – Держатель для пробирок
Воронки.Служат для переливания жидкостей, для фильтрования и т. Д. Химические воронки выпускают различных размеров, верхний диаметр их составляет 35, 55, 70, 100, 150, 200, 250 и 300 мм.
При работе воронки устанавливают или в специальном штативе, или в кольце на обычном лабораторном штативе (рис. 1.5).
При переливании жидкости в бутыль или колбу не следует наполнять воронку до краев.
Если воронка плотно прилегает к горлу сосуда, в который переливают жидкость, то переливание затрудняется, так как внутри сосуда создается повышенное давление. Поэтому воронку время от времени нужно приподнимать.

Рисунок 1.5 – Штатив с укреплёнными в специальных держателях воронками
Еще лучше сделать между воронкой и горлом сосуда щель, вложив между ними, например, кусочек бумаги. При этом нужно следить, чтобы прокладка не попала в сосуд.
Химические стаканыпредставляют собой цилиндры различной емкости. Так же как и другую химическую посуду, стаканы делают из фарфора (рис. 1.6) и из химически стойкого стекла (рис. 1.7). Они бывают: с носиками и без носиков, фарфоровые стаканы – с ручками и без ручек, стеклянные – с делениями для приблизительного измерения объёма или без делений.
Нагревать стаканы из обычного стекла на голом пламени нельзя – от этого они лопаются. Нагревание следует проводить только через асбестированную сетку или на водяной либо другой бане.

Рисунок 1.6 – Фарфоровые кружки и стаканы

Рисунок 1.7 – Стеклянные стаканы
Плоскодонные колбы.Бывают самой разнообразной емкости (рис.1.8), начиная от 50 мл и до нескольких литров, со шлифом и без шлифа на горле. Их изготовляют из обычного, а также из кварцевого и специальных сортов стекла.

Рисунок 1.8 – Плоскодонные колбы
Конические колбы(Эрленмейера). Находят широкое применение при аналитических работах (титрование). Они бывают различной емкости, с носиками и без носиков, узкогорлые и широкогорлые (рис. 1.9).

Рисунок 1.9 – Конические колбы
Нагревать колбы следует только через асбестированную сетку или на какой-либо бане.
Мерная посуда
Мерной называют посуду, применяемую для измерения объема жидкости.
Мерные цилиндры.Представляют собой стеклянные толстостенные сосуды с нанесенными на наружной стенке делениями, указывающими объем в миллилитрах (рис. 1.10 а). Они бывают самой разнообразной емкости: от 5—10 млдо 1 л и больше. Чтобы отмерить нужный объем жидкости, ее наливают в мерный цилиндр до тех пор, пока нижний мениск не достигнет уровня нужного деления.

а б
Рисунок 1.10 — Мерные цилиндры (а) и мензурки (б)
Кроме цилиндров, для той же цели употребляют мензурки (рис. 1.10 б). Это сосуды конической формы, на стенке которых имеются деления. Они очень удобны для отстаивания мутных жидкостей, когда осадок собирается в нижней, суженной части мензурки.
Пипетки.Служат для точного отмеривания определенного объема жидкости. Различают пипетки для жидкостей и газовые пипетки.
Пипетки для жидкостей (рис. 1.11). Обычные пипетки (пипетки Мора) представляют собой стеклянные трубки небольшого диаметра с расширением посредине. Нижний конец пипетки слегка оттянут и имеет диаметр около 1 мм.
Пипетки бывают емкостью от 1 до 100 мл,в верхней части их имеется метка, до которой набирают жидкости. Широко применяют также градуированные пипетки различной емкости, на наружной стенке которых нанесены деления в 0,1 мл.
Для наполнения пипетки нижний конец ее опускают в жидкость и втягивают последнюю при помощи груши или ртом, но лучше при этом пользоваться специальными приспособлениями.
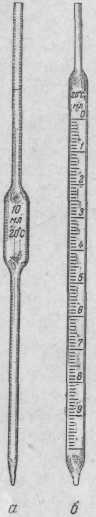
Рисунок 1.11 – Пипетки: а – простая (пипетка Мора), б – градуированная
Жидкость набирают так, чтобы она поднялась на 2—3 смвыше метки, затем быстро закрывают верхнее отверстие, указательным пальцем правой руки, придерживая в то же время пипетку большим и средним пальцами. Очень полезно указательный палец слегка увлажнить, так как влажный палец более плотно закрывает пипетку.
Когда пипетка наполнена, ослабляют нажим указательного пальца, в результате чего жидкость будет медленно вытекать из пипетки; как только нижний мениск жидкости окажется на одном уровне с меткой, палец снова прижимают. Если на конце пипетки после этого будет висеть капля, ее следует осторожно удалить. Введя пипетку в сосуд, отнимают указательный палец и дают жидкости стечь по стенке сосуда. После того как жидкость вытечет, пипетку держат в течение еще 5 сек (считая до 5) прислоненной к стенке сосуда, слегка поворачивая вокруг оси, после чего удаляют пипетку, не обращая внимания на оставшуюся в ней жидкость.
При выливании раствора из пипетки в коническую колбу очень важно, чтобы раствор стекал именно по стенке конической колбы и не разбрызгивался, так как при этом часть выливаемого раствора может попасть на стенку колбы и при последующем титровании не вступит в реакцию с раствором, выливаемым из бюретки.
Никогда не следует стремиться выгонять остатки жидкости из пипетки выдуванием или нагреванием рукой расширенной части пипетки.
Для отмеривания малых объемов жидкостей применяют микропипетки емкостью 1, 2, 3 и 5 мл.Микропипетки часто градуируют, они имеют деления в 0,01 мл,что позволяет делать отсчет с точностью 0,002— 0,005 мл.
Градуированной пипеткой можно отбирать не только один определенный объем жидкости (как обыкновенными пипетками), но любой в пределах ее емкости. Жидкость набирают в пипетку до нужной метки (нижний мениск жидкости находится на уровне последней) и затем выливают ее, как обычно.
Пипетки должны быть всегда чисто вымытыми; их следует ставить в особый штатив (рис. 1.12) и закрывать сверху маленькими пробирками или куском чистой фильтровальной бумаги. Если штатива в лаборатории нет, пипетки можно хранить в стеклянном цилиндре, на дно которого предварительно кладут несколько слоев чистой фильтровальной бумаги, вырезанной кружками. После работы пипетку ополаскивают несколько раз дистиллированной водой и помещают в стеклянный цилиндр, каждый раз заменяя верхний слой фильтровальной бумаги свежим. Обычными пипетками нельзя отмерять жидкости, вязкость которых заметно отличается от вязкости воды, например, концентрированные кислоты, щелочи и т. П., так как объем отобранной жидкости не будет соответствовать указанному. Для отбора таких жидкостей пользуются специально прокалиброванными пипетками.

Рисунок 1.12 – Штативы для пипеток
При обращении со всеми видами пипеток нужно обязательно придерживаться следующих правил:
1. Пипетка при отборе жидкостивсегда должна находиться в строго вертикальном положении.
2.При установке нижнего мениска на уровне черты глаз наблюдателя должен быть расположен в одной плоскости с меткой (метки на передней и задней стенках должны при этом сливаться в одну).
Бюретки.Применяют при титровании, для измерения точных объемов и пр. Различают бюретки объемные, весовые, поршневые, микробюретки и газовые.
Объемные бюретки. Это — стеклянные трубки с несколько оттянутым нижним концом или снабженные краном. На наружной стенке по всей длине бюретки нанесены деления в 0,1 мл,так что отсчеты можно вести с точностью до 0,02 мл.
Бюретки (рис. 1.13) бывают двух типов: с притертым краном (б) и бескрановые с оттянутым концом (а),к которому посредством резиновой трубки присоединяют оттянутую в капилляр стеклянную трубку; резиновую трубку зажимают зажимом Мора.

Рисунок 1.13 – Бюретки объемные
Резиновая трубка должна иметь стенку толщиной не менее 1,5 мм,а внутренний диаметр — около 3 мм.Таким образом, наружный диаметр резиновой трубки – около 6 мм.
В бюретки с краном можно наливать все жидкости за исключением щелочей, которые могут вызывать заедание притертого крана. Для работы со щелочами применяют бескрановые бюретки с резиновой насадкой.
Для работы в учебных лабораториях или в тех случаях, когда титрование проводят редко, и при всех временных работах бюретки укрепляют на лабораторных штативах в лапках (рис. 1.14).

Рисунок 1.14 – Штатив с бюретками
Так как бюретки предназначены для очень ответственной работы — титрования, их следует содержать в особенной чистоте.
После работы бюретку следует вымыть водой и оставить ее в штативе, перевернув открытым концом вниз. Чтобы в бюретку не попадала пыль, ее лучше заткнуть кусочком ваты. У бюреток с краном нужно вынуть кран, обернуть его один раз куском чистой фильтровальной бумаги и снова вставить в бюретку. Если этого не сделать, шлиф может испортиться и кран будет протекать.
Бюретку устанавливают на нуль только после того, как работающий убедится, что в капилляре или кончике бюретки не осталось пузырьков воздуха (рис. 1.15).
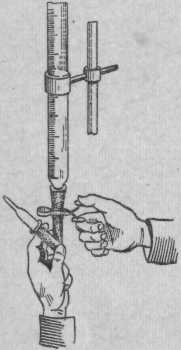
Рисунок 1.15 – Удаление воздуха из кончика бюретки
Бюретку следует заполнять так, чтобы вначале уровень жидкости был несколько выше нулевого деления шкалы (до 3–4 см).Затем, осторожно приоткрывая кран, аккуратно устанавливают уровень жидкости на нулевое деление. Каждое титрование следует начинать только после заполнения бюретки до нуля. Уровень жидкости прозрачных растворов устанавливают по нижнему мениску, а непрозрачных – по верхнему.
Мерные колбы. Необходимая посуда для большинства аналитических работ (рис. 1.16); они представляют собой плоскодонные колбы различной емкости; в большинстве случаев мерные колбы имеют пришлифованные стеклянные пробки. Однако часто применяют мерные колбы без пришлифованных стеклянных пробок. В таких случаях для закрывания мерных колб используют резиновые пробки соответствующего размера.

Рисунок 1.16 – Мерные колбы
Различают узкогорлые и широкогорлые мерные колбы. Диаметр горла последних приблизительно в полтора раза больше по сравнению с узкогорлыми. На горле колбы имеется кольцевая метка, а на самой колбе вытравлено число, указывающее ее емкость в миллилитрах при определенной температуре. Приведенная емкость означает, что при данной температуре объем воды, налитой в колбу до метки, точно соответствует указанному. Объем вылитой из колбы воды будет несколько меньше помеченного, так как часть ее останется на стенках. Поэтому обычные мерные колбы не пригодны для отмеривания точного объема воды с последующим выливанием ее.
Содержание отчета и его форма
Каждый студент должен иметь лабораторный журнал, который является документом, отражающим всю его работу.
Все наблюдения и выводы по экспериментальной работе, проделанной в лаборатории, студент заносит в лабораторный журнал непосредственно после ее выполнения в виде отчета.
Дата____________
ЛАБОРАТОРНАЯ РАБОТА 2
Аппаратура и материалы
Прибор для определения эквивалента металла. Аналитические весы. Термометр. Барометр. Мензурка на 25-50 мл. Стаканчик химический вместимостью 50 мл. Воронка с длинным концом. Фильтровальная бумага. Навеска металла (х.ч.) около 0,1 г. Раствор соляной кислоты 2н.
Содержание отчета и его форма
Все наблюдения записать в лабораторный журнал. Сделать схематический рисунок прибора. Результаты измерений записать по следующей форме:
Масса металла, m, г
Объем выделившегося водорода, V, мл
Температура, T, К
Атмосферное давление, Р, Па
Давление насыщенного водяного пара при данной температуре Р(Н2О), Па.
Парциальное давление водорода, Р(Н2)=Р- Р(Н2О)
Рассчитать эквивалентную массу металла двумя способами:
1. Вычислить массу вытесненного водорода по уравнению Клапейрона-Менделеева. На основании закона эквивалентов вычислить массу эквивалента данного металла.
2. Привести объем выделившегося водорода к нормальным условиям по уравнению Клапейрона. Зная объем эквивалента водорода, расчитать массу эквивалента металла.
Расчеты и наблюдения.
Дата___________
ЛАБОРАТОРНАЯ РАБОТА 3
Аппаратура и материалы
Штатив с пробирками. Секундомер. Водяная баня (с крышкой имеющей отверстия для пробирок) - 2 шт. Термометр на 50 °С. Стеклянная палочка. Пипетки капельные. Фильтровальная бумага. Шпатель. Реактивы кристаллические: карбонат кальция (мел), хлорид калия. Реактивы концентрированные: хлороводородной кислоты (плотность 1,19 г /см3).Вода дистиллированная. Растворы: тиосульфата натрия (0,5 н.), серной кислоты (0,5 н.), хлорида железа (III) (0,5 н., насыщ.), роданида калия (0,5 н., насыщ.), сульфата меди (0,5 н.).
ЛАБОРАТОРНАЯ РАБОТА 4
Аппаратура и материалы
Весы технохимические. Часовое стекло (или лоток из вощеной бумаги). Шпатель (или ложка). Цилиндры мерные на 25, 50, 100, 250 мл. Колбы плоскодонные на 250 мл (или более). Химические стаканы на 50 (или 100 мл). Бюретки на 25 мл с штативами. Пипетки Мора на 10мл. Кристаллические реактивы: карбонат натрия. Вода дистиллированная. Индикаторы: фенолфталеин (р-р), метиловый оранжевый (р-р). Стандартный раствор хлороводородной кислоты (0,1 н).
Содержание отчета и его форма
Каждый студент должен иметь лабораторный журнал, который является документом, отражающим всю его работу. Все наблюдения и выводы по экспериментальной работе, проделанной в лаборатории, студент заносит в лабораторный журнал непосредственно после ее выполнения.
Отчет по лабораторной работе должен состоять из даты, названия и номера лабораторной работы, цели работы, методики проведения опытов, наблюдений, уравнений химических реакций, выводов и расчетов (формулы, таблицы, графики).После методики каждого опыта должна следовать таблица результатов по указанной форме (табл.4.2-4.4) и далее расчётные формулы с вычислениями.
Таблица 4.5. Варианты заданий
| Вариант | Данные для приготовления раствора Na2CO3 | ||||
| Раствор №1 | Раствор №2 | ||||
| ω, % | ρ, г/мл | V, мл | С, моль/л | V, мл | |
| 1,019 | 0,10 | ||||
| 1,039 | 0,11 | ||||
| 1,060 | 0,16 | ||||
| 1,081 | 0,18 | ||||
| 1,019 | 0,09 | ||||
| 1,039 | 0,12 | ||||
| 1,060 | 0,17 | ||||
| 1,081 | 0,19 |
Таблица 4.6. Варианты заданий
| Вариант | Индикатор для титрования |
| метилоранж | |
| метилоранж | |
| фенолфталеин | |
| фенолфталеин | |
| метилоранж | |
| метилоранж | |
| фенолфталеин | |
| фенолфталеин |
Дата____________
ЛАБОРАТОРНАЯ РАБОТА 5
Аппаратура и материалы
Калориметр, технические весы, цилиндры мерные, стеклянные пипетки, термометр (100-150оС), мешалка, дистиллированная вода, штатив, фильтровальная бумага, воронка, шпатель, пробка, секундомер, 1 н. растворы NaOH и HCl, негашеная известь (СаО).
Содержание отчета и его форма
Каждый студент должен иметь лабораторный журнал, который является документом, отражающим всю его работу. Все наблюдения и выводы по экспериментальной работе, проделанной в лаборатории, студент заносит в лабораторный журнал непосредственно после ее выполнения.
Отчет по лабораторной работе должен состоять из даты, названия и номера лабораторной работы, цели работы, методики проведения опытов, наблюдений, уравнений химических реакций, выводов и расчетов (формулы, таблицы, графики).
Дата___________
ЛАБОРАТОРНАЯ РАБОТА 6
Аппаратура и материалы
Штатив с пробирками, микрошпатель, стеклянные пипетки, универсальный индикатор, водяная баня, дистиллированная вода, 1 н. растворы СН3СООН, HCl, NaOH, NaHCO3, FeCl3, СН3СООNa, Al2(SO4)3, Na2СO3, растворы индикаторов метилового оранжевого, лакмуса и фенолфталеина, цинк металлический, кристаллические соли: СН3СООNa, Al2(SO4)3, Na2СO3, NaCl, Na2SO3. Растворы: хлороводородной кислоты (2 н.); уксусной кислоты (2 н.); аммиака (10%-ного); хлорида натрия(0,5 н.); хлорида кальция (0,5 н.); иодида калия (0,5 н.); нитрата серебра (1,0 н.); хромата калия (0,5 н.); оксалата аммония (0,5 н.); сульфида аммония; хлорид бария (0,5 н.); бромид натрия (0,5 н.).
Опыт 3. Дробное осаждение
В двух пробирках получите раздельно хлорид и хромат серебра взаимодействием растворов хлорида натрия ( NaCl ) и хромата калия (K2CrO4) с нитратом серебра (AgNO3), взяв по 2-4 капли каждого раствора. Напишите
ионные уравнения реакций, отметьте цвета осадков и запишите величину произведения растворимости для хлорида и хромата серебра. Какая соль менее растворима? Какое вещество будет выпадать в осадок в первую очередь из раствора, содержащего ионы Cl- , CrO42-, Ag+ в равных концентрациях? Проверьте предположение опытом. Для этого внесите в одну пробирку по 2-3 капли растворов NaCl и K2CrO4, добавьте 5-6 капель воды и перемешайте растворы. Осторожно, по каплям (1-2 капли) прибавьте в него раствор AgNO3. Что наблюдается? С какими ионами в первую очередь реагируют ионы серебра? Какое вещество при этом образуется? Добавьте в раствор еще несколько капель нитрата серебра. Наблюдается ли образование хлорида серебра? Отметьте начало его образования при дальнейшем увеличении концентрации иона серебра. Объясните последовательность образования осадков в данном опыте, учитывая величины произведений растворимости хлорида и хромата серебра.
Наблюдения:
Выводы:
Осадителями
Получите осадок оксалата бария (BaС2O4) взаимодействием 4 капель раствора хлорида бария (BaCl2) и 6 капель оксалата аммония ((NH4)2C2O4). Дайте раствору отстояться и прозрачный раствор перенесите пипеткой в две чистые пробирки по 3-4 капли в каждую. В одну из них добавьте 1-2 капли раствора (NH4)2C2O4, чтобы убедиться в полноте осаждения иона бария по отношению к ионам оксалата аммония. В другую пробирку добавьте 3-4 капли раствора K2CrO4. Какое вещество выпадает в осадок? Напишите ионные уравнения протекающих реакций. Укажите величины произведений растворимости оксалата и хромата бария и объясните образование осадка ВаСrO4 после удаления из раствора ионов бария в виде ВаС2O4. Каким из примененных реактивов наиболее полно удаляются ионы бария из раствора?
Наблюдения:
Выводы:
На растворение осадков
В трех пробирках раздельно получите осадки хлорида, бромида и иодида серебра взаимодействием растворов соответствующих солей с нитратом серебра (по 2-3 капли каждого реактива). Отметьте цвет осадков. К осадкам в каждую пробирку добавьте по несколько капель раствора аммиака. Размешайте содержимое пробирок. В растворе аммиака наблюдается растворение осадков с образованием комплексного иона [Ag(NH3)2]+. Напишите уравнения реакций образования осадков и выражения произведений растворимости для хлорида, бромида и иодида серебра (указать их числовые значения). Почему бромид серебра растворяется в аммиаке медленнее, чем хлорид, а иодид серебра практически нерастворим в аммиаке?
Наблюдения:
Выводы:
ЛАБОРАТОРНАЯ РАБОТА 7
ГИДРОЛИЗ СОЛЕЙ
Цель и содержание
Теоретически и экспериментально изучить процессы гидролиза солей и влияние различных факторов на процесс протекания гидролиза.
Аппаратура и материалы
Штатив с пробирками. Пипетки капельные. Микрошпатель. Вода дистиллированная. Реактивы кристаллические: хлорид олова (II). Индикаторы: лакмус (р-р), фенолфталеин (р-р). Растворы: хлороводородной кислоты (0,5 н.), ацетата натрия (0,5 н.), сульфата алюминия (0,5 н.), хлорида натрия (0,5 н.), ацетат аммония (0,5 н.), сульфита натрия (0,5 н.), карбоната натрия (0,5 н.), сульфида натрия (0,5 н.), хлорида железа (III)(0,5 н.).
Гидролиза
В одну пробирку внести 2-3 мл раствора карбоната натрия (Na2CO3),а во вторую столько же раствора сульфита натрия (Na2SO3).В каждую пробирку добавить по одной капле фенолфталеина.
Запись данных опыта. Написать уравнения гидролиза карбоната и сульфита натрия (по первой ступени). В растворе какой соли окраска фенолфталеина более интенсивна? Степень гидролиза какой соли больше? Объяснить почему?
Наблюдения и уравнения:
Выводы:
ЛАБОРАТОРНАЯ РАБОТА 8
Приборы и реактивы
Штатив с пробирками; стеклянные пипетки, фильтровальная бумага, наждачная бумага, железные гвозди, дистиллированная вода.
Жидкие реактивы: CuSO4, I2, свежеприготовленные 0.5 н. растворы Na2SO3, KMnO4, H2SO4, NaOH, KNO2, K2Cr2O7,соль Мора FeSO4, FeCl3 или Fe2(SO4)3, KI, раствор крахмала.
Выводы
ЛАБОРАТОРНАЯ РАБОТА 9
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
Цель и содержание
Получение комплексов различного типа. Изучение строения комплексных ионов и их свойств.
Приборы и реактивы
Штатив с пробирками, пипетки капельные, микрошпатель, универсальная индикаторныя бумага, вода дистиллированная.
Жидкие реактивы: раствор аммиака (25%), сульфата цинка (0,5 н.), сульфата никеля (0,5 н.), сульфата меди (II) (0,5 н.), сульфата алюминия (0,5 н.), хлорида хрома (III) (0,5 н.), хлорида бария (0,5 н.), раствор аммиака (2 н.), гидроксида натрия (2 н.), сульфида натрия (0,5 н.), гексацианоферрата (III) калия (0,5 н.).
Сухие реактивы: гранулы олова, соль Мора.
Опыт 1. Анионные комплексы
Анионными в частности являются гидроксокомплексы. Для их получения в три пробирки раздельно поместите растворы солей цинка, хрома (III) и алюминия. В каждую из них добавьте по каплям раствор щёлочи. Наблюдайте вначале выпадение осадков по ионным реакциям типа
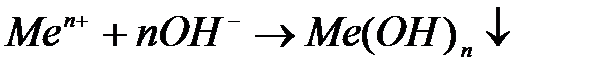 ,
,
а затем их растворение в избытке щёлочи с образованием растворимых гидроксокомплексов
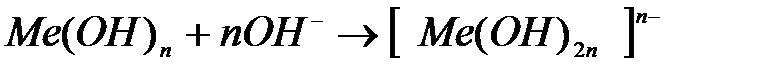 .
.
Запись данных опыта. Напишите уравнения всех проделанных реакций. Гидроксиды каких металлов способны образовывать такие анионные комплексы?
Наблюдения и уравнения:
Выводы:
Опыт 2. Катионные комплексы
Катионными комплексами в частности являются аммиакаты. Для получения аммиаката никеля внесите в пробирку 3–4 капли сульфата никеля (NiSO4)и такой же объём раствора гидроксида натрия (NaOH).Образуется осадок гидроксида никеля (II). Аккуратно слейте раствор, из пробирки оставив осадок. Остатки жидкой фазы можно удалить полоской фильтровальной бумаги.
К осадку добавьте 5–6 капель концентрированного раствора аммиака. Тщательно перемешайте до полного растворения осадка. В отдельную пробирку поместите несколько капель раствора сульфата никеля и сравните его окраску с окраской раствора гидроксида гаксаамминникеля (II) полученного по реакции
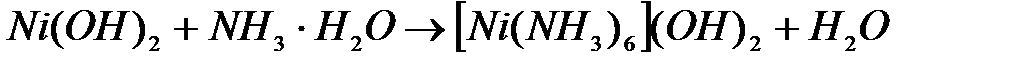 .
.
Запись данных опыта. Напишите уравнения проведённых реакций. Какое основание является более сильным: простое или комплексное? Ответ обоснуйте.
Наблюдения и уравнения:
Выводы:
ЛАБОРАТОРНАЯ РАБОТА 10
ОБЩИЕ СВОЙСТВА МЕТАЛЛОВ
Цель и содержание
Ознакомится с характерными свойствами различных металлов и их соединений. Провести качественное определение металлов.
Приборы и реактивы
Пробирки, газовая горелка, держатели пробирок, синяя лакмусовая бумага.
Жидкие реактивы: соляная кислота (2 н.), серная кислота (2 н.), азотная кислота (2 н. и 2%), концентрированная серная кислота, концентрированный раствор щелочи, раствор нитрата свинца (2 н.), растворы солей цинка, железа (II), олова, меди (II), серебра.
Сухие реактивы: алюминий металлический, магний металлический, железные опилки, олово, медная стружка, цинк металлический.
ЛАБОРАТОРНАЯ РАБОТА 11
Приборы и реактивы
Штатив с пробирками, фарфоровый тигель.
Жидкие реактивы: раствор серной кислоты (2 н.), раствор соляной кислоты, азотная кислота (конц.), раствор гексацианоферрата калия K3[Fe(CN)6], раствор уксусной кислоты, 5% раствор KI, цинк.
Сухие реактивы: медная проволока, оцинкованное и луженое железо, железные гвозди, свинец.
Выводы
Опыт 4. Протекторная защита
1. В две пробирки с раствором разбавленной уксусной кислоты прилейте несколько капель 5% раствора КI.
2. В одну пробирку опустите кусочек свинца, а в другую - кусочки свинца и цинка так, чтобы они соприкасались.
Запись данных опыта. Наблюдайте, где быстрее будет разрушаться свинец (там где быстрее появится желтый осадок, так как ионы I- играют роль индикатора на ионы Pb2+, образуя с ним малорастворимое соединение иодид свинца PbI2). Составьте схему действия гальванопары Pb-Zn. Какой металл играет роль протектора?
Наблюдения и уравнения:
Выводы:
Содержание отчета и его форма
Каждый студент должен иметь лабораторный журнал, который является документом, отражающим всю его работу. Все наблюдения и выводы по экспериментальной работе, проделанной в лаборатории, студент заносит в лабораторный журнал непосредственно после ее выполнения.
Отчет по лабораторной работе должен состоять из даты, названия и номера лабораторной работы, цели работы, методики проведения опытов, наблюдений, уравнений химических реакций, выводов и расчетов (формулы, таблицы, графики).
Дата__________
ЛАБОРАТОРНАЯ РАБОТА 12
Приборы и реактивы
Стеклянная коническая колба для титрования объемом 250 мл – 3 шт., мерный цилиндр на 100 мл, стеклянные пипетки, штатив с бюреткой на 25 мл, химический стакан, метиловый оранжевый.
Жидкие реактивы: раствор HCl (0,1 н.), водопроводная вода.
ЛАБОРАТОРНАЯ РАБОТА 13
Приборы и реактивы
Штатив с пробирками, держатель пробирок.
Жидкие реактивы: 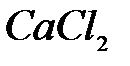 ,
, 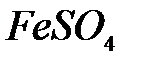 ,
, 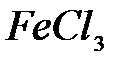 ,
, 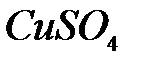 ,
, 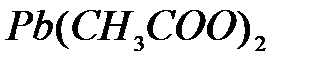 ,
, 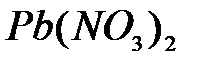 ,
, 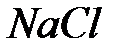 ,
, 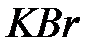 ,
, 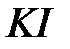 ,
, 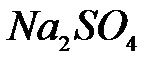 ,
, 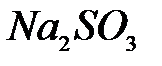
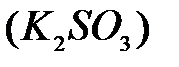 ,
, 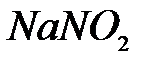
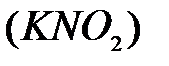
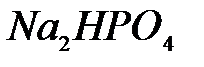 ,
, 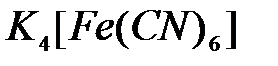 ,
, 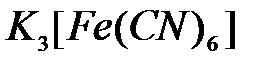 ,
, 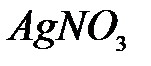 ,
, 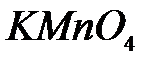 ,
, 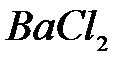 ,
, 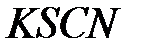 ,
, 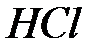 ,
, 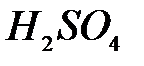 ,
, 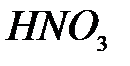 ,
, 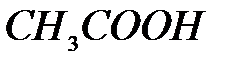 .
.
Порошкообразные реактивы: 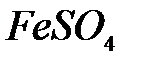 .
.
Содержание отчета и его форма
Каждый студент должен иметь лабораторный журнал, который является документом, отражающим всю его работу. Все наблюдения и выводы по экспериментальной работе, проделанной в лаборатории, студент заносит в лабораторный журнал непосредственно после ее выполнения.
Отчет по лабораторной работе должен состоять из даты, названия и номера лабораторной работы, цели работы, методики проведения опытов, наблюдений, уравнений химических реакций, выводов и расчетов (формулы, таблицы, графики).
Приложение.
Таблица 1 – Константы диссоциации некоторых слабых электролитов в водных растворах при 25˚С
| Химическая формула | Название электролита | Константа диссоциации |
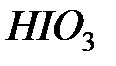 | Йодноватая кислота | 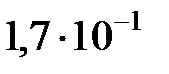 |
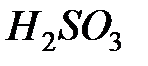 | Сернистая кислота | 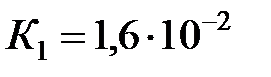 |
