Фазовое равновесие в системе жидкость - пар.
Принцип ректификации.
Сущность процесса ректификации можно охарактеризовать как разделение жидкой смеси на дистиллят и остаток в результате двухступенчатого взаимодействия жидкости с парами.
Материальный баланс разделения:
Для всей смеси:
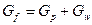
Для легколетучего компонента в смеси:
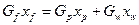
Флегмовое число – отношение количества возвращённого в колонну дистиллята (флегмы) к количеству отобранного дистиллята в виде продукта.
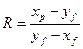 ,
,
где 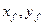 - исходная смесь,
- исходная смесь, 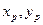 - итоговая смесь.
- итоговая смесь.
Разделение смеси при ректификации возможно в результате взаимодействия потоков паров и жидкостей в ректификационном аппарате при кратности испарения 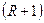 и кратности конденсации
и кратности конденсации 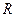 .
.
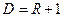
или
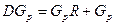
Материальный баланс ректификации по летучему компоненту:
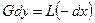
С уменьшением флегмового числа и, следовательно, затрат тепла на провеение процесса уменьшается движущая сила, и наоборот.
Тепловой баланс процесса ректификации.
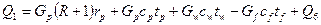 ,
,
где 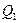 - тепло, поступающее в кипятильник ректификационного аппарата с греющим паром, в ккал/ч;
- тепло, поступающее в кипятильник ректификационного аппарата с греющим паром, в ккал/ч; 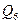 - тепло, теряемое в окружающую среду, в ккал/ч;
- тепло, теряемое в окружающую среду, в ккал/ч; 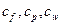 - теплоёмкости соответственно исходной смеси, дистиллята и остатка в ккал/(кг·град);
- теплоёмкости соответственно исходной смеси, дистиллята и остатка в ккал/(кг·град); 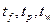 - температура исходной смеси, дистиллята и остатка в °С;
- температура исходной смеси, дистиллята и остатка в °С; 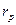 - теплота испарения дистиллята в ккал/кг.
- теплота испарения дистиллята в ккал/кг.
Если нагревание в кипятильнике производится водяным паром расход его на проведение процесса составит:
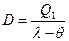 ,
,
где 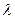 - энтальпия водяного пара в ккал/кг,
- энтальпия водяного пара в ккал/кг, 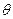 - температура конденсата в °С.
- температура конденсата в °С.
Расход тепла на ректификацию резко уменьшается с ростом концентрации исходного вещества в разделяемой смеси.
РАЗДЕЛ 3
ЭКСТРАКЦИЯ
Экстракция – извлечение одного или нескольких растворённых веществ из одной жидкой фазы другой, практически не смешивающейся с первой.
Процесс широко используется для извлечения ценных продуктов из разбавленных растворов, а также для получения концентрированных растворов. Но главное, экстракцию следует рассматривать, наряду с ректификацией, как один из основных способов разделения жидких однородных смесей.
1. Равновесие в процессах экстракции.
Равновесие для некоторых систем «жидкость – распределяемое вещество – жидкость» следует так называемому закону распределения. Согласно этому закону отношение равновесных концентраций распределённого между двумя жидкими фазами вещества при постоянной температуре есть величина постоянная, она называется коэффициентом распределения.
Пусть распределяющими фазами являются 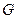 и
и 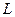 , а равновесными концентрациями будут
, а равновесными концентрациями будут 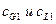 ,
, 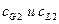 , …
, … 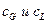 , тогда по закону распределения:
, тогда по закону распределения:
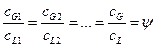 (14.1)
(14.1)
или
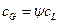 (14.2),
(14.2),
где 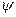 - коэффициент распределения.
- коэффициент распределения.
В уравнении (14.2) концентрации выражены в кг/м3. Если обозначить концентрации распределяемого в фазах вещества через 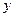 и
и 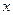 (в кг/кг инертного вещества (растворителя)) и обозначить плотности фаз
(в кг/кг инертного вещества (растворителя)) и обозначить плотности фаз 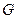 и
и 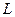 через
через 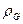 и
и 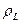 , уравнение (14.2) примет вид:
, уравнение (14.2) примет вид:
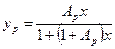 (14.3),
(14.3),
где
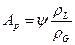 (14.4)
(14.4)
Произведением 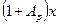 при малых концентрациях
при малых концентрациях 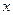 можно пренебречь, поэтому допустимо принимать:
можно пренебречь, поэтому допустимо принимать:
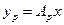
2. Материальный баланс экстракции.
Уравнение материального баланса по общим потокам:
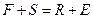 (14.10),
(14.10),
где 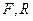 - соответственно весовые количества исходного раствора и полученного рафината в кг/ч;
- соответственно весовые количества исходного раствора и полученного рафината в кг/ч; 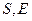 - соответственно весовые количества экстрагента и полученного экстракта в кг/ч.
- соответственно весовые количества экстрагента и полученного экстракта в кг/ч.
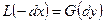
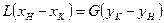
РАЗДЕЛ 4
АДСОРБЦИЯ
Адсорбция – поглощение газов или паров из газовых смесей или растворённых веществ из растворов твёрдыми поглотителями, называемыми адсорбентами.
Особенностью процессов адсорбции являются избирательность и обратимость. Благодаря этой особенности процесса возможно поглощение из паро-газовых смесей или растворов одного или нескольких компонентов, а затем в других условиях, десорбирование их, то есть выделение нужного компонента из твёрдой фазы в более или менее чистом виде.
Адсорбция широко распространена в различных отраслях химической технологии как метод разделения смесей. В качестве конкретных примеров можно указать выделение бензола из паро-газовых смесей, разделение смесей газообразных углеводородов, сушку воздуха, очистку жидких нефтепродуктов от распространённых в них примесей и т.д.
