Vii спектральные методы анализа
Спектральные методы анализа основаны на взаимодействии электромагнитного излучения с веществом. Это взаимодействие сопровождается явлениями, из которых наиболее важны испускание, поглощение и рассеяние излучения. Возникающие сигналы несут качественную и количественную информацию о веществе. Качественную информацию несет частота сигнала (интенсивное свойство), связанная с природой вещества, количественную – интенсивность сигнала (экстенсивное свойство), зависящая от его количества.
В зависимости от используемого диапазона электромагнитного излучения и соответствующего ему физического процесса, спектральные методы анализа классифицируют на следующие виды:
· Радиочастотная спектроскопия (ЯМР, ЭПР – изменение спинов ядер и электронов) – l = 101-10-1 м;
· Микроволновая спектроскопия (изменение вращательных состояний) – l = 10-1-10-3 м;
· Оптическая спектроскопия (изменение состояний валентных электронов): ультрафиолетовая – l = 400-200 нм, видимая – l = 750-400 нм;
· Инфракрасная спектроскопия (ИК, КР – изменение колебательных состояний) – l = 10-3-10-6 м;
· Рентгеновская спектроскопия (изменение состояний внутренних электронов) – l = 10-8-10-10 м;
· Спектроскопия гамма-излучения (ядерные реакции) – l = 10-10-10-13 м.
Совокупность всех частот (длин волн) электромагнитного излучения называют электромагнитным спектром. Поток фотонов с одинаковой частотой называют монохроматическим излучением, с разными частотами – полихроматическим.
Непосредственное отношение к спектроскопическим методам анализа имеет строение атомов и молекул.
Энергетическое состояние каждого электрона в атоме описывается набором четырех квантовых чисел: главного, побочного, магнитного и спинового.
При изменении хотя бы одного квантового числа электрон, а, следовательно, и атом, получает или отдает энергию. Такое явление может произойти при взаимодействии атома с электромагнитным полем, при непосредственном обмене энергией с другими атомами или молекулами, например при столкновениях или при химических реакциях. В отсутствии внешних воздействий атом находится в основном состоянии, т.е. обладает наименьшей энергией. При получении энергии извне атом переходит в возбужденное состояние.
Атом не может получить или отдать любое количество энергии. Энергетический обмен осуществляется только конечными порциями, квантами электромагнитной энергии. Таким образом, атом может находиться только в определенных энергетических состояниях, отличающихся друг от друга на определенную величину (рис.1).
|

|
|
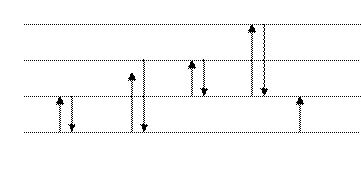
Рис. 1. Энергетические переходы в атоме:
Один атом за один акт поглощает или испускает только один фотон с определенной энергией (частотой). Вещество состоит из множества одинаковых атомов, способных переходить на разные энергетические уровни, испуская или поглощая фотоны разных частот. Совокупность всех фотонов одной и той же частоты составляет спектральную линию. Совокупность всех спектральных линий, принадлежащих данной частице, составляет ее спектр. Если спектр обусловлен энергетическим переходом из состояния с меньшей энергией в состояние с большей энергией, то спектр называется спектром поглощения (абсорбционным), а при переходе из состояния с большей энергией в состояние с меньшей энергией – спектром испускания. Спектры, испускаемые термически возбужденными частицами, называются эмиссионными. Спектры испускания нетермически возбужденных частиц (квантами света, электронами) называются спектрами люминесценции. Последние разделяют на спектры флуоресценции и фосфоресценции. Быстрое спонтанное испускание фотонов возбужденной частицей (без изменения спина электронов) называется флуоресценцией, а замедленное (с изменением спина электронов) – фосфоресценцией.
Спектр поглощения получают, помещая исследуемое вещество в поле электромагнитного излучения (например, на пути светового потока), а для получения спектра испускания предварительно переводят атомы в возбужденное состояние, которое достигается за счет подведения какого-либо вида энергии (тепловой, химической, электрического разряда, электромагнитной и др.). После возбуждения атомы возвращаются (через 10-9 – 10-7 с) в основное состояние, испуская фотоны либо теплоту (в последнем случае переход будет безизлучательным).
Частота испускаемого или поглощаемого излучения определяется разностью энергии между электронными состояниями DЕ: n = DЕ / h.
Наиболее вероятны переходы электрона с первого возбужденного уровня (Е1) на основной (Ео). Соответствующие им спектральные линии называют резонансными. Электрон может перейти и в более высокое энергетическое состояние (Е2, Е3 и т.д.).
Методы анализа, основанные на изменениях энергетического состояния атомов веществ, входят в группу атомно-спектроскопических методов, различающихся по способу получения и регистрации сигнала.
· Оптические методы основаны на использовании энергетических переходов внешних (валентных) электронов. Общим для них является необходимость предварительной атомизации (разложение на атомы) вещества. К ним относят атомно-эмиссионную, атомно-флуоресцентную и атомно-абсорбционную спектроскопию.
· Рентгеновские методы основаны на энергетических переходах внутренних электронов атомов. В зависимости от способа получения и регистрации сигнала различают рентгеноэмиссионную, рентгеноабсорбционную и рентгенофлуоресцентную спектроскопию. Разновидности этих методов – оже-спектроскопию, рентгеновский электронно-зондовый анализ, электронную спектроскопию – используют в основном для исследования строения веществ. Рентгеновские методы не требуют атомизации вещества и позволяют исследовать твёрдые пробы без предварительной подготовки.
· Ядерные методы основаны на возбуждении ядер атомов.
Молекулярно-спектроскопические методы анализа основаны на регистрации энергетических состояний молекулы, которые сложнее, чем у атома. Кроме движения электронов в атомах происходят и колебательные движения самих атомов, и вращение молекулы как целого. Поэтому в любом стационарном состоянии энергия молекулы складывается из электронной, колебательной и вращательной энергий: Е = Еэл + Екол + Евр
Наибольший вклад в полную энергию вносит энергия электронов, наименьший – энергия вращения молекулы: Еэл > Екол > Евр.
Переходы между энергетическими уровнями с изменением главного квантового числа являются электронными, между колебательными уровнями – колебательными (рис. 2), между вращательными – вращательными (соответственно спектры называются электронными, колебательными и вращательными).

поглощение излучение
Рис. 2. Энергетические переходы в молекуле.
Вращение молекул проявляется у веществ лишь в газообразном состоянии, в конденсированном состояниях (жидком и твердом) вращение затрудненно.
По происхождению аналитического сигнала выделяют несколько молекулярно-спектроскопических методов: абсорбционную молекулярную, инфракрасную, люминесцентную, магнитную резонансную, фотоакустическую, рентгеновскую спектроскопию.
Спектральные сигналы наблюдают и регистрируют (записывают, фотографируют, измеряют и т.д.) с помощью спектральных приборов.
Для аналитических целей наибольшее значение имеют спектроскопические методы, использующие оптический диапазон шкалы электромагнитных волн. Регистрация сигналов в ультрафиолетовой (λ = 100 – 400 нм) и видимой (λ = 400-750 нм) части спектра осуществляется фотометрическими методами, которые в зависимости от типа используемого прибора делятся на спектрофотометрический и фотоэлектроколори-метрический.
