Лаборатортшя работа n 6
Определение А в горных пород
Теория.При прохождении электрического тока через породу происходит ее поляризация, которая обусловливает проявление вызванной электрохимической активности.
Большинство пород (кроме рудных) являются диэлектриками. Под действием электрического тока заряженные молекулы, атомы и ионы, следуя за изменением электрического поля, смещаются относительно друг друга, создавая отдельные поля. Совокупность этих полей и образует новое поле поляризации, вызывающее появление вызванного потенциала. Существует несколько гипотез появления вызванных потенциалов
В породах с электронной проводимостью (угли, колчеданы, железные руды) появление вызванных потенциалов связано с электродными процессами, протекающими в местах входа и выхода электрического тока в зернах с электронной проводимостью. В этих местах происходят окислительно-восстановительные реакции, которые протекают за счет катионов Na+1, Са+2, Mg+2 и др., присутствующих в растворах, заполняющих поры пород. Катионы, продвигаясь за счет поляризующего тока, встречают минералы с электронной проводимостью, разряжаются на них и превращаются в атомы, вступающие В реакции с водой
Na+1 +е- + Н2О= NaOH + Н;
Са+2+2е- +2Н2О = Са(ОН)2 +2Н;
Mg+2 +2е-+2Н2О = Mg(OH)2 +2Н.
Таким образом, на поверхности, на которой протекает реакция, образуются свободный водород и щелочи. Частично поляризованный водород на поверхности твердой фазы образует газовый водородный электрод [4].
На противоположном конце зерна с электронной проводимостью (в месте выхода тока) проте-кает обратный процесс. Твердая фаза отбирает электрон у аниона хлора, который превращается в атом и насыщает поверхность рудного включения. Некоторые атомы хлора ионизируются за счет электронов, возникающих при ионизации водорода, и входят в электролит, где их меньше, сообщая этому участку отрицательный заряд. Остальные атомы хлора вступают в реакцию с водой
4Сl – 4е- +2Н2О → 4HCl + 2О.
В результате образуется свободный кислород. Если он не окисляет твердую фазу, он выде-ляется. Таким образом, в породе образуются элементы с газовыми электродами - водородным и хлорным, которые, разряжаясь, дают токи поляризации.
У сульфидов, углей кислород, образовавшийся на выходе тока, окисляет твердую фазу ; ион, образовавшийся после диссоциации, адсорбируется твердой фазой, которая и приобретает заряд адсорбированного иона.
Образовавшийся атомарный кислород может окислять углистые вещества (для углей), создавая на поверхности карбоксильные группы
 Раствор в этом случае оказывается заряженным положительно. В породах с ионной проводимостью и большим электрическим сопротивлением (карбонаты, обломочные породы) возникновение вызванной поляризации связано с деформацией диффузной части двойного электрического слоя под действием приложенного напряжения. Катионы смещаются к отрицательному полюсу. В противоположной стороне от него появляется избыток отрицательно заряженных ионов. При снятии приложенного напряжения деформированные силы стремятся восстановиться, что приводит к появлению токов поляризации.
Раствор в этом случае оказывается заряженным положительно. В породах с ионной проводимостью и большим электрическим сопротивлением (карбонаты, обломочные породы) возникновение вызванной поляризации связано с деформацией диффузной части двойного электрического слоя под действием приложенного напряжения. Катионы смещаются к отрицательному полюсу. В противоположной стороне от него появляется избыток отрицательно заряженных ионов. При снятии приложенного напряжения деформированные силы стремятся восстановиться, что приводит к появлению токов поляризации.
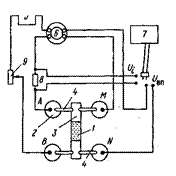
Рис.37. Электрическая блок-схема измерения электро-
химиической активности.
Существует гипотеза, по которой в песчано-глинистых породах различные участки имеют различную концентрацию катионов. В местах контакта отдельных зерен с глинистыми частицами появляется повышенная концентрация катионов вследствие наличия диффузных слоев глинистых частиц и минимальная в порах. При пропускании электрического тока в суженных каналах через единицу площади будет, перенесено гораздо больше катионов, чем через расширенную часть поры. В результате этого в породе создается неравномерное распределение зарядов в ее различных частях. При выключении тока поляризации происходит движение ионов, направленное на восстановление первоначального равновесного положения, вызывая токи поляризации.
| 1) электрохимическая ячейка с помещенным в нее образцом (рис. 38); 2) каломельные электроды; 3) агар-агаровые сифоны; 4) растворы NaCl и KCl соответствующих концентраций, приготовленные из NaCl, КCl х.ч. или ч.д.а.; 5) источник постоянного тока напряжением 100-120 В; 6) автоматический переключатель 6; 7) цифровой вольтметр; 8) эталонное сопротивление Rэт= 100 Ом; 9) свинцовые электроды; 10) электродные стаканчики. |
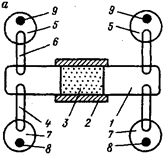
Рис. 38. Электрохимическая ячейка для определения электрохимической активности А вызв
Различные горные породы имеют различную величину вызванной поляризации. Для всех пород характерно увеличение потенциала вызванной поляризации с увеличением поляризующего тока. Породы с электронной проводимостью имеют довольно сложную зависимость. В большинстве пород величина вызванной поляризации вначале растет быстро, а затем медленно достигает некоторого насыщения с увеличением плотности поляризующего тока j . Породы с ионной проводимостью имеют чаще всего линейный характер зависимости
ΔUв.п. = f ( j ). ( ).
Способность горной породы поляризоваться под действием электрического тока, пропуска-емоrо через породу, оценивается ее поляризуемостью и связана с ее вызванной электрохимической активностью Ав.
Аппаратура, оборудоваuие, материалы. Измерения вызванных потенциалов можно выполнить при помощи специальной аппаратуры. описание которой в данной работе не приводится, либо с использованием автоматического переключателя, который подключает к исследуемому образцу попеременно цепь измерения (рис. 37).
Для этого используется: электрохимическая ячейка (см. рис. 38). Она представляет собой две L-образные стеклянные
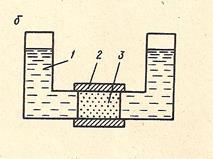 |
ческий образец породы 3 при помощи эластичного резинового шланга 2, концы которого натягиваются на стеклянные L-образные трубки. В трубки заливается раствор NaCl (обычно концентрации 2-3 г/л), имеющий удельное сопротивление ρр = 2-3 Ом м. Свободные концы трубок соединяются агар-агаровыми сифонами 4-6 с электродными стаканчиками 5, 7. В два электродных стаканчика 5, соединенных с разными концами трубок, устанавливаются свинцовые токовые (питающие) электроды 9 и в два других 7 каломельные электроды 8. Переключатель включается в схему таким образом, что при работе его контакты замыкают поочередно токовую цепь поляризации и измерительную цепь, в которую включен вольтметр.
Тем самым обеспечивается питание образца короткими импульсами тока, а в промежутках - измерение вызванной разности потенциалов.
Источник постоянного тока обеспечивает питание токовой цепи стабилизированным напряжением, регулировка которого предусмотрена в источнике питания .
Эталонное сопротивление R ЭТ = 100 Ом, включенное последовательно в токовую цепь, позволяет устанавливать ток питания I = ΔUэт / Rэт и измерять ΔUпр = IRобр.
NB. 1) Для лабораторной работы используются неполяризующиеся электроды: каломельные, хлорсеребряные или хлорталлиевые. Потенциалы этих электродов устойчивы и точно известны относительно стандартного водородного или другого электрода сравнения. В используемых стандартных электродах потенциал обычно не превышает 0,1 – 0,3 мВ и остаётся постоянным.
2) Агар-агаровые сифоны представляют собой U-образные стеклянные трубки, заполненные электропроводящим агаровым студнем , приготовленным из агар-агара, растворённого в дистиллированной воде с добавленным КСl или пластовой воде. Они служат для обеспечения электрической связи рабочего раствора с измерительной схемой.
