K×с2(СО)×с(О2)
Учитывая, что концентрация и парциальное давление связаны прямо пропорциональной зависимостью
рi = сi×RT,
получим, что υ= k×р2(СО)×р(О2).
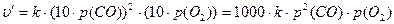 |
После увеличения давления в системе в 10 раз парциальное давление каждого из реагентов возрастет тоже в 10 раз, т. е.
Отсюда υ¢/υ = 1000. Следовательно, скорость реакции увеличится в 1000 раз.
3. Задача. В реакции А ® В + С с общим порядком, равным единице, константа скорости k1 = 5×10-5 с-1. Определите концентрацию веществ А и В и скорость реакции через 1 час и через 5 часов, если начальная концентрация А составляла 0,2 моль/л.
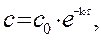 |
Решение. Для реакции 1-го порядка справедливо уравнение
где с – текущая концентрация вещества в момент времени τ, с0 – начальная концентрация, k – константа скорости, τ – время.
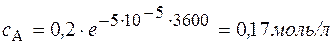
Через 1 час
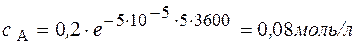
Через 5 часов
Концентрация вещества В находится по стехиометрическому соотношению веществ А и В. Из уравнения реакции следует, что концентрация вещества В возрастает на ту же величину, на какую убывает концентрация А, т. к. из 1 моль А получается 1 моль В.
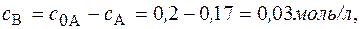
Поэтому через 1 час
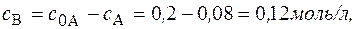
Через 5 часов 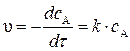
Рассчитаем скорость реакции по уравнению:
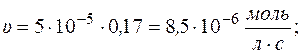
Через 1 час
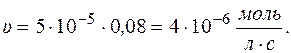
Через 5 часов
4. Задача. Для реакции первого порядка А ® 2В определите время, за которое
прореагирует 90 % вещества А. Константа скорости реакции k1 = 10-4 с-1.
Решение. После превращения 90 % вещества А его концентрация составит 10% от начальной концентрации, т. е. 0,1 с0.
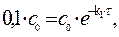
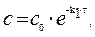
Из уравнения получим, что
Следовательно, τ = ln 10/k1 = 23026 с = 6,4 ч.
5. Задача. При изучении кинетики термического разложения ацетона, являющегося реакцией первого порядка, в соответствии с уравнением:
СН3СОСН3(г) ® С2Н4(г) + СО(г) + Н2(г)
получены следующие экспериментальные данные при Т = 802 К: давление
в реакторе изменилось от начального р0 = 312 мм. рт. ст. до 408 мм. рт. ст.
за 390 с. Рассчитайте константу скорости реакции.
Решение. Все вещества в системе находятся в газообразном состоянии, и, учитывая условия проведения опыта, предполагаем, что они подчиняются законам идеальных газов. Следовательно, концентрация и парциальное давление газа связаны зависимостью
pi=ci×R×T
или
Отсюда, для реакции I-го порядка
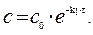
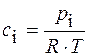 |
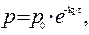
и
Если р0 – это начальное давление ацетона в реакционном сосуде, то для решения задачи необходимо определить парциальное давление этого вещества к моменту времени, когда общее давление
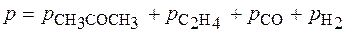 составило 408 мм. рт. ст.
составило 408 мм. рт. ст.
Из стехиометрии реакции видно, что 1 моль ацетона, распадаясь, образует 3 моль газа. Из закона Авогадро следует, что при уменьшении парциального давления ацетона на Dр сумма парциальных давлений образовавшихся газов составит 3Dр. Таким образом, можно записать
P = p0 – Dp + 3×Dp
или
408 = 312 + 2×Dp, Dp = 48 мм рт.ст.
Следовательно, парциальное давление ацетона через 390 с после начала опыта составило 312 – 48 = 264 (мм. рт. ст.).
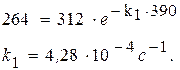 |
После подстановки в уравнение получим:
6. Задача. При температуре 100°С константа скорости реакции второго порядка
2НI(г) ® Н2(г) + I2(г)
равна 8,83×10-16 л/(моль×с). Определите время полупревращения йодистого
водорода, если начальная концентрация его равна 1 моль/л.
Решение. Воспользуемся уравнением для реакции второго порядка:
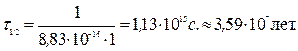
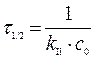 |
Далее рассчитаем
7. В реакции второго порядка А + В ® D за 1 час концентрации веществ А и В уменьшились по сравнению с начальной с0 А = с0 В = 0,2 моль/л на 30 %. Определите константу скорости и скорость реакции в начальный момент времени и через час после начала реакции.
Решение. Концентрации веществ А и В за 1 час уменьшились на
0,3×с0 = 0,06 моль/л. Отсюда, через час концентрации составят
сА = сВ = 0,2 – 0,06 = 0,14 (моль/л).
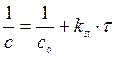
Для реакции II-го порядка
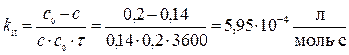
Отсюда
8. Рассчитайте изменение константы скорости реакции, имеющей энергию
активации 191 кДж/моль, при увеличении температуры от 330 до 400 К.
Решение. Зависимость константы скорости реакции от температуры определяется уравнением Аррениуса
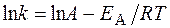
или
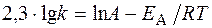
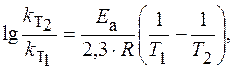 |
Логарифм отношения констант скоростей реакции при температурах Т2 и Т1 соответственно равен
где R = 8,31 Дж/(моль×К) – универсальняая газовая постоянная.
