Анализ неизвестного неорганического вещества. Предварительные испытания. Переведение анализируемого вещества в раствор. Проведение анализа
Анализ неизвестного вещества можно условно разделить на 3 этапа:
I. Предварительные испытания
II. Переведение анализируемого вещества в растворимое состояние
III. Обнаружение катионов и анионов
Твердый образец измельчают и делят на 4 части: первая часть используется для предварительных испытаний, вторая – для обнаружения катионов, третья – для обнаружения анионов, четвертая – для повторного исследования.
Предварительные испытания
-органолептическое исследование (определение цвета, запаха, формы кристаллов, реакция среды с помощью индикатора, летучесть)
- окрашивание пламени горелки (на очищенную, промытую и тщательно высушенную нихромовую или платиновую проволоку помещают пробу и вносят в пламя, разные металлы окрашивают пламя в различные цвета: натрий-желтый, калий-фиолетовый, медь-зеленый и т.д.)
- действие кислот (при действии на пробу разб.минеральных кислот могут выделяться различные газы СО2,SO2,H2S,NO2)
- растворение пробы в воде и определение рН раствора (если проба полностью растворяется в воде, то после определения рН можно сделать выводы о составе образца: в кислом растворе не могут содержаться соли неустойчивых кислот, в щелочном – соли слабых оснований, кроме того по окраске полученного раствора можно судить о наличии в образце окрашенных ионов(например, кобальта, никеля, меди, хрома))
Переведение анализируемого вещества в раствор
-если вещество не растворяется в воде, изучаютего растворимость в кислотах, вначале проводят растворение в разбавленной соляной кислоте, в случае необходимости продолжают испытания в концентрированной. В разбавленной растворяются большинство оксидов, гидроксиды, карбонаты, некоторые сульфиды, в азотной кислоте растворяются все оксиды, гидроксиды и сульфиды, а также соли слабых кислот.
- малорастворимые в воде, кислотах и щелочах соединения переводят в растворимое состояние частными методами. К таким соединениям относят галогениды серебра, сульфаты щелочно-земельных металлов и свинца, силикаты, некоторые оксиды металлов. Галогениды серебра различают по растворимости а аммиаке, соли малорастворимых сульфатов растворяют в 30% р.ацетата аммония, силикаты сплавляют с карбонатами калия и натрия, оксиды металлов переводят в растворимое состояние сплавлением с гидросульфатом или пиросульфатом калия.
Проведение анализа
I. Обнаружение катионов
- сначала проводят обнаружение ионов аммония, калия, натрия, лития, железа, ртути, мышьяка.
- затем определяют наличие II и III групп при помощи групповых реагентов соляной и серной кислот.
- далее на исследуемый раствор действуют изб.гидрокида нария в присутствии перекиси, в осадок выпадают катионы V и VI, а в оставшемся растворе определяют катионы IV группы.
- осадок V и VI групп обрабатывают раствором аммиака, в полученном растворе открывают катионы VI группы, а осадок исследуют на наличие катионов V группы.
II. Обнаружение анионов
-мешающие катионы удаляются из раствора (кипячение раствора с избытком карбоната натрия → «содовая вытяжка»). Если исследуемый раствор содержит только катионы первой группы , то осаждение катионов не проводится.
-прежде, чем приступить к обнаружению анионов, необходимо нейтрализовать раствор до рН = 7 уксусной или соляной кислотой, при нейтрализации в осадок выпадает гидроксид алюминия и гидрокарбонат меди.
- этот осадок отделяют, а в фильтрате обнаруживают анионы I-III групп.
17.Химическое равновесие. Константа химического равновесия. Виды констант химического равновесия, используемые в аналитической химии (термодинамические, реальные и условные концентрационные, общие, ступенчатые)
Химическое равновесие — состояние химической системы, в котором обратимо протекает одна или несколько химических реакций, причём скорости в каждой паре прямая-обратная реакция равны между собой. Для системы, находящейся в химическом равновесии, концентрации реагентов, температура и другие параметры системы не изменяются со временем. А2 + В2 ⇄ 2AB
Константа равновесия — величина, определяющая для данной химической реакции соотношение между термодинамическими активностями исходных веществ и продуктов в состоянии химического равновесия. Зная константу равновесия реакции, можно рассчитать равновесный состав реагирующей смеси, предельный выход продуктов, определить направление протекания реакции. Константа химического равновесия не зависит от механизма реакции. Для записи выражения химического равновесия, необходимо знать лишь стехиометрическое уравнение реакции.
В аналитической химии используют:
1. Термодинамические константы химического равновесия (К0 ) – выражают через активность частиц, принимающих участие в равновесии, которое характеризует соответствующая константа. Для равновесия aA+ bB=cC+dD, термодинамическая константа равновесия описывается:
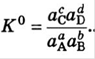
2. Реальные концентрационные константы хим. равновесия (К)- предполагают использование равновесных концентраций частиц. Для ее расчета используют уравнение 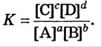 Термодинамич. константа зависит от природы веществ, участвующих в равновесии, температуры, растворителя, давления. Концентрационные константы зависят не только от природы веществ, температуры, давлении и т.д., но и от ионной силы. Связь между концентрационной и термодинамической константами описывается уравнением:
Термодинамич. константа зависит от природы веществ, участвующих в равновесии, температуры, растворителя, давления. Концентрационные константы зависят не только от природы веществ, температуры, давлении и т.д., но и от ионной силы. Связь между концентрационной и термодинамической константами описывается уравнением: 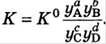
3. Общие константы – сумма равновесных концентраций всех форм существования данного вещества. Отношение равновесной концентрации определенной формы вещества к общей концентрации этого вещества называется молярной долей данной формы вещества 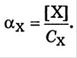
4. Условные концентрационные константы хим. равновесия. Отличаются от реальных тем, что в описывающие их выражения входят общие концентрации веществ, участвующих в равновесии: 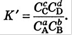
5. Равновесные константы – концентрация определенной формы вещества, участвующего в равновесии. Она представляет собой сумму равновесных концентраций всех форм существования данного вещества
6. Ступенчатые константы – константы, характеризующие каждую ступень.
Произведение ступенчатых констант называется общей константой равновесия.
Существуют также смешанные констант равновесия, в которых, например, содержание одного иона выражено через активность, а остальных – через концентрации. В аналит. химии спользуются несколько типов химического равновесия, отличающихся друг от друга тем, обмен какими частицами происходит в процессе реакции.
Константы равновесий могут быть очень малые или очень большие величины. Часто вместо значений констант равновесия более удобным оказывается использовать десятичные логарифмы. Отрицательный десятичный логарифм константы равновесия называется показателем данной константы и обозначается как рК.
18.Отклонения от идеальности в растворах сильных электролитов. Активность и коэффициент активности. Ионная сила раствора. Зависимость активности сильного электролита от ионной силы раствора.
Активность(а) - это такая концентрация вещества в растворе, при использовании которой свойства данного раствора могут быть описаны теми же уравнениями, что и свойства идеального раствора. Активность называют действующей концентрацией. Измеряется моль/л.
Активность может быть меньше номинальной концентрации, а может быть и больше. Активность чистого растворителя, нерастворенного вещества или жидкости, не смешивающейся с данным раствором, принимается равной 1.
Отношение активности вещества в данном растворе к его концентрации называется коэффициентом активности. В зависимости от способа описания количественного состава раствора различают молярный(У), моляльный и рациональный (f) коэффициенты активности. Молярный коэффициент активности – отношение эффективной молярной концентрации веществ к его действительной молярной концентрации, моляльный – отношение эффективной моляльности к действительной, рациональный – отношение эффективной молярной доли к действительной молярной доле вещества в растворе. 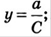
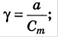
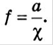
Заметное отклонение от идеальности имеется в растворах сильных электролитов. Это отражается на их температурах кипения и замерзания, давления пара над раствором, на величины различных констант равновесий в таких растворах.
Для характеристики активности электролитов используются среднеионные коэффициенты активности, характеризующие поведение электролита в целом, и индивидуальные коэффициенты активности ионов: они характеризуют активность отдельных ионов, входящих в состав электролита.
Активность вещества, находящегося в растворе электролита, зависит от концентрации всех ионов, присутствующих в нем и их заряда. Величина, которая учитывает влияние концентрации и заряда всех ионов, находящихся в растворе, на активность растворенного вещества, называется ионной силой: 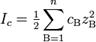 .
.
Ионная сила имеет размерность концентрации. При ее расчете учитывается концентрация и заряд всех ионов, образовавшихся при ионизации всех сильных электролитов, присутствующих в растворе. Неэлектролиты не оказывают влияния на величину ионной силы.
Универсального уравнения, с помощью которого можно было бы рассчитать коэффициент активности любого электролита при любой величине ионной силы, не существует. Для описания зависимости коэффициента активности от ионной силы в очень разбавленных растворов (до ионной силы меньше О, О1) используют предельный закон Дебая-Хюккеля: 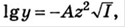
При расчетах коэффициентов активности при ионных силах порядка 0,01- 0,1 используют расширенное уравнение Дебая-Хюккеля: 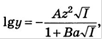
При высоких значениях ионной силы( до 1) используют уравнение Дэвиса 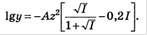 19.Важнейшие теории кислот и оснований: протолитическая теория Бренстеда-Лоури, теория Аррениуса, теория Льюиса. Количественное описание силы кислот и оснований (константа кислотности, константа основности, константа кислотности сопряженной кислоты, их показатели).
19.Важнейшие теории кислот и оснований: протолитическая теория Бренстеда-Лоури, теория Аррениуса, теория Льюиса. Количественное описание силы кислот и оснований (константа кислотности, константа основности, константа кислотности сопряженной кислоты, их показатели).
Теория Бренстеда-Лоури( протолитческая теория): кислоты- это вещества, способные отдавать протон(доноры протона), основания – это в-ва, способные присоединять протон( акцепторы протона). Кислоты и основания, согласно теории Бренстеда, существуют как сопряженные пары. Частица, содержащая на один протон больше, чем исходное основание, называется кислотой, сопряженный с данным основанием, а частица, содержащая на один протон меньше, чем исходная кислота, называется основанием, сопряженная с данной кислотой. Понятие «соль» в протолитической теории не используется. Протон, согласно этой теории, не существует в растворе в свободном виде, а связывается с молекулами растворителя.
Теория Аррениуса: кислоты – это электролиты, при диссоциации которых в водном растворе образуются катионы только одного вида – катионы водорода, а основания – электролиты, при диссоциации которых в водном растворе в качестве анионов образуются только гидроксид-ионы. Кислота и основание могут взаимодействовать друг с другом с образованием соли и воды (р-ция нейтрализации). Если хотя бы один из компонентов, вступающих в реакцию нейтрализации, не относится к сильным электролитам, то данная реакция является обратимой. Реакция, обратная реакции нейтрализации – р-ция гидролиза. Применение теории Аррениуса, было ограничено только водными растворами, и далеко не все соединения подходили под определения «кислота» и «основание».
Теория Льюиса (электронная теория кислот и оснований): основания – доноры пары электронов( кислоты, катионы металлов), кислоты – акцепторы пары электронов. Следствие Льюиса: любое органическое соединение можно представить как кислотно -основный комплекс.
Теории Бренстеда и Льюиса являются наиболее широко использующимися теориями кислот и оснований в современной химии.
Для количественной силы кислот, находящихся в растворе, используют константу, характериз. способность кислоты отдавать протон молекуле растворителя, выступающей в качестве основания. Такая константа называется константой кислотности (Ка).Константа кислотности характеризует равновесие и описывается выражениями 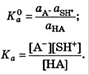
Активность растворителя не входит в выражение для этой константы, т.к.считается равной 1. Термодинамическая константа кислотности для водных растворов описывается уравнением 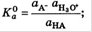 , а концентрационная
, а концентрационная . Отрицательный десятичный логарифм константы кислотности называется показателем константы кислотности (рКа): рКа=-lgкА. Чем больше Ка и меньше рКа, тем сильнее кислота.
. Отрицательный десятичный логарифм константы кислотности называется показателем константы кислотности (рКа): рКа=-lgкА. Чем больше Ка и меньше рКа, тем сильнее кислота.
Силу оснований можно описывать двояко: либо с помощью константы основности(Кb), характеризующей равновесие  , либо с помощью константы кислотности сопряженной кислоты (Квн+), характеризующей равновесие
, либо с помощью константы кислотности сопряженной кислоты (Квн+), характеризующей равновесие  .Константа основности применяется редко. Константа основности не несет никакой новой информации, так как ее легко рассчитать, зная величину константы кислотности сопряженной кислоты.
.Константа основности применяется редко. Константа основности не несет никакой новой информации, так как ее легко рассчитать, зная величину константы кислотности сопряженной кислоты.
Отрицательный десятичный логарифм константы кислотности сопряженной кислоты называется показателем константы кислотности сопряженной кислоты(рКвн+): рКвн+=-lgКвн+
Чем больше Квн+ и меньше рКвн+ , тем сильнее сопряженная с описываемым основанием кислота и тем слабее само основание.
20. Классификация растворителей по кислотно-основным свойствам и полярности. Автопротолиз растворителя. Константа автопротолиза. Нивелирующее и дифференцирующее действие растворителя. Сильные и слабые кислоты и основания. Водородный показатель.
Сила кислоты зависит от природы взаимодействующего с ней основания, а сила основания – от природы взаимодействующей с ним кислоты. В зависимости от наличия или отсутствия склонных к ионизации атомов водорода растворители можно условно разделить на протонные и апротонные. В составе молекул протонных растворителей имеется склонный к ионизации атом водорода (вода, спирты, карбоновые кислоты и т.д.). У апротонных растворителей подобных атомов водорода нет. В зависимотсти от диэлектрической проницаемости апротонные растворители можно разделить на 2 группы: неполярные апротонных растворители(гексан, бензол ит.д.) и полярные растворители(ацетон).
В зависимости от кислотно-основных свойств можно выделить 4 группы растворителей: кислотные(протогенные), основные( протофильные), амфотерные и инертные. К группе кислотных растворителей относят в-ва, у которых преобладает кислотные свойства (уксусная кислота). Кислотные растворители повышают – по сравнению с водой – силу растворенных в них оснований и понижают силу кислот. У основных растворителей сильнее выражены основные свойства ( аммиак) Основные растворители повышают силу растворенных в них кислот и понижают силу оснований. У амфотерных растворителей кислотные и основные свойства выражены приблизительно одинаково (спирты, вода). Инертные растворители практически не способны принимать участие в кислотно-основном взаимодействии(бензол).
Автопротолиз – процесс кислотно-основного взаимодействия между двумя молекулами вещества, при котором одна молекула ведет себя как кислота, а вторая – как основание.Автопротолизу подвержено большинство растворителей.
В реакции кислотно-основного взаимодействия между 2 молекулами растворителя: SH+SH=SH2++ S- . Частица SH2+ называется ионом лиония, а частица S- - ионом лиата. Равновесие можно охарактеризовать с помощью константы равновесия(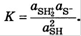 ). Для чистого растворителя аSH=1, поэтому можно заменить выражением
). Для чистого растворителя аSH=1, поэтому можно заменить выражением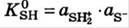 . Полученная константа – константа автопротолиза (КSH )
. Полученная константа – константа автопротолиза (КSH )
Отрицательный десятичный лагорифм константы автопротолиза называется показателем константы автопротолиза (рКSH).
Константа автопротолиза является мерой протяженности шкалы кислотности.
Кислоты, более сильные, чем ион лиония, или основания, более сильные, чем ион лиата, уравниваются по силе. Такое явление называется нивелирующим действием растворителя. Способность растворителя оказывать нивелирующее или дифференцирующее действие зависит от его кислотно-основных свойств и склонности к автопротолизу. Растворитель с сильными основными свойствами нивелирует силу кислот и дифференцирует силу оснований. Сильно кислотный растворитель, напротив, дифференцирует силу кислот и нивелирует силу оснований. Чем меньше величина константы автопротолиза растворителя, тем выше вероятность того, что он будет оказывать дифференцирующее действие на силу кислот и оснований.
Водородный показатель(рН) – отрицательный десятичный логарифм активности ионов водорода в растворе: рН=-lg(H+). Шеала кислотности зависит от величины рКSH растворителя. Для характеристики кислотности и щелочности водных растворов используется интервал рН от 0 до 14.
