Общие методы получения дубильных веществ
Из растительного сырья
Поскольку дубильные вещества представляют собой смесь очень лабильных полифенолов, имеющих нередко сложную структуру, выделение и анализ индивидуальных компонентов представляет собой трудоемкий процесс.
Для выделения из растений суммарных фракций дубильных веществ используют экстракцию растительного материала органическими растворителями: петролейным эфиром, бензолом или смесью бензол - хлороформ (1 : 1) для удаления основной массы хлорофилла, терпеноидов и липидов, затем экстрагируют этиловым эфиром, который извлекает некоторые фенольные соединения, в том числе оксикоричные кислоты и катехины; после чего проводят экстракцию этилацетатом, в результате которой в экстракт переходят лейкоантоцианидины, димерные проантоцианидины, эфиры оксикоричных кислот и др. В завершение растительный материал экстрагируют метиловым или этиловым спиртом, при этом в раствор переходит сумма дубильных и сопутствующих веществ.
Для получения суммы дубильных веществ используются и другие способы: растительное сырье вначале экстрагируют горячей водой, а затем охлажденный водный экстракт обрабаты-вают последовательно вышеперечисленными растворителями.
Широкое распространение получил способ выделения дубильных веществ, осаждением из водных или водноспиртовых растворов солями свинца. Полученные осадки затем обрабатывают разбавленной серной кислотой.
Суммарные извлечения дубильных веществ разделяют на индивидуальные компоненты с помощью хроматографических методов: адсорбционно-распределительной хроматографии на колонках целлюлозы, силикагеля или полиамида, ионообменной хроматографией на колонках катионита (Дауэкс-50), гель-хроматографией на колонках сефадекса G-50 или G100.
ИРИДОИДЫ
По химической природе эта группа соединений относится к гликозидам, специфичным для отдельных видов «горьких» растений.
Обычно иридоиды легко растворимы в воде и низших спиртах (метиловом и этиловом) и плохо растворимы в органических растворителях (бензоле, хлороформе).
Иридоиды легко гидролизуются на агликон и сахар. Агликоны легко полимеризуются в темно-коричневые пигменты. Этот химический процесс происходит при участии ферментов и наиболее часто возможен при неправильной сушке сырья и его хранении при повышенной влажности - сырье буреет ("явление черной пигментации").
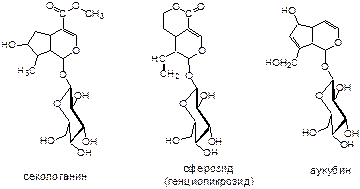 |
Наибольней биоактивностью отличаются иридоиды: секологанин, генциопикрозид и аукубин:
Выделение:
Навеску измельченного растительного сырья экстрагируют 50-80% спиртом этиловым или метиловым при нагревании в колбе с обратным холодильником в течение 30-40 мин, фильтруют.
Для проведения качественного анализа используют 1-3 мл извлечений.
Качественный анализ [11,12]:
q Добавляют 1-2 мл реактива Трима-Хилла (смесь 5 мл кислоты хлороводородной концентрированной, 10 мл 0.2% раствора меди сульфата и 100 мл кислоты уксусной ледяной), нагревают до кипения, появляется интенсивное синее окрашивание.
q Добавляют 1-2 мл кислоты серной концентрированной, нагревают до температуры 1000С, прибавляют 3-5 капель 0.5% водного раствора аммония ванадата в кислоте серной, появляется синее окрашивание, которое вскоре обесцвечивается.
q Добавляют 2-3 мл реактива Шталя (5 мл кислоты хлороводородной концентрированной, 50 мл спирта этилового 95%, 1 г п-диметил-аминобензальдегида, добавляют до 100 мл спиртом этиловым), появляется сине-зеленое окрашивание
q ТСХ (силуфол), хлороформ-метанол 9:1 1100С, через 5- 8 минут, сине-зеленое окрашивание.
Методы хроматографии широко используются для исследования растительных иридоидов. Поиску оптимальных методик анализа иридоидов в тонком слое посвящено множество работ, предложено несколько десятков различных хроматографических систем. Группа болгарских ученых для разделения, сравнительной идентификации и препаративного выделения предлагает использовать системы: этилацетат – пропанол-2 – вода 6:3:1, хлороформ – метанол – вода – муравьиная кислота 75:24:1:0.2, хлороформ – метанол – вода 60:22:4 и 60:15:4 (нижний слой) [72]. Помимо указанных систем, наиболее часто используются: хлороформ – метанол – вода 80:20:2, 7:2:1 и 61:32:7, а также этилацетат – метанол (9:1) [73,74]. Помимо классических хроматографических методов для выделения и анализа иридоидов может быть использован метод ВЭЖХ.
Анализ предлагаемых методик позволяет сделать вывод, что наиболее удобными для анализа иридоидов являются октадецилпермафазные сорбенты: Whatman ODS-3, Lichrospher RP18, Zorbax SB-C18. Подвижными фазами, чаще всего, являются водно-метанольные смеси различного состава с добавлением минеральной или органической кислоты. Так, группой проф. М.И.Митовой для препаративного выделения иридоидов предложено использовать 5% водный метанол с добавлением 15мкл орто-фосфорной кислоты на 100 мл подвижной фазы, УФ детектор при 233 нм [72]. 30% водный метанол с добавлением 0.5% уксусной кислоты предложено использовать в качестве подвижной фазы корейскими учеными (Prof. W.C.Ye) [75]. Градиентным элюированием смесями А(0.15% уксусная кислота) и В(метанол), у увеличением содержания А в В от 25 до 90% за 40 мин предложено анализировать сумму иридоидов Wulfenia carinthiaca [76]. В обеих работах использовался УФ детектор (205 нм). Другим вариантом элюентной системы может служить ацетонитрил – вода (25:75), с использованием рефрактометрического детектора [73].
Количественное определение:
Около 2 г (точная навеска) измельченного сырья помещают в мерную колбу со шлифом вместимостью 100 мл, прибавляют 50 мл спирта этилового 50% и настаивают, периодически помешивая при комнатной температуре в течение 1 часа. Затем извлечение фильтруют через бумажный фильтр в мерную колбу вместимостью 50 мл, избегая попадания частиц сырья на фильтр, и доводят объем извлечения спиртом этиловым 50% до метки.
10 мл полученного раствора пропускают через стеклянную колонку диаметром 10 мм с 2 г алюминия оксида для хроматографии второй степени активности. В мерную колбу вместимостью 25 мл помещают 5 мл элюата, прибавляют 5 мл 10% раствора гидроксиламина основного и оставляют на 20 минут. Через 20 мин прибавляют 10 мл 1М кислоты хлороводородной, доводят объем раствора до метки 1% раствором железа окисного хлорида в 0.1М кислоте хлороводородной, перемешивают.
Измеряют оптическую плотность полученного раствора при длине волны 512 нм в кювете с толщиной слоя 10 мм. В качестве раствора сравнения используют смесь, приготовлен-ную в колбе вместимостью 25 мл: к 5 мл воды очищенной прибавляют 5 мл раствора кислоты хлороводородной, доводят объем раствора 1% раствором железа окисного хлорида в 0.1 М кислоте хлороводородной до метки и перемешивают.
Содержание иридоидов в процентах (X) в пересчете на абсолютно сухое сырье, вычисляют по формуле:
|
 D . 50 . 100 . 100
D . 50 . 100 . 100 Е . m . 10 . (100 - W)
где D - оптическая плотность испытуемого раствора при длине волны 512 нм;
Е - удельный показатель поглощения СО иридоида при длине волны 512 нм;
m – масса навески сырья, в граммах;
W – потеря в массе при высушивании сырья, в процентах.
Примечания. Растворы, используемые при проведе-нии анализа, должны быть свежеприготовленными.
Приготовление 1% раствора железа окисного хлорида в 0.1М кислоте хлороводородной. 1 г железа окисного хлорида растворяют в мерной колбе вместимостью 100 мл в 30 мл 0.1 М кислоты хлороводородной, доводят объем раствора этой кислотой до метки, перемешивают. Раствор устойчив в течение недели.
* Методика пригодна для анализа лекарственного растительного сырья и для анализа препаратов.
** Возможно использование любого доступного СО иридоида. Например, если СО пеонифлорин, Е = 16.2, если СО гарпагида ацетат Е = 56.
