Задачи и методы исследования термодинамических процессов
Задачами исследования термодинамических процессов в газах является выявление закономерностей изменения параметров при протекании процессов и установление закономерностей превращения энергии, т.е. определение значения теплоты 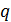 , работы l и изменения внутренней энергии Δu.
, работы l и изменения внутренней энергии Δu.
Методика исследования процессов в газах предусматривает решение следующих вопросов:
1. Установление уравнения процесса;
2. Определение графика процесса;
3. Нахождение связи между параметрами состояния газа, изменяющимися при протекании процесса;
4. Определение теплоемкости газа;
5. Определение количества теплоты q, подведенной к газу, совершенной
им работы l и изменения его внутренней энергии Δu.
Будем рассматривать только равновесные процессы в идеальных газах.
Изохорный процесс
Изохорным называется процесс, протекающий при постоянном объеме.
1. Уравнение процесса – 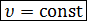 .
.
2. График процесса – вертикальная линия в р,υ -координатах (рис. 2.5).
3. Связь между параметрами состояния газа. Для этого запишем уравнение состояния для точек 2 и 1 и разделим их друг на друга
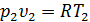 ,
, 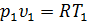 .
.
Так как в изохорном процессе 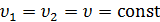 , то
, то
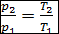 . (2.14)
. (2.14)
4. Теплоемкость газа в изохорном процессе обозначается символом 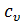 . Для идеального газа при умеренных температурах
. Для идеального газа при умеренных температурах
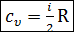
где 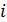 – число степеней свободы молекулы газа.
– число степеней свободы молекулы газа.
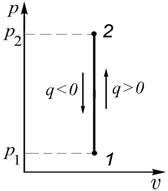 |
| Рис. 2.5. График изохорного процесса |
5. Определение количества теплоты q, подведенной к газу, совершенной им работы l и изменения его внутренней энергии Δu:
- так как  , то
, то 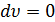 , значит, элементарная работа
, значит, элементарная работа 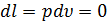 и работа расширения газа l = 0 ;
и работа расширения газа l = 0 ;
- согласно первому закону термодинамики 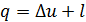 . Так как l = 0, то
. Так как l = 0, то
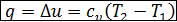 . (2.15).
. (2.15).
Если 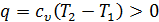 , то
, то 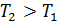 . Тогда из (2.14) следует, что
. Тогда из (2.14) следует, что 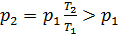 . Значит, при подводе теплоты к газу его давление возрастает и наоборот (рис. 2.5).
. Значит, при подводе теплоты к газу его давление возрастает и наоборот (рис. 2.5).
Таким образом, в изохорном процессе теплота, сообщаемая газу, идет только на увеличение его внутренней энергии, т.е. на увеличение его температуры.
Изобарный процесс
Изобарным называется процесс, протекающий при постоянном дав-
Лении.
1. Уравнение процесса – 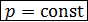 .
.
2. График процесса – горизонтальная линия в р,υ -координатах (рис. 2.6).
3. Связь между параметрами состояния газа. Для этого запишем уравнение состояния для точек 2 и 1 и разделим их друг на друга
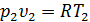 ,
, 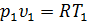 .
.
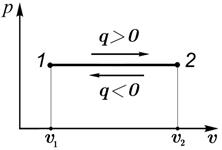 |
| Рис. 2.6. График изобарного процесса |
Так как в избарном процессе 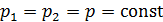 , то
, то
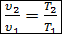 . (2.16)
. (2.16)
4. Теплоемкость газа в изобарном процессе обозначается символом ср. Для идеального газа при умеренных температурах
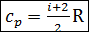 .
.
5. Определение количества теплоты q, подведенной к газу, совершенной им работы l и изменения его внутренней энергии Δu:
— работа расширения газа: так как  , то
, то
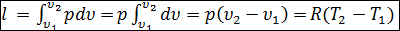 (2.17)
(2.17)
— количество тепла, подведенного к газу
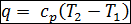 ; (2.18)
; (2.18)
— изменение внутренней энергии газа
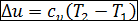 ; (2.19)
; (2.19)
Если 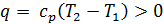 , то
, то 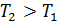 . Тогда из (2.16) следует, что
. Тогда из (2.16) следует, что 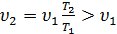 . Значит, при подводе к газу теплоты его удельный объем возрастает и наоборот (рис. 2.6).
. Значит, при подводе к газу теплоты его удельный объем возрастает и наоборот (рис. 2.6).
