Свободного пробега молекул воздуха
Лабораторная работа 1.
Определение коэффициента внутреннего трения и средней длины
свободного пробега молекул воздуха.
Цель работы: экспериментальное определение коэффициента внутреннего трения и средней длины свободного пробега молекул воздуха.
Теоретическое введение
Молекулы газа, находясь в тепловом движении, непрерывно сталкиваются друг с другом. Термин «столкновение» не следует понимать буквально и представлять себе этот процесс подобным соударению твердых шаров. Под столкновением молекул подразумевается процесс их взаимодействия, в результате которого изменяются направление движения и модуль скорости молекул.
 Взаимодействие между молекулами характеризуется их взаимной потенциальной энергией
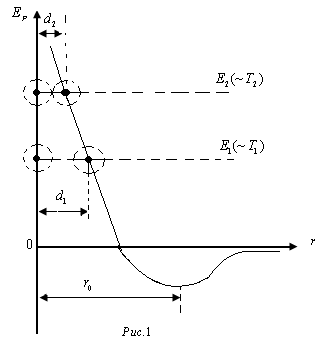
Взаимодействие между молекулами характеризуется их взаимной потенциальной энергией 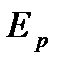 . На рис. 1 приведена кривая зависимости
. На рис. 1 приведена кривая зависимости 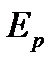 двух молекул от расстояния
двух молекул от расстояния 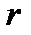 между центрами молекул. Центр первой молекулы помещается в начале координат (в точке 0), центр второй молекулы перемещается вдоль оси
между центрами молекул. Центр первой молекулы помещается в начале координат (в точке 0), центр второй молекулы перемещается вдоль оси 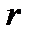 . В скобках проставлена температура
. В скобках проставлена температура 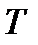 , соответствующая начальной скорости второй молекулы.
, соответствующая начальной скорости второй молекулы.
Из механики известно, что сила действует в направлении убывания потенциальной энергии т.е. 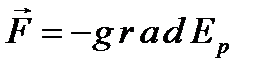 или
или 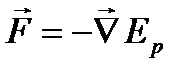 . Следовательно, на участке от
. Следовательно, на участке от 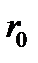 до бесконечности между молекулами действует сила притяжения, которая при
до бесконечности между молекулами действует сила притяжения, которая при 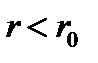 сменяется быстро возрастающей силой отталкивания.
сменяется быстро возрастающей силой отталкивания.
Пусть вторая молекула начинает движение в направлении к первой из бесконечности, имея запас кинетической энергии
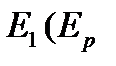 на бесконечности равна нулю
на бесконечности равна нулю 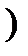 . По мере приближения к первой молекуле кинетическая энергия второй молекулы возрастает, (потенциальная энергия
. По мере приближения к первой молекуле кинетическая энергия второй молекулы возрастает, (потенциальная энергия 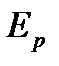 уменьшается), достигает максимума при
уменьшается), достигает максимума при 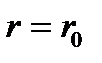 после чего начинает быстро убывать. Когда потенциальная энергия молекулы становится равной начальной энергии
после чего начинает быстро убывать. Когда потенциальная энергия молекулы становится равной начальной энергии 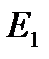 , молекула останавливается. Затем молекулы будут двигаться в обратном направлении.
, молекула останавливается. Затем молекулы будут двигаться в обратном направлении.
Минимальное расстояние 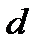 , на которое сближаются при столкновении центры молекул, называется эффективным диаметром молекулы
, на которое сближаются при столкновении центры молекул, называется эффективным диаметром молекулы 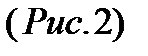 . На рисунке видно, что, чем больше начальная кинетическая энергия молекулы (т.е. чем выше температура), тем меньше
. На рисунке видно, что, чем больше начальная кинетическая энергия молекулы (т.е. чем выше температура), тем меньше 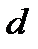 .
.
Величина
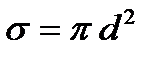 (1)
(1)
называется эффективным сечением молекулы
Силы притяжения на участке от 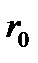 до бесконечности малы, а силы отталкивания при
до бесконечности малы, а силы отталкивания при 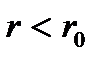 напротив, очень велики. Это дает основание рассматривать соударение молекул, как столкновение не взаимодействующих на расстоянии твердых упругих шаров диаметра
напротив, очень велики. Это дает основание рассматривать соударение молекул, как столкновение не взаимодействующих на расстоянии твердых упругих шаров диаметра 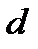 .
.
Воспользуемся этой моделью шаров для нахождения средней длины свободного пробега молекул, т.е. среднего расстояния 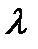 проходимого молекулой между двумя последовательными соударениями с другими молекулами.
проходимого молекулой между двумя последовательными соударениями с другими молекулами.
Сначала найдем число 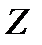 столкновений в единицу времени одной движущейся молекулы с остальными неподвижными
столкновений в единицу времени одной движущейся молекулы с остальными неподвижными 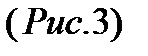 . В единицу времени молекула проходит путь, равный в среднем
. В единицу времени молекула проходит путь, равный в среднем 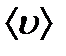 .
.
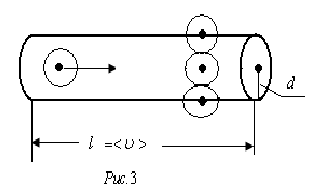
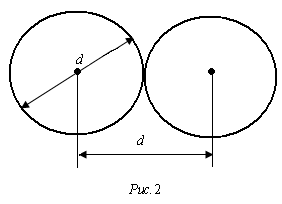
Движущаяся молекула столкнется со всеми молекулами, центры которых лежат внутри цилиндра, радиус сечения которого равен эффективному диаметру молекул 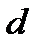
 . Число столкновенийz равно числу молекул n в этом цилиндре, т.е.
. Число столкновенийz равно числу молекул n в этом цилиндре, т.е.
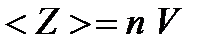
(2)
где n-число молекул в единице объема; 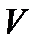 - объем цилиндра, равный
- объем цилиндра, равный
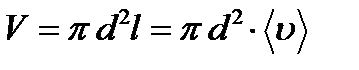 (3)
(3)
подставив (3) в (2) получим выражение:
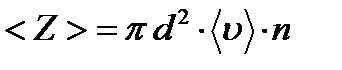 (4)
(4)
Теория вероятности позволяет подсчитать, что если учесть движение всех молекул, то число столкновений будет в 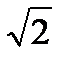 раза больше полученного нами в предположении, что движется лишь одна молекула. Итак:
раза больше полученного нами в предположении, что движется лишь одна молекула. Итак:
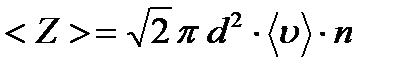 (5)
(5)
где 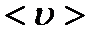 – среднеарифметическая скорость молекулы.
– среднеарифметическая скорость молекулы.
Среднюю длину свободного пробега молекул можно получить, если весь путь, пройденный молекулой за единицу времени, разделить на число соударений в единицу времени, т.е.
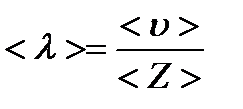 (6)
(6)
С учетом (5) получим
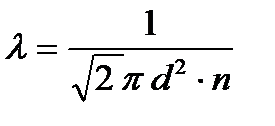 (7)
(7)
Основное уравнение молекулярно-кинетической теории может быть записано в форме:
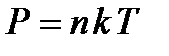 (8)
(8)
Если подставить значение n из формулы (8) в (7), получим
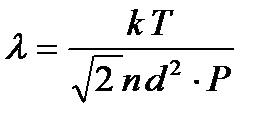 (9)
(9)
Здесь 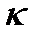 - постоянная Больцмана,
- постоянная Больцмана, 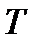 - термодинамическая температура,
- термодинамическая температура, 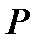 - давление газа.
- давление газа.
Из формулы (9) видно, что средняя длина свободного пробега 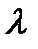 обратно пропорциональна давлению, т.е.
обратно пропорциональна давлению, т.е.
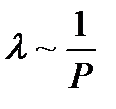 (10)
(10)
Эта зависимость используется при получении вакуума.
Средняя длина свободного пробега молекул 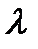 связана коэффициентами переносов. К явлениям переноса относятся теплопроводность, диффузия и внутреннее трение (вязкость). Уравнение этих явлений переносов сходны между собой. Мы рассмотрим явления внутреннего трения (вязкости) которое, как показал опыт, подчиняется закону И. Ньютона.
связана коэффициентами переносов. К явлениям переноса относятся теплопроводность, диффузия и внутреннее трение (вязкость). Уравнение этих явлений переносов сходны между собой. Мы рассмотрим явления внутреннего трения (вязкости) которое, как показал опыт, подчиняется закону И. Ньютона.
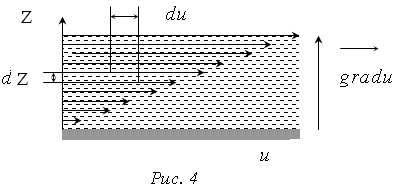
Рассмотрим ламинарный поток вязкой жидкости по горизонтальному руслу. Ламинарные течения жидкости возникают, когда жидкость течет медленно. В этом случае течение имеет слоистый, тихий характер.
Слой, “прилипший” ко дну неподвижен. По мере удаления от дна скорость жидкости увеличивается. Максимальная скорость жидкости будет у слоя, который граничит с воздухом. Со стороны слоя который движется быстрее, на слой который движется медленнее, действует ускоряющая его сила. Эти силы, направленные по касательной поверхности слоя, называют силами внутреннего трения. Они тем больше, чем больше площадь соприкасающихся слоев и зависит от изменения скорости течения жидкости (газа) при переходе от слоев к слою (уравнение Ньютона):
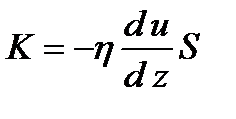 (11)
(11)
Так как разделение на слои условно, то принято выражать силу в зависимости от изменения скорости, приходящегося на единицу длины в направлении, перпендикулярном скорости, то есть от величины 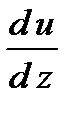 , называемой градиентом скорости (gradu ).
, называемой градиентом скорости (gradu ).
Здесь h - коэффициент пропорциональности, называемый коэффициентом внутреннего трения, или динамической вязкостью который численно равен потоку импульса через поверхности 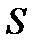 , при градиенте скорости, равном единице. Вязкость зависит от химического состава, примесей и температуры. В системе
, при градиенте скорости, равном единице. Вязкость зависит от химического состава, примесей и температуры. В системе 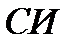 вязкость измеряется
вязкость измеряется 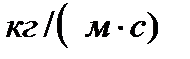 или, что то же самое, в паскаль – секундах
или, что то же самое, в паскаль – секундах 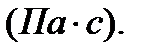
Если вывести опытный закон Ньютона (11) из молекулярно- кинетической теории, то получается выражение для коэффициента вязкости, т.е.
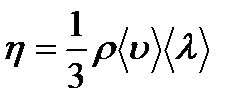 (12)
(12)
где 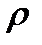 – плотность газа,
– плотность газа, 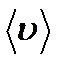 - среднеарифметическая скорость молекул газа,
- среднеарифметическая скорость молекул газа, 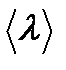 - средняя длина свободного пробега молекул.
- средняя длина свободного пробега молекул.
Если определить коэффициент внутреннего трения (вязкость) экспериментально, то по формуле (12)можно вычислить 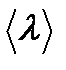 .
.
