Пример 2. Вычислите теплоту образования оксида железа, исходя из уравнения
Вычислите теплоту образования оксида железа, исходя из уравнения
8Al + 3Fe3O4 = 4Al2O3 + 9Fe, DH0 = -3326 кДж.
Энтальпия образования оксида алюминия равна 1669 кДж/моль.
Решение.
В основе термохимических расчетов лежит закон Гесса: «Тепловой эффект реакции зависит только от конечного и начального состояния веществ и не зависит от промежуточных стадий процесса». Часто в термохимических расчетах используется следствие из закона Гесса: «Тепловой эффект реакции равен сумме энтальпий образования продуктов реакции за вычетом суммы энтальпий образования исходных веществ с учетом коэффициентов реакции»:
DH0х.р. = 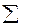 n × DH0продуктов -
n × DH0продуктов - 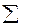 n × DH0исходных веществ.
n × DH0исходных веществ.
Распишем тепловой эффект реакции восстановления железа, используя следствие из закона Гесса:
DH0х.р. = (9 · DH0(Fe) + 4 · DH0(Al2O3) - (8 · DH0(Al) + 3 · DH0(Fe3O4).
Поскольку энтальпии образования простых веществ равны нулю, а теп-ловой эффект реакции и энтальпия образования оксида алюминия даны в условии задачи, то можно рассчитать энтальпию образования оксида железа.
-3326 = [9 · 0 + 4 · (-1669)] - (2 · 0 + 3DH0(Fe3O4),
DH0(Fe3O4) = 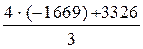 = -1116,7 кДж/моль.
= -1116,7 кДж/моль.
