Основные классы неорганических соединений. Цель работы: ознакомиться со свойствами неорганических соединений и способами их получения.
Лабораторная работа № 1
Цель работы: ознакомиться со свойствами неорганических соединений и способами их получения.
Общие сведения:
Оксиды–это сложные вещества, в состав которых атомы кислорода какого-либо другого элемента (ЭхОу). Степень окисления кислорода в оксидах равна -2. Например, Fe2O3- оксид железа (III), CuO-оксид меди (II) или оксид меди (+2).
Основные оксиды - это оксиды металлов в степенях окисления .К ним относятся:
· оксиды металлов главной подгруппы первой группы (щелочные металлы) Li — Fr
· оксиды металлов главной подгруппы второй группы (Mg и щелочноземельные металлы) Mg — Ra
· оксиды переходных металлов в низших степенях окисления
Кислотные оксиды – это оксиды всех неметаллов (исключение – F, благородные газы), а также металлов в высокой степени окисления (+5, +6, +7) (Cl2O3, Mn2O7, P2O5 и др.).
Амфотерные оксиды — солеобразующие оксиды, проявляющие в зависимости от условий либо основные, либо кислотные свойства (то есть проявляющие амфотерность). Образуются переходными металлами. Металлы в амфотерных оксидах обычно проявляют степень окисления от III до IV, за исключением ZnO, MnO2, SnO, PbO.
Кислоты — химические соединения, способные отдавать катион водорода (кислоты Брёнстеда) либо соединения, способные принимать электронную пару с образованием ковалентной связи (кислоты Льюиса).
В быту и технике под кислотами обычно подразумеваются кислоты Брёнстеда, образующие в водных растворах избыток ионов гидроксония H3O+. Присутствие этих ионов обуславливает кислый вкус растворов кислот, способность менять окраску индикаторов и, в высоких концентрациях, раздражающее действие кислот. Подвижные атомы водорода кислот способны замещаться на атомы металлов с образованием солей, содержащих катионы металлов и анионы кислотного остатка.
Основания (гидроксиды) — неорганические соединения, содержащие в составе гидроксильную группу -OH. Известны гидроксиды почти всех химических элементов; некоторые из них встречаются в природе в виде минералов. Гидроксиды щелочных и щёлочноземельных металлов, а также аммония являются щелочами. Например, Сu(ОН)2-гидроксид меди (II), Fe(ОН)3-гидроксид железа (III).
Основные гидроксиды — это сложные вещества, которые состоят из атомов металла или иона аммония и гидроксогруппы (OH) и в водном растворе диссоциируют с образованием анионов ОН− и катионов. Название основания обычно состоит из двух слов: слова «гидроксид» и названия металла в родительном падеже (или слова «аммония»). Хорошо растворимые в воде основания называются щелочами.
Кислотные гидроксиды (кислородсодержащие кислоты)— всегда содержат атомы водорода, способные замещаться на атомы металла. Исключение составляет борная кислота В(ОН)3, которая акцептирует ионы ОН-в результате чего в водномрастворе создается избыток гидроксоний-катионов.
Амфотерные гидроксиды —неорганические соединения, гидроксиды амфотерных элементов, в зависимости от условий проявляющие свойства кислотных или основных гидроксидов. Все амфотерные гидроксиды являются твёрдыми веществами. Нерастворимы в воде, в основном являются слабыми электролитами.
Соли — сложные вещества, которые в водных растворах диссоциируют на катионы металлов и анионы кислотных остатков. ИЮПАК определяет соли как химические соединения, состоящие из катионов и анионов. Есть ещё одно определение: солями называют вещества, которые могут быть получены при взаимодействии кислот иоснований с выделением воды.
Средние (нормальные) соли — продукты замещения всех катионов водорода в молекулах кислоты на катионы металла (Na2CO3, K3PO4, Ca3(PO4)2).
Кислые соли — продукты частичного замещения катионов водорода в кислотах на катионы металла (NaHCO3, CaHPO4). Они образуются при нейтрализации основания избытком кислоты (то есть в условиях недостатка основания или избытка кислоты).
Основные соли — продукты неполного замещения гидроксогрупп основания (OH-) кислотными остатками ((CuOH)2CO3). Они образуются в условиях избытка основания или недостатка кислоты.
Двойные соли – атомы водорода двух- или многоосновной кислоты замещены не одним металлом, а двумя различными: NaKCO3, KAl(SO4)2
Смешанныесоли, в составе которых присутствует два различных аниона (Ca(OCl)Cl).
Комплексные– вещества, содержащие сложный комплексный ион, способный к самостоятельному существованию.
Пример: (NH4)2[PtCl4(OH)2] — дигидроксотетрахлороплатинат(IV) аммония
Ход работы:
1. Несколько кристалликов дихромата аммония нагрейте на спиртовке. Напишите уравнение реакции.
2. К 2-3 мл соляной кислоты прибавьте кусочек мела. Обратите внимание на выделение пузырьков газа. Напишите уравнение реакции.
3. В металлической ложечке в пламени спиртовки сожгите немного красного фосфора. Что при этом получится? Напишите уравнение реакции.
4. К 2-3 мл нитрата ртути (II) прибавьте гидроксида натрия. Что выпало в осадок?
Напишите уравнение реакции
5. К 2-3 мл сульфата меди (II) прибавьте щелочи. Обратите внимание на Cu(OH)2. Напишите уравнение реакции. Разделите осадок на 2 части. Одну нагрейте на спиртовке. Что произошло с цветом осадка? Напишите уравнение реакции. Другую часть осадка сохраните для опыта 7.
6. К 2-3 мл сульфата хрома (III) прилейте до осадка гидроксида натрия. Выпавший осадок разделите пополам. К одной части осадка прилейте еще гидроксида натрия, а к другой – раствора соляной кислоты. Что наблюдаете? Напишите уравнения происходящих реакций.
II часть. Получение солей
7. К полученному в опыте 5 осадку гидроксида меди (II) прилейте соляной кислоты. Напишите уравнение реакции. Назовите образующуюся соль.
8. К раствору нитрата свинца (II) прилейте раствор иодида калия. Обратите внимание на осадок выпавшей соли. Напишите уравнение реакции. Назовите соли.
9. В раствор разбавленной азотной кислоты опустите кусочек меди. Нагрейте содержимое. Напишите уравнение реакции, если в результате образуется соль, газ (одноокись азота) и вода.
10. К раствору сульфата меди (II) прилейте раствора гидроксида аммония до появления светло – зеленного осадка основной соли. Напишите уравнение реакции. Назовите соли.
11. Через раствор хлорида кальция пропустите диоксид углерода (из аппарата Киппа). Выпадет осадок карбоната кальция. Продолжайте пропускать диоксид. Осадок исчезнет, т.е. образуется растворимая соль гидрокарбоната кальция.
Получение оксидов и гидроксидов:
Опыт №1:
(NH4)2CrO7 t→ N2↑ + Cr2O3 + H2O
Оранжевый Зеленый
Cr2O3 – оксид хрома (III), амфотерный оксид.
Структурная формула: O = Cr – O – Cr = O
Опыт №2:
CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
CO2- оксид углерода(IV), кислотный оксид.
Структурная формула: O = С = O
Опыт №3:
4P + 5O2 → 2P2O5
2P2O5 – оксид P(V).
| O |
| O |
| r |
| P |
| P |
| O |
| O |
O O
Опыт №4:
CuSO4 + 2NaOH → Cu(OH)2  + Na2SO4
+ Na2SO4
Cu(OH)2 – осадок голубого цвета,
Cu(OH)2 – гидроксид Сu(II).
Структурная формула: OH – Cu – OH
Опыт №5
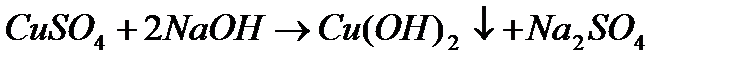
В ходе реакции наблюдаем появление осадка ярко-голубого цвета.
Разделяем вещество на 2 части. Первую часть нагреваем на спиртовке. Наблюдаем изменение цвета осадка с ярко-голубого на черный.
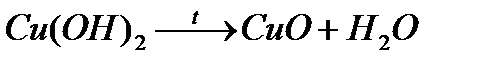
К полученному осадку добавляем соляную кислоту.
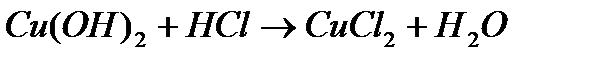
Наблюдаем растворение осадка.
Опыт№6
6NaOH + Cr2(SO4)3 → 3Na2SO4 + 2Cr(OH)3↓
Сr(ОН) 3 + 3NaОН → Na3[Сr(ОН) 6]
Cr(OH)3 + 3HCl → CrCl3 + 3H2O
Опыт№7.
Cu(OH)2 + 2HCl → CuCl2 + 2H2O
Хлорид меди(II) - средняя соль
Cl-Cu-Cl
Опыт№8
Pb(NO3)3 + 2KI→ 2 KNO3 + PbI2↓
Нитрат калия Иодид Ртути (II). – средняя соль.
I-Pb-I
Опыт№9
Cu+4HNO3→Cu(NO3)2+2NO2+2H2O
нитрат меди (II)- средняя соль
Структурная формула:
O= N - O - Cu - O - N =O
Опыт№10
Cu2SO4 + 2 NH4OH → 2 (CuOH)2SO4 + (NH4)2SO4
сульфат меди (II) сульфат аммония
Опыт№11
CaCl2+H2O+CO2 →CaCO3 + 3HCl
CaCO3+H2O+CO2→ Ca(HCO3)2
Гидрокарбонат кальция (II) кислая соль
Структурная формула:
O=C-O-Ca-O-C=O
Контрольные вопросы:
1. Написать формулы и определить степень окисленности каждого элемента в соединениях: сульфат калия, гидрофосфат железа, нитрат кальция, оксид марганца (VI), сульфат гидроксокобальта.
Ответ:
Cульфат калия: K2SO4 – K+1 S+6 O-2
Гидрофосфат железа: FeHPO4 – Fe+2 H+1 P+5 O-2
Нитрат кальция: Ca(NO3)2 – Ca+2 N+5 O-2
Оксид марганца (VI): MnO3 - Mn+6 O-2
Cульфат гидроксокобальта: [Co+3(O-2H+1)](S+6 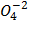 )2
)2
2. Дать определение понятиям: оксид, гидроксид, соль. Привести примеры.
Оксиды –это сложные вещества, в состав которых атомы кислорода какого-либо другого элемента (ЭхОу). Степень окисления кислорода в оксидах равна -2.
Пример: Fe2O3- оксид железа (III), CuO-оксид меди (II) или оксид меди (+2).
Гидроксиды–сложные вещества, в состав которых входят атомы металлов (катионов) и одна или несколько гидроксильных групп-Ме(ОН)n.
Пример: Ca(ОН)2 ,NaOH
Соли – это продукты полного или частичного замещения атомов водорода в кислоте на атомы металла или гидроксогрупп в основании на кислотные остатки. В случае полного замещения образуются средние (нормальные соли). В случае частичного замещения получаются кислые и основные соли.
Пример: NaCl, Na2SO4, СаSO4
3. Дописать уравнения реакций (получить среднюю, кислую, основную соли):
KOH+H2CO3= H2O + K2CO3
Zn(OH)2+2HCl= ZnCl2 + 2H2O
Ответ: KOH+H2CO3= K2CO3+H2O
Zn(OH)2+HCl= Zn(OH)Cl + H2O
ZnOHCL +HCL= ZnCL2 +H2O
4. Доказать амфотерный характер гидроксида, рассматривая его взаимодействие с кислотой и щелочью.
Sn(OH)2+2HCl→SnCl2+H2O – хлорид олова (II)
Sn(OH)2+2NaCl→Na2[Sn(OH)4] – гексагидрокостаннат (IV) натрия
Так как Sn(OH)2 прореагировал с кислотой и со щёлочью, то сделаю вывод о том, что он амфотерный.
Вывод: На лабораторной работе я ознакомился со свойствами неорганических соединений и способами их получения.
