Критические параметры природных газов и их компонентов
(РИС 31-39)
Критическим называется такое состояние вещества, при котором исчезает граница между его газовой и жидкой фазами и свойства этих фаз становятся равными. Для природного газа, являющегося смесью углеводородных и неуглеводородных компонентов, критические параметры (давление, температура, плотность, объем и т.д.) определяются как псевдокритические по составу газа.
Наиболее простым способом определения псевдокритических давления и температуры при известной плотности газа и неизвестном составе является графический способ. На рисунке 2.1 показаны зависимости псевдокритических давления Рп.кр и температуры Тп.кр от относительной по воздуху плотности газа. При наличии в газе азота, сероводорода и углекислого газа на псевдокритические параметры, определяемые из рисунка 2.1, вводятся поправки с соответствующим знаком, величины которых в зависимости от содержания этих компонентов показаны на рисунке 2.2. (Руководство по исслед. СКВ. Алиева стр.36)
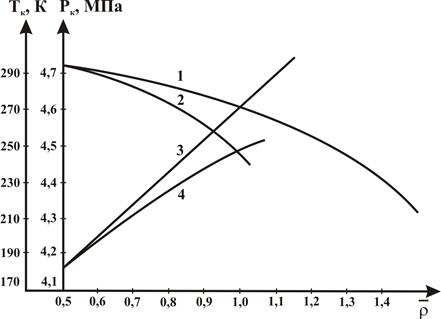
Рисунок 2.1 – Зависимости псевдокритичских давления и температуры для газа (кривые 1 и 4) и газоконденсатной смеси (кривые 2 и 3)
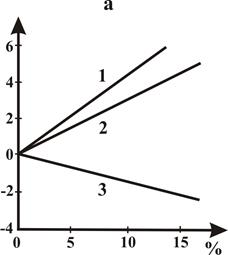
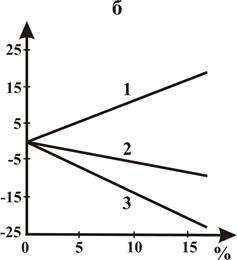
Рисунок 2.2 – Поправки к псевдокритическим давлениям – (а) и температурам – (б) газов, содержащих примеси H2S (1), CO2 (2), N2 (3).
При известном составе газа, если содержание метана составляет ≥95% псевдокритические параметры Рп.кр и Тп.кр определяются по формулам:
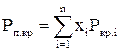 ;
; 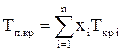 (2.3)
(2.3)
где xi – доля i-го компонента в газе; Ркр.i, Ткр.i – критические давление и температура i-го компонента в смеси, значения которых приведены в таблице 2.2.
Для более точного определения псевдокритических параметров газовых смесей Рп.кр и Тп.кр газоконденсатных месторождений рекомендуется использовать формулы:
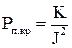 ;
; 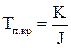 (2.4)
(2.4)
где 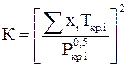 ;
; 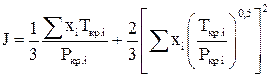 (2.5)
(2.5)
Если смесь газа включает в себя полярные и неполярные компоненты, то при превышении содержания полярных компонентов 5% мольных псевдокритические параметры определяются согласно методике, изложенной в работе [18].
Все углеводородные компоненты газа, азот и углекислый газ относятся к неполярным соединениям. К полярным соединениям относятся пары воды, сероводород и вводимые в поток газа метанол, соляная кислота и др.
Фактор ацентричности молекул реальных газов (РИС стр.44)
Молекулы реальных газов имеют конечные размеры и форму и оказывают значительное взаимное влияние. Поэтому для характеристики реальных газов необходимо учесть параметры, связанные молекулярным взаимодействием.
Молекулы простых газов имеют сферическую форму, для них схемы притяжения, которые действуют по линии, соединяющей их центры, пропорциональны расстоянию в шестой степени. Для газов с несферической формой молекул схемы притяжения или отталкивания состоят не только из сил между центрами молекул, но и из дополнительных нецентричных сил. Для учета дополнительных нецентричных сил между молекулами газа несферической формы введен дополнительный параметр, названный ацентрическим фактором.
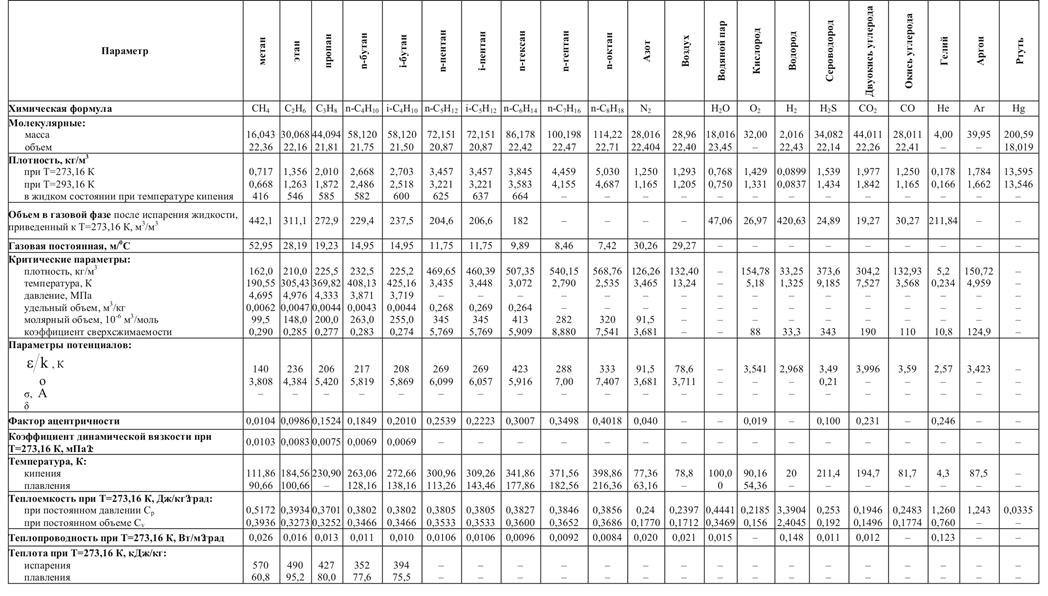
Таблица 2.2 – Физико-химические свойства компонентов природного газа при Р=0,1013 МПа.
Он является одним из параметров, оценивающих отклонения газов со сложной формой молекул от газов со сферической формой молекул. Для отдельных компонентов газов значения ацентрического фактора приведены в таблице 2.2.
Приближенно ацентрический фактор компонентов может быть определен формулой:
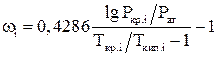
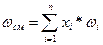 (2.6)
(2.6)
где Ткип.i – температура кипения i-го компонента, значение которой определяется из таблицы 2.2.
Если содержание высококипящих углеводородов С5+ в газе не превышает 1% мольных, то критические параметры этой группы могут быть заменены критическими параметрами нормального гептана. При содержании С5+ превышающем 1%, желательно эту группу углеводородов заменить фракцией товарного конденсата и рассматривать их как компоненты смеси.
Если в составе газа содержится до 50% кислых компонентов СО2 и H2S и при этом концентрация каждого из них не превышает 25%, то для определения псевдокритических параметров можно использовать приближенные формулы:
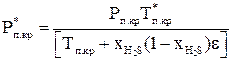 ;
; 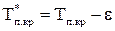 (2.7)
(2.7)
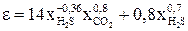 (2.8)
(2.8)
где 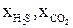 – мольные доли сероводорода и углекислого газа в составе газа; Рп.кр, Тп.кр – псевдокритические давление и температура, определяемые с использованием формулы (2.3).
– мольные доли сероводорода и углекислого газа в составе газа; Рп.кр, Тп.кр – псевдокритические давление и температура, определяемые с использованием формулы (2.3).
Приведенные параметры природных газов (РИС 39-40)
Приведенными параметрами называются отношения любых значений давления, температуры, объема и плотности к их критическим значениям и определяются формулами:
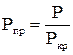 ;
; 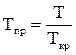 ;
; 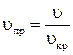 ;
; 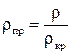 (2.9)
(2.9)
Эти параметры позволяют использовать принципы соответственных состояний для определения физических и теплофизических свойств газов. Наибольшее распространение получила двух- и трехпараметрическая форма принципа соответственных состояний. При двухпараметрической форме, т.е. без фактора ацентричности молекул, равенство физических свойств сравниваемых веществ достигается при равенстве двух приведенных параметров Рпр и Тпр. При трехпараметрической форме равенства теплофизических свойств, кроме двух приведенных параметров Рпр и Тпр, учитывается и ацентрический фактор ω.
Плотность газа (РИС стр 40-43)
Плотность - это отношение массы газа к единице его объема. Единица измерения плотности - кг/м3. Плотность газа при стандартных условиях, т.е. при Р=0,1013МПа и Тст=293 К, может быть определена по формуле:
ρст=М/υст=М/24,04 (2.10)
где М - молекулярная масса газа. Для более точного определения плотности отдельных компонентов и смеси газов следует использовать равенства:
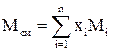 ;
; 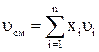 ;
; 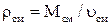 (2.11)
(2.11)
где xi - мольная доля i-го компонента; Мi - молекулярная масса i-го компонента; υi - объем одного моля i-го компонента.
Значения Мi и υi, приведены в таблице 2.2. Как видно из этой таблицы объем одного моля различных компонентов, входящих в состав природных газов, меняется от 20,87·10-3 м3/моль для пентана до 22,71·10-3 м3/моль для октана.
Плотность газов зависит от их состава, давления и температуры. Плотность газа при заданных давлении и температуре определяется по известной плотности при нормальных или стандартных условиях по формуле:
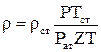 (в рабочих условиях) (2.12)
(в рабочих условиях) (2.12)
где ρст - плотность газа при стандартных условиях, т.е. при Р=0,1013 МПа и Тст=293 К, значение которой для отдельных компонентов берется из таблицы 2.2, а при известном составе газа ρст определяется по формуле:
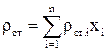 ;
; 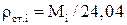 (2.13)
(2.13)
где Tст - стандартная температура, К; Рат - атмосферное давление, МПа; Z - коэффициент сверхсжимаемости газа при заданных Р и Т.
Пример: 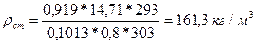 где:
где: 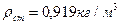 Р = 14,71 МПа, Тст = 293К, Рат = 0,1013 МПа, Z = 0,8
Р = 14,71 МПа, Тст = 293К, Рат = 0,1013 МПа, Z = 0,8
При наличии влаги - водяных паров в газе, его плотность определяется по формуле:
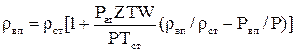 (2.14)
(2.14)
где W - влагосодержание газа при условиях Р и Т, определяется согласно методам, изложенным в пункте 2.2.7; рвп - плотность насыщенного водяного пара; Рвп - давление насыщенного водяного пара.
Значения ρвп и Рвп приведены в таблице 2.3 и показаны на рисунке 2.3. При использовании формулы (2.14) значение Z должно быть определено без учета наличия паров воды в газе.
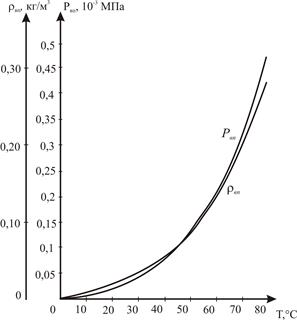
Рисунок 2.3 - Зависимости плотности ρвп и давления Рвп насыщенного водяного пара от температуры.
Таблица 2.3 - Зависимости плотности и давления насыщенного пара воды от температуры.
| Т, К | Рвп, МПа | ρвп, кг/м3 | Т, К | Рвп, МПа | ρвп, кг/м3 | Т, К | ρвп, МПа | ρвп, кг/м3 |
| 0,000611 | 0,00485 | 0,003564 | 0,02576 | 0,015002 | 0,0998 | |||
| 0,000656 | 0,00519 | 0,003778 | 0,02722 | 0,015740 | 0,1044 | |||
| 0,000706 | 0,00556 | 0,004004 | 0,02875 | 0,016509 | 0,1092 | |||
| 0,000757 | 0,00594 | 0,004241 | 0,03036 | 0,017311 | 0,1142 | |||
| 0,000804 | 0,00636 | 0,004491 | 0,03220 | 0,018146 | 0,1193 | |||
| 0,000882 | 0,00679 | 0,004753 | 0,03381 | 0,019015 | 0,1257 | |||
| 0,000934 | 0,00726 | 0,005029 | 0,03565 | 0,019917 | 0,1307 | |||
| 0,001001 | 0,00775 | 0,005318 | 0,03758 | 0,020859 | 0,1360 | |||
| 0,001072 | 0,00826 | 0,005622 | 0,03960 | 0,021839 | 0,1420 | |||
| 0,001147 | 0,00882 | 0,005940 | 0,04172 | 0,022849 | 0,1482 | |||
| 0,001227 | 0,00940 | 0,006274 | 0,04393 | 0,023909 | 0,1546 | |||
| 0,001312 | 0,01001 | 0,006624 | 0,04623 | 0,025007 | 0,1630 | |||
| 0,001401 | 0,01066 | 0,006991 | 0,04564 | 0,026144 | 0,1682 | |||
| 0,001496 | 0,01134 | 0,007375 | 0,05115 | 0,027243 | 0,1753 | |||
| 0,001597 | 0,01206 | 0,007777 | 0,05376 | 0,028557 | 0,1827 | |||
| 0,001704 | 0,01282 | 0,008198 | 0,05659 | 0,029832 | 0,1903 | |||
| 0,001817 | 0,01363 | 0,008639 | 0,05935 | 0,031156 | 0,1982 | |||
| 0,001936 | 0,01447 | 0,004099 | 0,06234 | 0,032529 | 0,2064 | |||
| 0,002062 | 0,01536 | 0,009582 | 0,06545 | 0,033960 | 0,2148 | |||
| 0,002196 | 0,01630 | 0,010085 | 0,06868 | 0,035431 | 0,2236 | |||
| 0,002337 | 0,01729 | 0,010612 | 0,07205 | 0,036961 | 0,2326 | |||
| 0,002485 | 0,01833 | 0,011169 | 0,07557 | 0,038550 | 0,2420 | |||
| 0,002642 | 0,01942 | 0,011735 | 0,07923 | 0,040187 | 0,2516 | |||
| 0,002507 | 0,02057 | 0,012335 | 0,08302 | 0,041894 | 0,2605 | |||
| 0,002982 | 0,02177 | 0,012960 | 0,08696 | 0,043649 | 0,2718 | |||
| 0,003166 | 0,02304 | 0,013612 | 0,09107 | 0,045473 | 0,2824 | |||
| 0,003360 | 0,02437 | 0,014293 | 0,09535 | 0,047356 | 0,2923 |
Величины поправок на плотность сухих газов при различных температурах приведены в таблице 2.4. Эти поправки на влажность добавляются или вычитаются из плотности сухого газа в зависимости от знака поправок, указанного в таблице 2.4.
Таблица 2.4 - Поправки к плотности сухого газа на его влажность.
| Плотность сухого газа, кг/м3 | Поправки (в%) при температуре | |||||||||
| 323 К | ||||||||||
| 0,4 0,5 0,6 0,7 0,8 0,9 1,0 | +1,2 +0,7 +0,4 +0,1 -0,2 -0,3 | +1,5 +0,9 +0,5 +0,1 -0,1 -0,3 -0,4 | +2,0 +1,2 +0,6 +0,2 -0,1 -0,4 -0,6 | +2,7 +1,5 +0,7 +0,2 -0,2 -0,6 -0,8 | +3,4 +1,9 +0,9 +0,2 -0,4 -0,8 -1,1 | +5,5 +2,4+1,0 +0,4 -0,6 -1,2 -1,6 | +6,4 +2,9 +1,2 -0,9 -1,6 -2,1 | +7,0 +3,5 +1,4 -0,1 -1,3 -2,2 -2,9 | +8,5 +4,3 +1,6 -0,3 -1,7 -3,0 -3,9 | |
При неизвестном компонентном составе плотность газоконденсатной смеси определяется по формуле
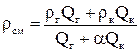 (2.15)
(2.15)
где ρг, ρк – плотности отсепарированного газа и конденсата; Qг, Qк – дебиты газа и конденсата; α – кажущийся объемный коэффициент конденсата при условиях определения плотностей ρсм, ρг и ρк. Значение α при стандартной температуре определяется по формуле:
α=24,04∙ρк/Мк (2.16)
где Мк – молекулярная масса конденсата, кг/моль.
В практике расчета часто используется относительная плотность газа по воздуху 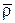 , равная отношению плотности газа при Р=0,1013 МПа и Т=293 К к плотности воздуха ρвоз при тех же условиях:
, равная отношению плотности газа при Р=0,1013 МПа и Т=293 К к плотности воздуха ρвоз при тех же условиях:
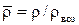 (2.17)
(2.17)
При Р=0,1013 МПа и Т=273 К плотность воздуха равна ρвоз=1,293 кг/м3, а при Т=293 К – ρвоз=1,205 кг/м3. Учитывая идентичность объемов газа и воздуха при стандартных условиях, относительную плотность можно определить по формуле: 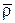 =М/28,96 (2.18)
=М/28,96 (2.18)
Коэффициенты сверхсжимаемости газов (РИС стр-44-56)
Коэффициент сверхсжимаемости газов – это отношение объема υ при заданных значениях Р и Т к объему этого газа, определенному при идентичных Р и Т по законам идеального газа υид. Коэффициент сверхсжимаемости характеризует отклонение объема реального газа от объема “идеального”. Формула, связывающая основные параметры газа – объем, давление и температуру, называется уравнением состояния газа. Уравнение состояния идеального газа получено из условия отсутствия межмолекулярных взаимодействий и без учета объема самих молекул и имеет вид
υид=nRT/P (2.19)
где n – число молей газа; R – универсальная газовая постоянная; Т и Р – температура и давление газа.
Уравнение состояния реального газа может быть представлено в виде:
υ=nZRT/P (2.20)
Универсальная газовая постоянная R выражает работу одного моля газа при повышении его температуры на один градус и в системе СИ имеет размерность Дж/кмоль·град.
Коэффициент сверхсжимаемости газа Z зависит от состава газа, давления и температуры. Значение коэффициента может быть определено графическим и аналитическим способами. Способ определения следует выбирать, исходя из требуемой точности его значения. Наиболее простым способом определения Z является графический. Для определения Z природных газов, содержащих не более 2% (мольных) высококипящих углеводородов С5+, 2% ароматических углеводородов и около 5% полярных и кислых компонентов, можно использовать графическую зависимость Z от приведенного давления Рпр и приведенной температуры Тпр, показанных на рисунках 2.4 и 2.5. На рисунках 2.6÷2.8 приведены зависимости Z от Р и Т для N2, CO2 и H2S.
При более высоком содержании в газе высококипящих углеводородов С5+ и полярных компонентов коэффициент сверхсжимаемости Z следует определять с учетом ацентричного фактора по формуле:
Z=Z(0)+ωсмZ(1) (2.21)
где Z(0), Z(1) – коэффициенты, определяемые из графиков зависимостей Z(0) и Z(1) от приведенных параметров Рпр и Тпр, показанных на рисунках 2.9 и 2.10; ωсм – фактор ацентричности, определяемый по известному составу газа по формуле:
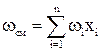 (2.22)
(2.22)
где ωi – фактор ацентричности i-го компонента, определяемый из таблицы 2.2 или по формуле (2.6).
Псевдокритические параметры, необходимые для определения Рпр и Тпр, с помощью которых из графиков находят Z(0) и Z(1), должны быть определены в зависимости от состава газа. Если в газе количество высококипящих углеводородов и полярных веществ более 5%, то псевдокритические параметры должны быть определены согласно [18]:
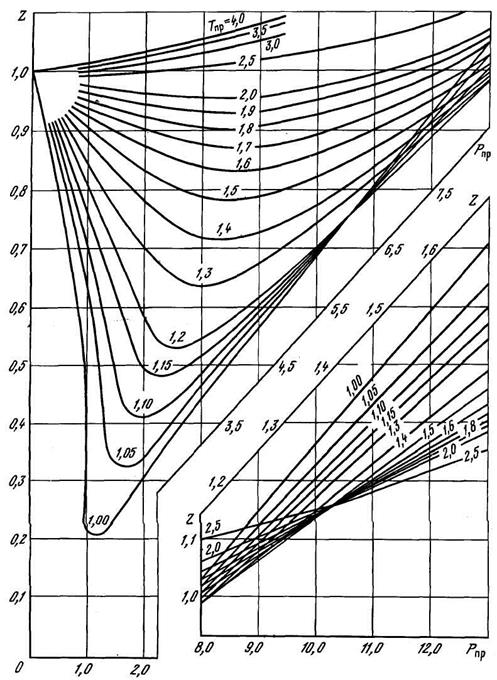
Рисунок 2.4 – Зависимость коэффициента сверхсжимаемости Z метана от приведенных давления и температуры.
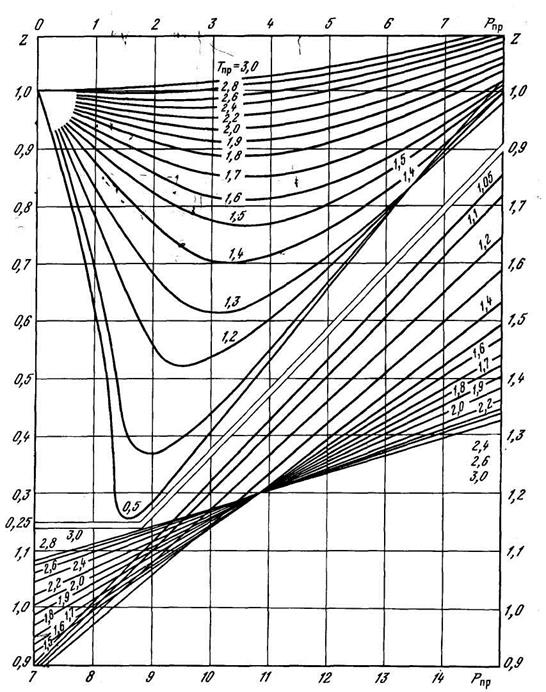
Рисунок 2.5 – Зависимость коэффициента сверхсжимаемости Z природного газа от приведенных давления и температуры.
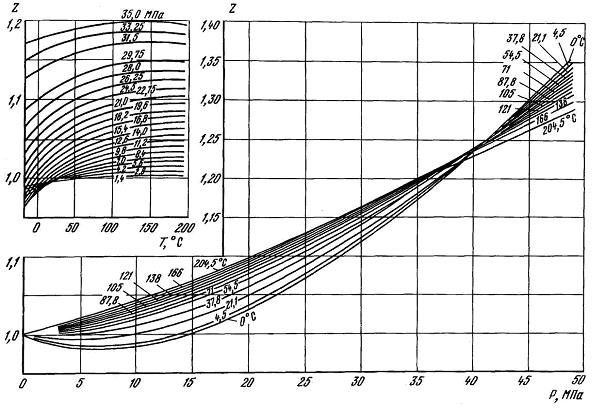
Рисунок 2.6 – Зависимость коэффициента сверхсжимаемости Z азота от давления и температуры.
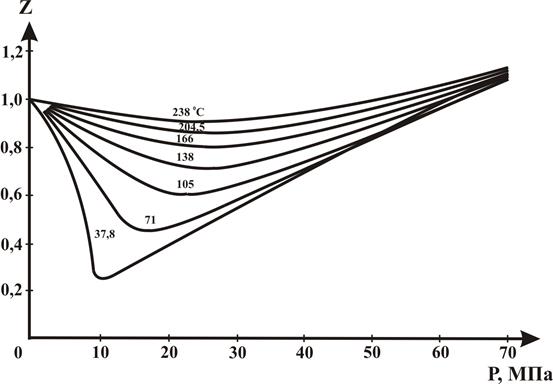
Рисунок 2.7 – Зависимость коэффициента сверхсжимаемости Z углекислого газа от давления и температуры.
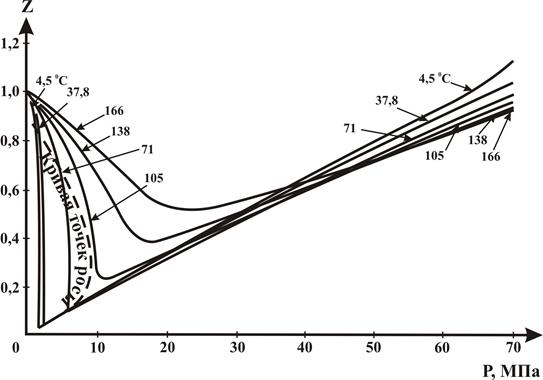
Рисунок 2.8 – Зависимость коэффициента сверхсжимаемости Z сероводорода от давления и температуры.
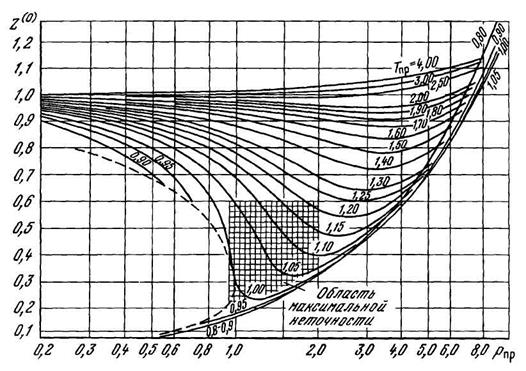
Рисунок 2.9 – Зависимость коэффициента сверхсжимаемости Z(0) простых веществ от приведенных давления и температуры.
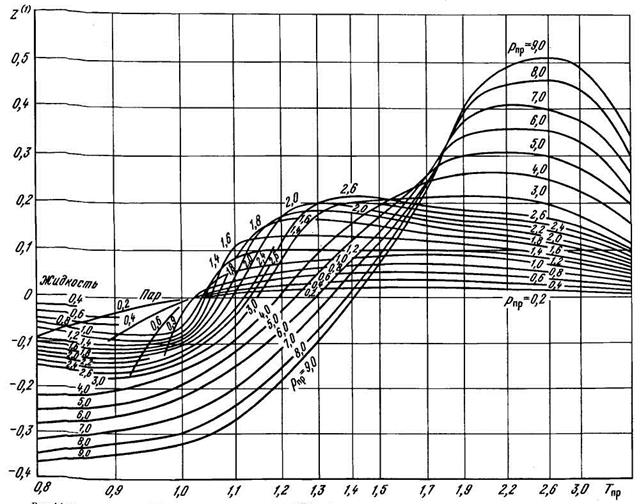
Рисунок 2.10 – Зависимость коэффициента сверхсжимаемости Z(1) несферических молекул от приведенного давления и температуры.
Если в газе содержится более 5% СО2, то значение Z должно быть рассчитано следующим образом:
– по формулам (2.3) вычисляют псевдокритические давление Рпк и температуру Тпк;
– вычисляется фактор ацентричности смеси ωсм, исключая из нее СО2, по формуле:
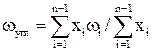 (2.23)
(2.23)
– по известной величине ωугл и концентрации СО2 в газе из графика, показанного на рисунке 2.11а и б, определяется величина ε, являющейся температурной поправкой для используемой при расчетах псевдокритической температуры. При наличии в газе СО2 и H2S значение ε может быть рассчитано и по формуле:
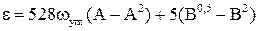 (2.24)
(2.24)
где А – суммарные мольные доли СО2 и H2S в газе; В – мольная доля H2S.
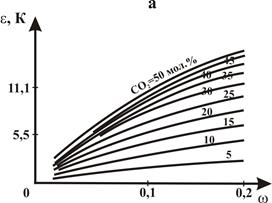
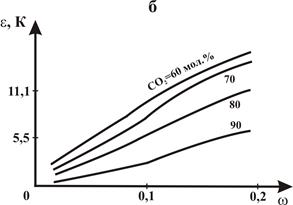
Рисунок 2.11 – Зависимость псевдокритической температурной поправки ε от концентрации в смеси СО2 и фактора ацентричности ω.
Зная Рпк, Тпк и ω вычисляют новые псевдокритические параметры:
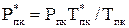 ;
; 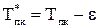 (2.25)
(2.25)
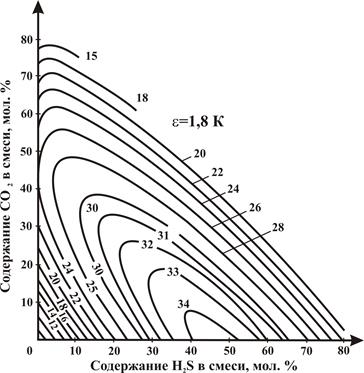
Рисунок 2.12 – Зависимость псевдокритической температурной поправки ε от концентрации в смеси СО2 и H2S.
Зная Рпк, Тпк и ω, вычисляют новые псевдокритические параметры:
По известным величинам заданных Р и Т и вычисленным Р*пк и Т*пк рассчитывают приведенные параметры:
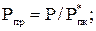
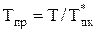 (2.26)
(2.26)
Используя графики, приведенные в [18] определяют Z(0) и Z(1), а затем, используя формулу (2.21), вычисляют значение Z.
При наличии в газе СО2 и H2S коэффициент сверхсжимаемости Z определяется аналогичным образом, с той лишь разницей, что при вычислении фактора ацентричности ωугл по формуле (2.23) из состава газа исключается не только СО2, но и H2S.
Если для определения газов, содержащих кислые компоненты, т.е. СО2 и H2S, используются графики, показанные на рисунках 2.1 и 2.2, то последовательность расчета выполняется следующим образом:
– по формулам (2.3) рассчитываются значения Рпк и Тпк;
– по графикам из рисунка 2.11 находят поправочный коэффициент ε;
– вычисляются новые псевдокритические параметры по формулам
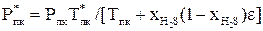 (2.27)
(2.27)
где xH2S – мольная доля сероводорода в смеси;
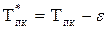 (2.28)
(2.28)
Используя формулу (2.26), рассчитывают величины Рпр и Тпр, а затем по этим приведенным параметрам из графика в[18] находят коэффициенты сверхсжимаемости Z(0) и Z(1). По известным Z(0) и Z(1) вычисляют Z.
Для более точных расчетов коэффициент сверхсжимаемости природных газов Z должен быть определен по кубическим уравнениям состояния газов, наиболее широкое распространение, среди которых получили уравнения Соаве, Редлиха-Квонга, Пенга-Робинсона. При этих методах расчета присутствие в газе кислых компонентов практически не влияет на величину погрешности при определении Z, если расчеты ведутся с учетом коэффициентов взаимодействия.
Для определения коэффициента сверхсжимаемости Z кубические уравнения состояния решаются относительно Z. Имеющее достаточно высокую точность уравнение Редлиха-Квонга для определения Z записывается в виде:
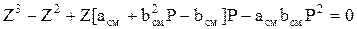 (2.29)
(2.29)
где
асм=∑xiai; bсм=∑xibi (2.30)
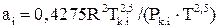 ;
; 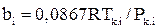 (2.31)
(2.31)
Уравнение (2.29) дает искомую точность для газообразных компонентов и их смесей. Наличие в смеси компонентов в жидком состоянии, а также молекул различного строения резко увеличивает погрешность расчетов.
Повышение точности величины Z при этом возможно путем введения поправки ΔZ на Z, определенной по формуле (2.21).
Наиболее точно коэффициент сверхсжимаемости Z определяется из уравнения состояния Пенга-Робинсона, имеющего относительно Z вид:
См. ниже за таблицей 2.5:
Z3–(l–A)Z2+(A–3B2–2B)Z–(AB–B2–B3)=0, (2.32)
где A=aP/R2T; B=bP/RT; (2.33)
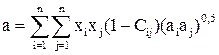 ;
; 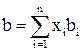 (2.34)
(2.34)
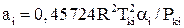 ;
; 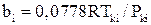 (2.35)
(2.35)
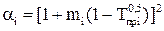 ;
; 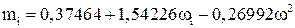 (2.36)
(2.36)
Значения коэффициента Cij в формуле (2.34) приведены в таблице 2.5.
Таблица 2.5 – Значение коэффициента Сij в формуле (2.34)
| Компоненты газа | Cij | ||||||||||||
| N2 | CO2 | H2S | CH4 | C2H6 | C3H8 | n-C4H10 | n-C5H12 | n-C6H14 | n-C7H16 | n-C8H18 | n-C9H20 | n-C10H22 | |
| N2 | 0,130 | 0,025 | 0,010 | 0,090 | 0,095 | 0,100 | 0,110 | 0,115 | 0,120 | 0,120 | 0,123 | ||
| CO2 | – | 0,135 | 0,105 | 0,130 | 0,125 | 0,115 | 0,115 | 0,115 | 0,115 | 0,115 | 0,115 | 0,115 | |
| H2S | – | – | 0,070 | 0,085 | 0,080 | 0,075 | 0,070 | 0,060 | 0,060 | 0,060 | 0,060 | 0,055 | |
| CH4 | – | – | – | 0,010 | 0,025 | 0,030 | 0,030 | 0,035 | 0,040 | 0,040 | 0,045 | ||
| C2H6 | – | – | – | – | – | 0,005 | 0,010 | 0,010 | 0,020 | 0,020 | 0,020 | 0,020 | 0,020 |
| C3H8 | – | – | – | – | – | 0,005 | 0,005 | 0,005 | 0,005 | 0,005 | 0,005 | ||
| n-C4H10 | – | – | – | – | – | – | 0,005 | 0,005 | 0,005 | 0,005 | |||
| n-C5H12 | – | – | – | – | – | – | – | ||||||
| n-C6H14 | – | – | – | – | – | – | – | – | |||||
| n-C7H16 | – | – | – | – | – | – | – | – | – | ||||
| n-C8H18 | – | – | – | – | – | – | – | – | – | – | |||
| n-C9H20 | – | – | – | – | – | – | – | – | – | – | – | ||
| n-C10H22 | – | – | – | – | – | – | – | – | – | – | – |
Более простой вариант
2. Коэффициент сверхсжимаемости газа рассчитываем по формуле Пенга – Робинсона:
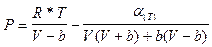 , (2.22)
, (2.22)
или
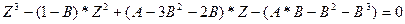 ,
,
где:
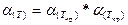 ,
,
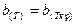 ,
,
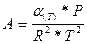 ,
,
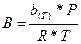 ,
,
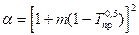 ,
,
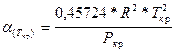 ,
,
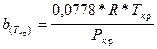 ,
,
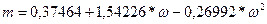
Вязкость газа (РИС 56-63)
Вязкость – физическое свойство вещества, которое проявляется при движении и характеризует сопротивляемость скольжению и сдвигу одной части относительно другой. Величина силы внутреннего трения между двумя движущимися слоями пропорциональна площади соприкосновения этих слоев и изменению скорости движения в направлении, перпендикулярном плоскости соприкосновения слоев. Коэффициент пропорциональности между силой внутреннего трения и произведением площади на изменение скорости движения называется коэффициентом динамической вязкости 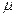 . Размерность коэффициента динамической вязкости: сила·время/(длина)2, т.е. H·с/м2 или Па·с., мПа·с
. Размерность коэффициента динамической вязкости: сила·время/(длина)2, т.е. H·с/м2 или Па·с., мПа·с
Коэффициент динамической вязкости 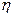 , отнесенный к плотности вещества при тех же условиях, называется кинематическим коэффициентом вязкости и имеет размерность м2/с.
, отнесенный к плотности вещества при тех же условиях, называется кинематическим коэффициентом вязкости и имеет размерность м2/с.
Коэффициент вязкости газа зависит от давления, температуры и состава газа. Методы определения коэффициента динамической вязкости газовых и газоконденсатных смесей основаны на использовании принципов соответственных состояний.
На рисунке 2.13 приведены зависимости для определения коэффициента приведенной динамической вязкости μ*пр природных газов при различных давлениях и температурах.
Величина μ*пр определяется по формуле:
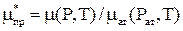 (2.37)
(2.37)
где μат – коэффициент вязкости газа при атмосферном давлении Рат=0,098 МПа и заданной температуре, который определяется по формуле:
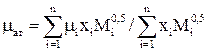 (2.38)
(2.38)
где μi – коэффициент динамической вязкости i-го компонента при заданной температуре и атмосферном давлении.
Величина μiат определяется из графика, показанного на рисунке 2.14, или по формуле:
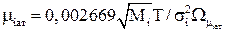 (2.39)
(2.39)
где Mi – молекулярная масса i-го компонента; 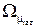 – интеграл столкновений; Т – температура газа; σi – параметр потенциалов.
– интеграл столкновений; Т – температура газа; σi – параметр потенциалов.
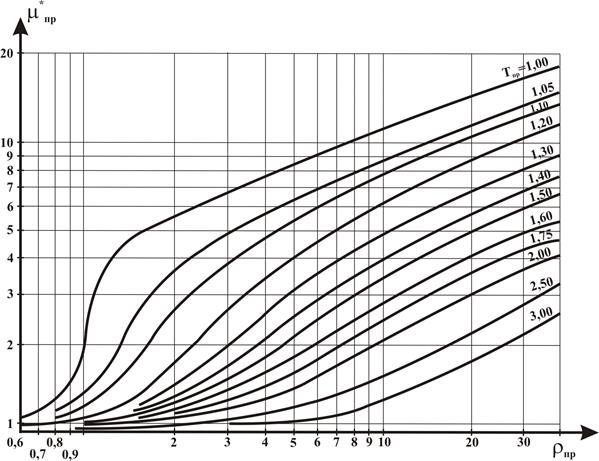
Рисунок 2.13 – Зависимость приведенной вязкости μ*пр от приведенных давления и температуры.
Значения констант σi и 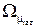 находят по таблицам 2.2 и 2.7 по известному компонентному составу газа. Для нахождения
находят по таблицам 2.2 и 2.7 по известному компонентному составу газа. Для нахождения 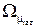 сначала вычисляют величину:
сначала вычисляют величину:
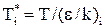 (2.40)
(2.40)
Величина (ε/k) дана в таблице 2.2. Значения 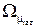 в зависимости от Т* приведены в таблицах 2.6 и 2.7.
в зависимости от Т* приведены в таблицах 2.6 и 2.7.
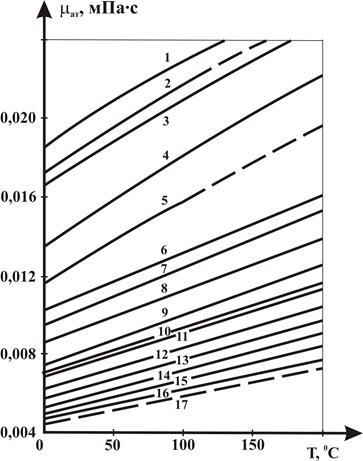
Рисунок 2.14 – Зависимость вязкости газов μат от температуры при атмосферном давлении:
1 – гелий; 2 – воздух; 3 – азот; 4 – углекислый газ; 5 – сероводород; 6 – метан; 7 – этилен; 8 – этан; 9 – пропан; 10 – i-бутан; 11 – n-бутан; 12 – n-пентан; 13 – n-гексан; 14 – n-гептан; 15 – n-октан; 16 – n-нонан; 17 – n-декан.
Если в составе газа присутствуют неуглеводородные компоненты, то их влияние на величину μат учитывается введением соответствующих поправок, зависящих от объемной концентрации неуглеводородных компонентов в смеси и от относительной плотности этой смеси при атмосферном давлении. Если вязкость газовой смеси μат определена из графика зависимости μат от относительной плотности 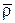 , показанной на рисунке 2.15, то значения поправок на вязкость неуглеводородных компонентов должны быть вычтены из величины μат. Значения поправок на присутствие в газе неуглеводородных компонентов могут быть вычислены аналитически по формулам:
, показанной на рисунке 2.15, то значения поправок на вязкость неуглеводородных компонентов должны быть вычтены из величины μат. Значения поправок на присутствие в газе неуглеводородных компонентов могут быть вычислены аналитически по формулам:
Таблица 2.6 – Значения интеграла столкновений 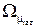 для полярных компонентов
для полярных компонентов
| T* | δ | |||||||
| 0,25 | 0,50 | 0,75 | 1,00 | 1,50 | 2,00 | 2,50 | ||
| 0,1 | 4,1005 | 4,2660 | 4,833 | 5,742 | 6,739 | 8,624 | 10,340 | 11,890 |
| 0,2 | 3,2626 | 3,3050 | 3,516 | 3,914 | 4,439 | 5,570 | 6,637 | 7,618 |
| 0,3 | 3,8399 | 2,8360 | 2,936 | 3,168 | 3,511 | 4,329 | 5,126 | 5,874 |
| 0,4 | 2,5310 | 2,5220 | 2,586 | 2,749 | 3,004 | 3,640 | 4,582 | 4,985 |
| 0,5 | 2,2837 | 2,2770 | 2,329 | 2,460 | 2,665 | 3,187 | 3,723 | 4,549 |
| 0,6 | 2,0838 | 2,0810 | 2,130 | 2,543 | 2,417 | 2,862 | 3,329 | 3,786 |
| 0,7 | 1,9220 | 1,9240 | 1,970 | 2,072 | 2,525 | 2,614 | 3,028 | 3,435 |
| 0,8 | 1,7902 | 1,7950 | 1,840 | 1,934 | 2,070 | 2,417 | 2,788 | 3,560 |
| 0,9 | 1,6823 | 1,6890 | 1,733 | 1,820 | 1,944 | 2,558 | 2,396 | 2,933 |
| 1,0 | 1,5929 | 1,6010 | 1,644 | 1,725 | 1,838 | 2,124 | 2,435 | 2,746 |
| 1,2 | 1,4551 | 1,4650 | 1,504 | 1,574 | 1,670 | 1,913 | 2,181 | 2,451 |
| 1,4 | 1,3650 | 1,400 | 1.461 | 1,344 | 1,754 | 1,989 | 2,528 | |
| 1,6 | 1,2800 | 1,2890 | 1,321 | 1,447 | 1,630 | 1,838 | 2,053 | |
| 1,8 | 1,2219 | 1,2310 | 1,259 | 1,306 | 1,370 | 1,332 | 1,718 | 1,912 |
| 2,0 | 1,1757 | 1,1840 | 1,509 | 1,251 | 1,307 | 1,451 | 1,618 | 1,715 |
| 2,5 | 1,0933 | 1,1000 | 1,119 | 1,150 | 1,193 | 1,304 | 1,435 | 1,578 |
| 3,0 | 1,0388 | 1,0440 | 1,059 | 1,083 | 1,117 | 1,504 | 1,310 | 1,428 |
| 3,3 | 0,9986 | 1,0040 | 1,016 | 1,035 | 1,062 | 1,133 | 1,520 | 1,319 |
| 4,0 | 0,9699 | 0,9732 | 0,9830 | 0,9991 | 1,021 | 1,079 | 1,153 | 1,536 |
| 5,0 | 0,9268 | 0,9291 | 0,9360 | 0,9473 | 0,9628 | 1,005 | 1,058 | 1,121 |
| 6,0 | 0,8917 | 0,8979 | 0,9030 | 0,9114 | 0,9230 | 0,9545 | 0,9955 | 1,044 |
| 7,0 | 0,8727 | 0,8741 | 0,8780 | 0,8845 | 0,8935 | 0,9181 | 0,9505 | 0,989 |
| 8,0 | 0,8538 | 0,8549 | 0,8580 | 0,8632 | 0,8703 | 0,8901 | 0,9164 | 0,948 |
| 9,0 | 0.8379 | 0,8338 | 0,8414 | 0,8456 | 0,8515 | 0,8678 | 0,8895 | 0,916 |
| 10,0 | 0,8243 | 0,8251 | 0,8273 | 0,8308 | 0,8356 | 0,8493 | 0,8676 | 0,890 |
| 12,0 | 0,8018 | 0,8024 | 0,8039 | 0,8065 | 0,8101 | 0,8201 | 0,8337 | 0,850 |
| 14,0 | 0,7836 | 0,7840 | 0,7852 | 0,7872 | 0,7899 | 0,7976 | 0,8081 | 0,821 |
| 16,0 | 0,7683 | 0,7687 | 0,7696 | 0,7712 | 0,7790 | 0,7730 | 0,7878 | 0,798 |
| 13,0 | 0,7552 | 0,7554 | 0,7562 | 0,7575 | 0,7592 | 0,7642 | 0,7711 | 0,780 |
| 20,0 | 0,7346 | 0,7435 | 0,7445 | 0,7455 | 0,7470 | 0,7512 | 0,7569 | 0,764 |
| 25,0 | 0,7198 | 0,7200 | 0,7204 | 0,7211 | 0,7221 | 0,7250 | 0,7289 | 0,734 |
| 30,0 | 0,7010 | 0,7011 | 0,7014 | 0,7019 | 0,7026 | 0,7047 | 0,7076 | 0,711 |
| 35,0 | 0,6854 | 0,6855 | 0,6858 | 0,6861 | 0,6867 | 0,6883 | 0,6905 | 0,693 |
| 40,0 | 0,6723 | 0,6724 | 0,6726 | 0,6728 | 0,6733 | 0,6745 | 0,6762 | 0,678 |
| 50,0 | 0,6510 | 0,6510 | 0,6512 | 0,6513 | 0,6516 | 0,6524 | 0,6534 | 0,655 |
| 75,0 | 0,6140 | 0,6241 | 0,6143 | 0,6145 | 0,6147 | 0,6148 | 0,6148 | 0,615 |
| 100,0 | 0,5887 | 0,5889 | 0,5894 | 0,5900 | 0,5903 | 0,3901 | 0,5895 | 0,488 |
Таблица 2.7 – Значения интеграла столкновений 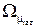 при различных T* для неполярных компонентов
при различных T* для неполярных компонентов
| T* | 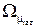 | T* | 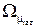 | T* | 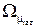 | T* | 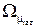 |
| 0,30 | 2,785 | 1,35 | 1,375 | 2,80 | 1,058 | 4,90 | 0,930 |
| 0,35 | 2,628 | 1,40 | 1,353 | 2,90 | 1,048 | 5,00 | 0,927 |
| 0,40 | 2,492 | 1,45 | 1,333 | 3,00 | 1,039 | 6,00 | 0,896 |
| 0,45 | 2,368 | 1,50 | 1,314 | 3,10 | 1,030 | 7,00 | 0,877 |
| 2,257 | 1,296 | 3,20 | 1,022 | 8,00 | 0,854 | ||
| 0,55 | 2,156 | 1,60 | 1,279 | 3,30 | 1,014 | 9,00 | 0,833 |
| 0,60 | 2,065 | 1,65 | 1,264 | 3,40 | 1,007 | 10,0 | 0,824 |
| 0,65 | 1,982 | 1,70 | 1,248 | 3,50 | 0,999 | 20,0 | 0,743 |
| 0,70 | 1,908 | 1,75 | 1,234 | 3,60 | 0,993 | 30,0 | 0,700 |
| 0,75 | 1,841 | 1,80 | 1,221 | 3,70 | 0,987 | 40,0 | 0,672 |
| 0,80 | 1,780 | 1,85 | 1,209 | 3,80 | 0,981 | 50,0 | 0,650 |
| 0,85 | 1,725 | 1,90 | 1,197 | 3,90 | 0,975 | 60,0 | 0,633 |
| 0,90 | 1,675 | 1,95 | 1,136 | 4,00 | 0,970 | 70,0 | 0,619 |
| 0,95 | 1,629 | 2,00 | 1,175 | 4,10 | 0,965 | 80,0 | 0,608 |
| 1,00 | 1,587 | 2,10 | 1,156 | 4,20 | 0,960 | 90,0 | 0,597 |
| 1,05 | 1,349 | 2,20 | 1,138 | 4,30 | 0,955 | 100,0 | 0,588 |
| 1,10 | 1,314 | 2,30 | 1,122 | 4,40 | 0,951 | 200,0 | 0,532 |
| 1,15 | 1,352 | 2,40 | 1,107 | 4,50 | 0,946 | 300,0 | 0,502 |
| 1,20 | 1,382 | 2,50 | 1,093 | 4,60 | 0,943 | 400,0 | 0,481 |
| 1,25 | 1,424 | 2,60 | 1,081 | 4,70 | 0,938 | – | – |
| 1,30 | 1,399 | 2,70 | 1,069 | 4,80 | 0,934 | – | – |
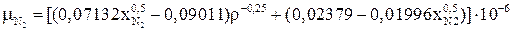 (2.41)
(2.41)
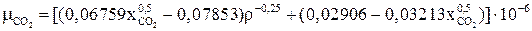 (2.42)
(2.42)
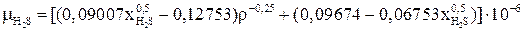 (2.43)
(2.43)
Погрешности определения μ*пр из рисунка 2.13 составляют 3÷5%. 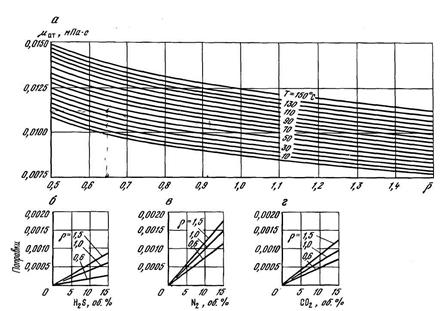
Рисунок 2.15 – Зависимость вязкости углеводородных газов μ от их относительных плотностей по воздуху (а) и поправки на величину вязкости газов, содержащих H2S (б), N2 (в), CO2 (г).
Влагосодержание газа
Влагосодержание – это количество паров воды, растворенных в единице объема природного газа при заданных условиях. Содержание водяных паров в газе характеризуется абсолютной и относительной влажностью. Под абсолютной влажностью газа W при заданных давлении и температуре понимается отношение массы водяных паров, содержащихся в газе, к объему, приведенному к стандартным условиям этого газа, из которого удалены пары воды. Абсолютная влажность измеряется в кг/1000 м3. Относительная влажность - это отношение фактического содержания паров воды в единице объема газа при заданных давлении и температуре к его влагоемкости, т.е. к количеству водяных паров в том же объеме и при тех же давлении и температуре, но при помощи насыщения газа парами воды. Относительная влажность измеряется в долях единицы или в процентах.
Влагосодержание газа зависит от состава газа, давления, температуры и физико-химических свойств конденсированной воды, с которой газ находится в термодинамическом равновесии, оно определяется по формуле
W=W0,6CcCp, (2.44)
где W0,6 – влагосодержание газа с относительной плотностью 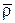 =0,6 с пресной водой; Сс – поправка на соленость воды; Ср – поправка на отклонение плотности данного газа от величины
=0,6 с пресной водой; Сс – поправка на соленость воды; Ср – поправка на отклонение плотности данного газа от величины 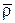 =0,6.
=0,6.
Влагосодержание газа с относительной плотностью 0,6 и поправки на соленость воды и на плотность газа определяются графически из рисунка 2.16. При отрицательных температурах, что связано с условиями подготовки газов на промыслах и газоперерабатывающих заводах, необходимо учесть и температурную поправку Сt, используя при этом графическую зависимость Сt от температуры Т для различных давлений, показанную на рисунке 2.17.
Величина W0,6 может быть рассчитана по формуле, полученной путем аппроксимации графической зависимости, показанной на рисунке 2.16:
W0,6=А/Р+В (2.45)
где А – влагосодержание идеального газа; В – коэффициент, зависящий от состава газа; Р – давление.
Значения коэффициентов А и В приведены в таблице 2.8. Эти же коэффициенты могут быть определены аналитическим путем.
Величину А можно определить по формуле:
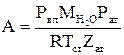 (2.46)
(2.46)
где Рвп – давление насыщенного пара воды над конденсированной фазой, которое может быть определено по данным, приведенным в таблицах 2.3 или 2.9 и из рисунка 2.3 для различных температур, или рассчитано приближенно при 203≤Т≤373 К по формуле:
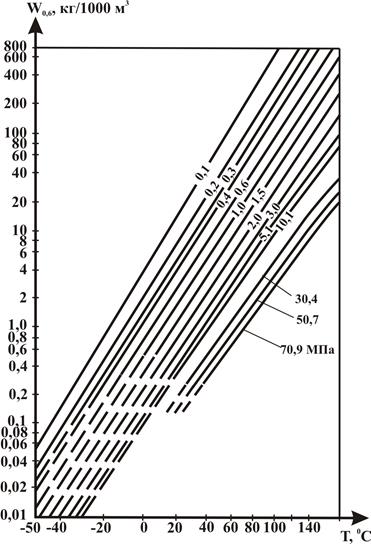
Рисунок 2.16 – Зависимость влагосодержания природного газа W0,6 с относительной плотностью 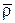 =0,6 от давления и температуры.
=0,6 от давления и температуры.
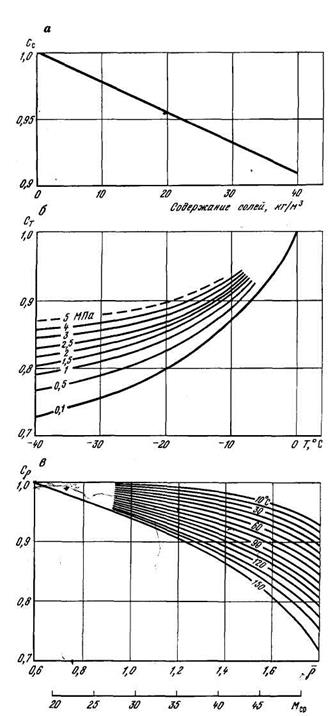
Рисунок 2.17 – Зависимости поправочных коэффициентов на влажность газа от содержания солей (а), температуры (б) и относительной плотности 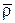 (или молекулярной массы М) (в).
(или молекулярной массы М) (в).
Таблица 2.8 – Значения коэффициентов А и В в формуле (2.45).
| Т, К | А | В | Т, К | А | В | Т, К | А | В |
| 0,1451 | 0,00347 | 8,20 | 0,0630 | 120,0 | 0,487 | |||
| 0,1780 | 0,00402 | 9,39 | 0,0696 | 138,0 | 0,521 | |||
| 0,2189 | 0,00465 | 10,72 | 0,0767 | 152,0 | 0,562 | |||
| 0,2670 | 0,00538 | 12,39 | 0,0855 | 166,5 | 0,599 | |||
| 0,3235 | 0,00623 | 13,94 | 0,0930 | 183,3 | 0,645 | |||
| 0,3930 | 0,00710 | 15,75 | 0,1020 | 200,5 | 0,691 | |||
| 0,4715 | 0,00806 | 17,87 | 0,1120 | 219,0 | 0,741 | |||
| 0,5660 | 0,00921 | 20,15 | 0,1227 | 238,5 | 0,793 | |||
| 0,6775 | 0,01043 | 22,80 | 0,1343 | 260,0 | 0,841 | |||
| 0,8090 | 0,01168 | 25,50 | 0,1453 | 283,0 | 0,902 | |||
| 0,9600 | 0,01340 | 28,70 | 0,1595 | 306,0 | 0,965 | |||
| 1,1440 | 0,01510 | 32,30 | 0,1740 | 335,0 | 1,023 | |||
| 1,3500 | 0,01705 | 36,10 | 0,1895 | 363,0 | 1,083 | |||
| 1,5900 | 0,01927 | 40,50 | 0,2070 | 394,0 | 1,148 | |||
| 1,8680 | 0,02115 | 45,20 | 0,2240 | 427,0 | 1,205 | |||
| 2,1880 | 0,02290 | 50,80 | 0,2420 | 462,0 | 1,250 | |||
| 2,5500 | 0,02710 | 56,25 | 0,2630 | 501,0 | 1,290 | |||
| 2,9900 | 0,03035 | 62,70 | 0,2850 | 537,5 | 1,327 | |||
| 3,4800 | 0,03380 | 69,25 | 0,3100 | 582,5 | 1,367 | |||
| 4,0300 | 0,03770 | 76,70 | 0,3350 | 624,0 | 1,405 | |||
| 4,6700 | 0,04180 | 85,29 | 0,3630 | 672,0 | 1,445 | |||
| 5,4000 | 0,04640 | 94,99 | 0,3910 | 725,0 | 1,487 | |||
| 6,2250 | 0,05150 | 103,00 | 0,4220 | 776,0 | 1,530 | |||
| 7,1500 | 0,05710 | 114,00 | 0,4540 | 1093,0 | 2,620 |
Таблица 2.9 – Значения Рвп от температуры.
| Т, К | Рвп, МПа | Т, К | Рвп, МПа | Т, К | Рвп, МПа |
| 0,000013 | 0,00126 | 0,02057 | |||
| 0,000023 | 0,00176 | 0,02582 | |||
| 0,000038 | 0,00241 | 0,03219 | |||
| 0,000065 | 0,00327 | 0,03982 | |||
| 0,000106 | 0,00441 | 0,04892 | |||
| 0,000170 | 0,00580 | 0,05971 | |||
| 0,000268 | 0,00762 | 0,07242 | |||
| 0,000496 | 0,00989 | 0,08731 | |||
| 0,000628 | 0,01274 | 0,10466 | |||
| 0,000902 | 0,01625 | 0,14799 |
Рвп=ехр[–0,60212(0,01Т)4+1,475(0,01Т)3–2,97304(0,01Т)2+
+7,19863(0,01Т)+6,41465] (2.47)
и при 373≤Т≤623 К по формуле:
Рвп=ехр[–0,0366(0,01Т)4+0,4375(0,01Т)3–2,2148(0,01Т)2+
+6,8574(0,01Т)+6,4856] (2.48)
Значение коэффициента В в формуле (2.45) приближенно может быть определено по формуле:
В=10-3ехр[0,0685(0,01Т)4–0,3798(0,01Т)3+1,06606(0,01Т)2–
–2,00075(0,01Т)+4,2216] (2.49)
где Т – температура, 0С.
Значение W0,6 может быть вычислено по формуле, полученной путем обработки данных по А и В, приведенных в таблице 2.8:
W0,6=0,4736ехр(0,0735T–0,00027T2)+0,0418ехр(0,054T–0,0002T2) (2.50)
При проведении расчетов со значительным объемом вычислений целесообразно поправки на соленость воды и на плотность с учетом влияния температуры производить аппроксимацией кривых, показанных на рисунке 2.17а, б в виде:
Сс=1–0,225·10-5∙К (2.51)
Сρ=10-7Т2–1,1·10-3Т 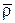 –0,079
–0,079 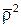 +0,73·10-3Т+0,156
+0,73·10-3Т+0,156 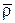 +0,927 (2.52)
+0,927 (2.52)
где К – соленость воды, кг/м3; Т – температура, 0С; 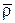 – относительная плотность газа.
– относительная плотность газа.
Приведенные выше графические и расчетные методы определения влагосодержания газа не учитывают наличие кислых компонентов. Наличие в газе СО2 и H2S повышает, а N2 снижает влагосодержание газов.
Если содержание сероводорода в природном газе превышает 20 об.%, то влагосодержание определяют по правилам аддитивности, учитывающей наличие в газе сероводорода:
W0,6 =хW+хС02WC02+xH2SWH2S (2.53)
где х, хCO2, хH2S – мольные доли углеводородных компонентов, двуокиси углерода и сероводорода в газе; W, WCO2, WH2S – содержание влаги в углеводородной части газа, двуокиси углерода и сероводорода.
Значения W, WCO2, WH2S определяются графически из рисунков 2.16, 2.18 и 2.19а.
