Г) окисление сульфита натрия перманганатом калия в нейтральной и щелочной средах
Экспериментальная часть
Цель: Исследовать окислительно-восстановительные реакции
Опыт 1
А)Выполнение опыта:к 3-4 каплям раствора иодида калия добавьте 5-7 капель хлорной воды.
Запись данных опыта: образовался жёлтый осадок.
Уравнение реакции
2K+ I - + Cl20 → 2K+ Cl - + I20;
Cl20 – 2e - → 2 Cl- │ 2
2I- + 2e - → I20 │ 2
Б) окислительные свойства серной кислоты.
Взаимодействие разбавленной кислоты с металлами.
Выполнение опыта:поместить в одну пробирку кусочек медной стружки, в другую один микрошпатель порошка цинка, а в третью – кусочек магниевой ленты и прибавить в каждую пробирку по 6-8 капель 10% (2 н) раствора серной кислоты.
Запись данных опыта:необходимо написать уравнения реакции в тех случаях, когда они протекают, указать какой ион выполняет по отношению к металлам функцию окислителя.
Запись данных опыта:
2Zn0 + H2+ SO4 - → Zn2+2 SO4- 2 + H20 ↑ Реакция протекает средне
Zn0 – 2e - → Zn+2│ 2
2H+ + 2e - → H20 │ 2 — Окислитель
Mg0 + H2+ SO4 - → Mg +2 SO4 - + H20 ↑ Реакция протекает средне
Mg 0 – 2e - → Mg +2 │ 2
2H+ + 2e - → H20 │ 2 — Окислитель
Реакция с медью не протекает.
В) окислительные свойства перманганата калия.
Окисление сульфида натрия перманганатом калия в кислой среде.
Выполнение опыта:налейте в пробирку 2-3 капли раствора перманганата калия и такой же объем разбавленной 2н серной кислоты, а затем прибавляйте по каплям раствор сульфида натрия до полного обесцвечивания раствора.
Запись данных опыта: какую степень окисления приобретает марганец в кислой среде? Укажите, какую функцию выполняют в ней сульфид натрия и серная кислота.
KMnO4 + H2SO4 + Na2S → MnSO4 + K2SO4 + Na2SO4 + H2O
pH<7, H+, H2O;
| MnO4- + 8H+ + 5e- → Mn+2 + 4H2O | |
| S-2 + 4H2O – 8e- → SO4-2 + 8H+ |
8MnO4- + 64H+ + 5S-2 + 20H2O → 8Mn+2 + 32H2O + 5SO4-2 + 40H+
8MnO4- + 24H+ + 5S-2 → 8Mn+2 + 12H2O + 5SO4-2
-8 + 24 – 10 → +16 – 10
+6 → +6
8KMnO4 + 12H2SO4 + 5Na2S → 8MnSO4 + 4K2SO4 + 5Na2SO4 + 12H2O
В кислой среде Mn принимает степень окисления +2, выполняя роль окислителя. Сульфид натрия выполняет роль восстановителя. Серная кислота определяет кислотность среды.
г) окисление сульфита натрия перманганатом калия в нейтральной и щелочной средах
Выполнение опыта: две пробирки налить по 3-4 капли раствора перманганата калия и такой же объем сульфита натрия. В одну из пробирок налить 5-6 капель концентрированного раствора гидроксида натрия или калия.
Запись данных опыта: как изменится окраска раствора? Какие ионы придают растворам окраску? Сделать вывод о характере продуктов восстановления перманганата иона в зависимости от рН среды. В какой среде перманганат-ион проявляет более высокую окислительную активность?
KMnO4 + Na2SO3 → реакция не идет
KMnO4 + Na2SO3 + KOH → K2MnO4 + Na2SO4 + H2O
pH>7, OH-, H2O;
| MnO4- + e- → MnO4-2 | |
| SO3-2 + 2OH- - 2e- → SO4-2 + H2O |
2MnO4- + SO3-2 + 2OH- → 2MnO4-2 + SO4-2 + H2O
-2 - 2 - 2→ -4 -2
-6 → -6
2KMnO4 + Na2SO3 + 2KOH → 2K2MnO4 + Na2SO4 + H2O
Окраска меняет фиолетовый цвет на темный, что связано с восстановлением марганца от Mn+7 до Mn+6. Темный цвет раствору придают ионы MnO4-2. Перманганат-ион при pH>7 восстанавливается до иона MnO4-2; при pH<7 восстанавливается до Mn+2. Перманганат-ион проявляет более высокую окислительную активность в кислой среде
Опыт2
а)Восстановители элементарные вещества
Поместили в 4 пробирки по 1-2 кусочка цинка, железа, олова или меди и прибавить по 5-7 капель 10% раствора соляной кислоты.
1) Zn + 2HCl → ZnCl2 + H2↑
2) 2Fe + 6HCl → 2FeCl3 + 3H2↑
3) Sn + 2HCl → SnCl2 + H2↑
4) Cu + HCl → не протекает
Наиболее интенсивнее протекает 1-я реакция, менее интенсивное протекает 2-я реакция, интенсивность меньше всего в 3-ей реакции, 4-я не протекает. Интенсивность зависит активности металла, которая идет в порядке Zn, Fe, Sn, Cu.
б)Восстановительные свойства сероводорода и сульфид-ионов. Восстановление сульфид-ионами хроматов и дихроматов.
К 2-3 каплям раствора дихромата калия прилили 4-5 капли раствора сульфида аммония и слегка нагрели.
K2Cr2O7 + (NH4)2S 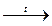 2Cr(OH)2↓ + S↓ + N2↑+ 2KOH + H2O
2Cr(OH)2↓ + S↓ + N2↑+ 2KOH + H2O
В осадок выпадают гидроксид хрома (II) и сера, которые имеет желтый цвет.
Опыт 3.
а) Окислительно-восстановительная двойственность. Двойственное поведение пероксида водорода.
К подкисленному раствору перманганата калия добавили по каплям раствор пероксида водорода до полного обесцвечивания раствора.
KMnO4 + HCl + H2O2 → KCl + MnCl2 + H2O + O2↑
pH<7, H+, H2O
| MnO4- + 8H+ + 5e- → Mn+2 + 4H2O | |
| H2O2 – 2e- → O2 + 2H+ |
2MnO4- + 16H+ + 5H2O2 → 2Mn+2 + 8H2O + 5O2 + 10H+
2MnO4- + 6H+ + 5H2O2 → 2Mn+2 + 8H2O + 5O2
-2 + 6 → +4
+4 → +4
2KMnO4 + 6HCl + 5H2O2 → 2KCl + 2MnCl2 + 8H2O + 5O2↑
Выделяется кислород.
б) Окислительно-восстановительные свойства иодид-иона.
В две пробирки внесли по 3 капли иодида калия и по 2 капли 2н раствора серной кислоты. В одну пробирку добавили 3 капли хлорной воды, в другую 3 капли сероводородной воды.
2KI + H2SO4 + Cl2 → 2KCl + H2SO4 + I2↓
| 2I- -2e- → I20 | |
| Cl20 + 2e- → 2Cl- |
2I- + Cl20 → I20 + 2Cl-
-2 → -2
2KI + H2SO4 + Cl2 → 2KCl + H2SO4 + I2↓
Ион I- проявляют восстановительные свойства.
Реакция не протекала во втором случае с сероводородом, т. к. сера находится в минимальной степени окисления -2 и не может более восстановиться.
в) Окислительно-восстановительная двойственность. Двойственное поведение азотистой кислоты и нитритов.
К 1-2 каплям раствора перманганата калия добавили 3-4 капли разбавленной серной кислоты, а затем по каплям прибавили раствор нитрита натрия или калия до полного обесцвечивания раствора.
KMnO4 + H2SO4 + KNO2 → MnSO4 + K2SO4 + NO2↑
pH<7, H+, H2O
| MnO4- +8H- + 5e- → Mn+2 + 4H2O | |
| NO2- - e- → NO20 |
MnO4- + 8H+ + 5NO2- → Mn+2 + 4H2O + NO20
+2 → +2
KMnO4 + 4H2SO4 + 5KNO2 → MnSO4 + 3K2SO4 + 5NO2↑
При протекании реакции выделился бурый газ NO2, что связано с окислением иона NO- и восстановлением иона MnO4- до Mn+2.
г) Окислительные и восстановительные свойства серы в соединениях в зависимости от степени окисления.
В три пробирки внесли по три капли раствора перманганата калия и 2 н раствора уксусной кислоты (для создания кислой среды). В одну пробирку прибавили 3 капли свежеприготовленной сероводородной воды, во вторую несколько кристалликов сульфита натрия, в третью 3 капли концентрированной кислоты.
1) KMnO4 + CH3COOH + H2S → MnSO4 + K2SO4 + (CH3COO)2Mg + H2O
pH<7, H+, H2O
| MnO4- +8H+ + 5e- → Mn+2 + 4H2O | |
| S-2 + 4H2O – 8e- → SO4-2 + 8H+ |
8MnO4- + 64H+ + 5S-2 + 20H2O → 8Mn+2 + 32H2O + 5SO4-2 + 40H+
8MnO4- + 24H+ + 5S-2 + → 8Mn+2 + 12H2O + 5SO4-2
- 8 + 24 – 10 → 16 – 10
+6 → +6
8KMnO4 + 14CH3COOH + 5H2S → MnSO4 + 4K2SO4 + 7(CH3COO)2Mg + 12H2O
2) KMnO4 + CH3COOH + Na2SO3 → MnSO4 + H2O + Na2SO4 + CH3COONa + K2SO4
pH<7, H+, H2O
| MnO4- +8H+ + 5e- → Mn+2 + 4H2O | |
| SO3-2 + H2O – 2e- → SO4-2 + 2H+ |
2MnO4- + 16H+ + 5SO3-2 + 5H2O → 2Mn+2 + 8H2O +5SO4-2 + 10H+
2MnO4- + 6H+ + 5SO3-2 → 2Mn+2 + 3H2O +5SO4-2
-2 + 6 – 10 → 4 – 10
-6 → -6
2KMnO4 + 6CH3COOH + 5Na2SO3 → 2MnSO4 + 3H2O + 2Na2SO4 + 6CH3COONa + K2SO4
В первых двух случаях реакция проходила с восстановлением марганца и окислением атомов серы. При добавлении в 3-ю пробирку концентрированной серной кислоты реакция не происходила, т. к. сера находится в высшей степени окисления +6 и не может быть восстановителем.
Опыт 4.
