Окисление с участием оксидаз
Происходит в основном на внешней мембране митохондрий. Оксидазы – аэроб. флавиновые ДГ, которые переносят электрон от окисляемых субстратов по короткой цепи на кислород. Пример: оксисление некоторых аминокислот ферментами аминокислотооксидазами, аминов – аминооксидазами, ксантина – ксантинооксидазами. В результате такого оксиления в тканях образуется очень активный радикал кислорода:
- Супероксид О2+1е→ФП О2- - ион – радикал
- Пероксид О2+2е→ФП О2 – пероксид радикал
В физиологических условиях образуется очень незначительное количество активных форм О2. Они выполняют функцию регуляции проницаемости клеточных мембран путем окисления липидов в составе мембран, активность мембранных ферментов, участвуют в синтезе биологически активных эйкозаноидов. Особо важную роль в физиологических условиях АФК играют в фагоцитозе т.к принимают участие в нескольких механизмах:
1. При контакте с чужеродными веществами в фагоцитах активируется мембранная флавиновая оксидаза под действием которой образуются ион-радикалы О2 которые вызывают окисление чужеродного вещества.
2. В фагоцитах активируется фермент миелопероксидаза, которая путем окисления хлоридов через образование НСLО образует атомарный О*, который так же окисляет чужеродные вещества и повышает проницаемость мембранных фагоцитов и облегчает эндоцитоз.
3. Образующийся из NО сильный окислитель ONOO так же участвует в фагоцитозе
4. Пептиды – формируют в поглощаемых микроорганизмах дополнительные ионные каналы и способствуют разрушению микроорганизмов
При фагоцитозе потребление кислорода увеличивается в 2-5 раз и это явление называется окислительный взрыв.
В патологических условиях высокие концентрации активных форм кислорода оказывают токсический эффект, окисляются липиды, белки, нуклеиновые кислоты. NO-R обладает угнетающим свойством окислительного фосфолирирования. Поэтому в организме для разрушения избыточных концентраций активных форм кислорода существует защитная антиокислительная система. Она представлена ферментами и веществами неферментной природы. К антиоксиданстным веществам относят:
- Супероксиддесмутаза – разрушает ион-R кислорода
- Каталаза
- Глютатионпероксидаза – разрушает пероксидазы при участии пептила глютатиона.
К неферментативным веществам относят: белки содержащие SH, глютатион, витамины Е, А, С, некоторые гормоны, белки крови (трансферрин, церулоплазмин), селен.
Окисление с участием оксигеназ.
Наиболее активно протекает в ЭПС.
Диокисгеназы – окисляют субстрат путем присоединения двух атомов кислорода R + O2→ДОГ RO2. Пример: диоксигеназа гомогентизиновой кислоты.
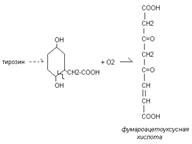
Окисление триптофанприролазы с разрывом пирольного кольца.
Мнооксигеназное окисление – окисляет субстрат путем присоединение кислорода. Это окисление активно происходит в ЭПС и часто в печени где на него тратится до 50% поглощаемого кислорода. В микросомальном окислении участвуют дополнительные вещества – косубстраты НАДН2 или витамин С. Микросомальное окисление в основном выполняет антитоксическую функцию (продукты гниения белков, лекарственные вещества). Путем этого окисления синтезируются некоторые аминокислоты (тир) биогенные амины. Благодаря микросомальному окислению происходит бласттрансформация различных ксенобионтов. В этих веществах формируется гидроксильная группа и к ней присоединяется глюкуроновоая кислота, Н2SО4, глютатион.
