Сосудистая реакция и экссудация
Включает в себя триаду патологических реакций:
1. Изменение кровообращения в очаге воспаления
2. Выход жидкой части крови из сосудов
3. Эмиграция (выход лейкоцитов из сосудов в очаг воспаления и развитие фагоцитарной реакции.
Параллельно с расстройствами микроциркуляции закономерно нарастают явления экссудации, то есть выхода жидкой части крови из сосудистого русла. Жидкость, выходящая за пределы сосудов, носит название экссудата, который отличается сравнительно высоким содержанием белка (до 5%), обилием ферментов, форменных элементов крови, интерлейкинов, продуктов распада тканей. При септическом воспалении экссудат содержит микроорганизмы.
Экссудация определяется формированием следующих факторов патогенеза:
1. Повышение внутрисосудистого гидростатического давления в капилярах и венулах.
2. Повышение проницаемости сосудистой стенки под действием клеточных и гуморальных медиаторов.
3. Физико-химические сдвиги в очаге воспаления (гиперонкия, гиперосмия).
Значение процесса экссудации в очаге воспаления может быть как положительное, так и отрицательное (рис. 8).
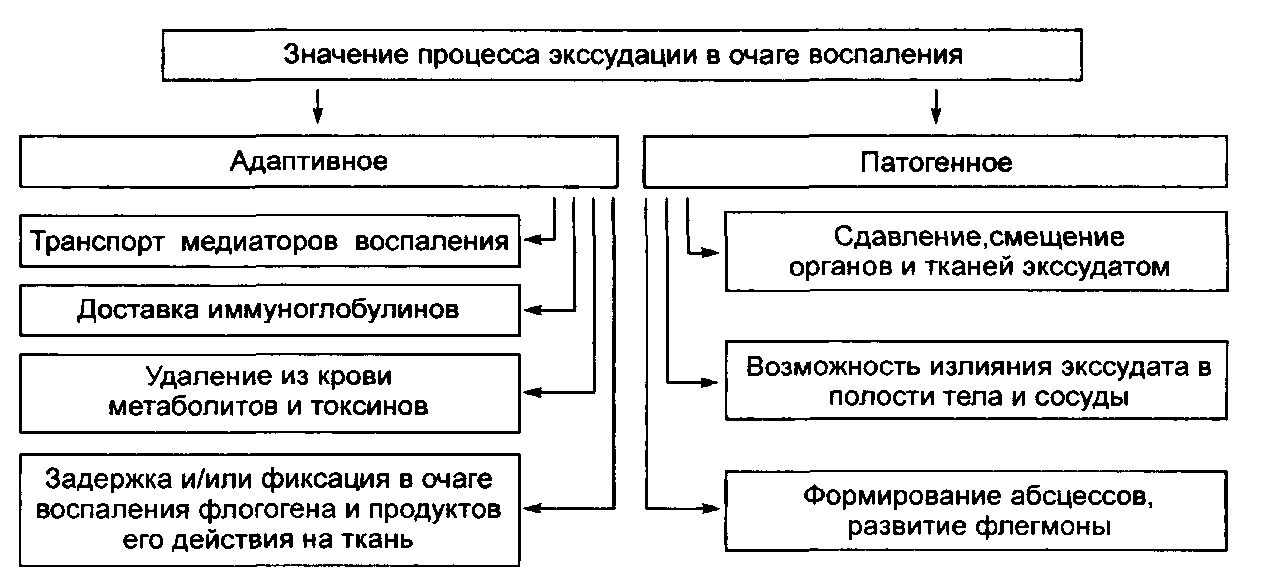
Рис. 8. Значение процесса экссудации в очаге воспаления.
Следующий этап второй стадии воспаления – выход лейкоцитов за пределы стенок сосудов – носит название эмиграции.
Эмиграция включает в себя три стадии:
1. Краевое стояние лейкоцитов (рис.9)
2. Эмиграция лейкоцитов из сосудистого русла (рис. 10)
3. Фагоцитоз
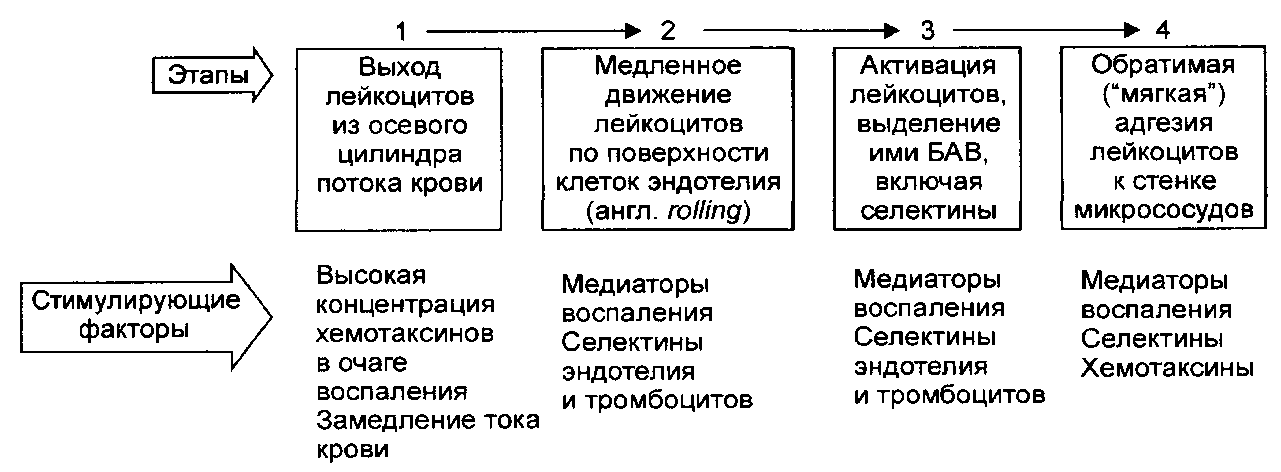
Рис. 9. Этапы стадии краевого стояния лейкоцитов и факторы, стимулирующие краевое стояние.
 |
Рис. 10. Краевое стояние и выход лейкоцитов в очаг воспаления
Исходя из закона эмиграции И.И. Мечникова, первыми из сосудистого русла мигрируют нейтрофилы и эозинофилы, а за ними устремляются моноциты. В первые сутки в воспалительном экссудате будут преобладать нейтрофилы, а на 3-4 сутки определяется большее процентное содержание макрофагальных элементов.
3. Фагоцитоз – эволюционно выработанная защитно-приспособительная реакция организма, заключающаяся в узнавании, активном поглощении и переваривании микроорганизмов, разрушенных клеток и инородных частиц специализированными клеточными компонентами или фагоцитами.
3. Пролиферацияначинается с периферии очага повреждения образованием так называемой грануляционной ткани. Свое название она получила из-за наличия гранулем (от лат. granulum – зернышко). Центр гранулемы представлен капилляром, сформированным из эндотелиальных клеток и клеток адвентиции, окруженных мезенхимальными элементами. Узелки сливаются и образуют демаркационный вал – барьер, отделяющий очаг воспаления от здоровой ткани. Основное значение в последующем принадлежит образующимся в результате дифференцировки клеток соединительной ткани фибробластам.
Со временем грануляционная ткань претерпевает изменения. Количество сосудов и клеток в ней уменьшается. Фибробласты пролиферируют, дифференцируются в зрелые формы — фиброциты, которые синтезируют коллагеновые волокна, формирующие рубцовую ткань.
Анализируя весь механизм развития воспалительной реакции, все основные компоненты воспаления в виде смены его фаз альтерации, экссудации и пролиферации можно представить схематично (рис. 12.). Как видно на этом рисунке, вектор процесса направлен на восстановление целостности морфофункциональных структур. Условия успешного хода воспалительного процесса состоят в реализации и затухании острых альтеративных и экссудативных изменений при полной деструкции или устранении флогогенного агента (фагоцитоз). Второе условие перехода к репаративным процессам – накопление в очаге ингибиторов протеолитических ферментов, антиагрегантов, фибринолитических молекул (гепарин, ингибиторы комплемента и плазмина). Стимуляторами пролиферации и ограничителями апоптоза выступают медиаторы воспаления, которые обладают ростостимулирующими свойствами (происходящими из макрофагов, лимфоцитов тромбоцитов, фибробластов).
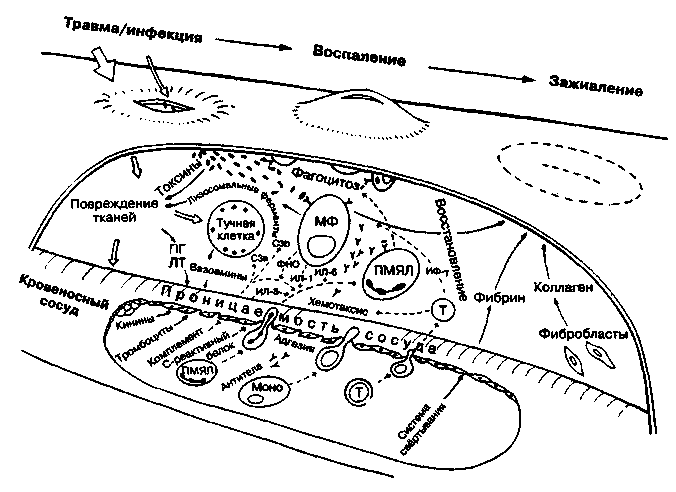
Рис. 12.Обобщенный анализ воспалительного процесса, заканчивающегося успешным репаративным восстановлением целостности ткани (по Дж. Плейферу)
