Биотехнология рекомбинантных белков
СОДЕРЖАНИЕ
Введение……………………………………………………………………………..…….3
1 Биотехнология рекомбинантных белков…………………………………………..…..4 2 Микроорганизмы для производства рекомбинантных белков…..………………..….7 3 Промышленное производство рекомбинантного инсулина……………….…………9 4 Описание технологического процесса производства ……………………………….14
Заключение…………………………………………...…………………………………..16
Список использованных источников…………………………………………………...17
ВВЕДЕНИЕ
Для получения коммерческих продуктов с помощью рекомбинантныхмикроорганизмов необходимо сотрудничество специалистов в двух областях: молекулярных биологов и биотехнологов. Задача молекулярных биологов заключается видентификации, изучении свойств, модификации нужных генов и создании эффективных систем их экспрессии в клетках микроорганизмов, которые можно будет использовать для промышленного синтеза соответствующего продукта, азадача биотехнологов — в обеспечении условийоптимального роста нужного рекомбинантногомикроорганизма с целью получения продукта снаибольшим выходом.
Микроорганизмы для производства рекомбинантных белков
В проблеме производства рекомбинантных белков очень важно, чтобы используемые в этом случае микроорганизмы, в которые вносят чужеродные гены, удовлетворяли бы следующим свойствам:
1. Метаболизм микроорганизма должен быть хорошо изучен, поэтому в качестве продуцентов рекомбинантных белков используют именно такие микроорганизмы: это Escherichia coli, Bacillus subtilis, Saccharomyces cerevisie.
2. Микроорганизмы должны быть не патогенны.
3. Микроорганизмы должны хорошо и интенсивно размножаться в условиях ферментера.
4. Желательно, чтобы микроорганизм был способен выделять секретируемый им чужеродный белок в среду. Это можно достичь, если ввести в клетку реципиента ген, который синтезирует рекомбинантный белок с дополнительной аминокислотной последовательностью, состоящий из гидрофобных аминокислот. Роль гидрофобных аминокислот состоит в том, что они перетаскивают белок в липидную мембрану, в которой с помощью определенных ферментов (сигнальных протеаз), гидрофобная последовательность отщепляется и образуется нужный целевой продукт – это рекомбинантный белок, выходящий в среду.
5. Должна быть возможность сделать клетки микроорганизмов компетентными для того, чтобы их клеточная стенка была бы проницаема для плазмид.
Правила безопасности при работе с рекомбинантными микроорганизмами:
1. Системы выброса оснащаются фильтрами, задерживающими микробные клетки.
2. После завершения процесса производится стерилизация оборудования, но не должно быть разъедания материалов (коррозия), из которых изготовлено оборудование.
3. В ферментере понижается давление на несколько миллиметров ртутного столба.
4. В клетку продуцента вставляется генетический дефект. Дефект заключается в том, что стираются несколько генов путем делеции, то есть избирательно удаляют гены, продуцирующие какую либо аминокислоту или фермент, синтезирующий витамин. Микроорганизм становится более капризным и уязвимым в случае изменения этой среды и соответственно не жизнеспособным. В среде должна быть обязательно для нормального функционирования микроорганизма именно эта аминокислота или витамин, иначе микроорганизм размножаться не будет, и мы не будем иметь целевой продукт.
На первом месте среди белков по значению стоит рекомбинантный инсулин, составляющий около 30% от всего рынка рекомбинантной продукции.
ЗАКЛЮЧЕНИЕ
Рекомбинантный инсулин имеет преимущества перед полученными иным способом препаратами. К таким преимуществам можно отнести идентичность по составу человеческому инсулину (соответственноотсутствуют аллергические реакции), экономичность по сравнению с животным инсулином (1 кг инсулина можно получить в 25 кубовом ферментере, используя кишечную палочку, или необходимо 35 тыс. голов с/х животных.
Многие другие белки синтезируются в организме человека в очень небольших количествах, и единственный способ получать их в масштабах, достаточных для использования в клинике, – технология рекомбинантных ДНК. К таким белкам относятся интерферон и эритропоэтин. Эритропоэтин совместно с миелоидным колониестимулирующим фактором регулирует процесс образования клеток крови у человека. Эритропоэтин используется для лечения анемии, связанной с почечной недостаточностью, и может найти применение как средство, способствующее повышению уровня тромбоцитов, при химиотерапии раковых заболеваний.
СОДЕРЖАНИЕ
Введение……………………………………………………………………………..…….3
1 Биотехнология рекомбинантных белков…………………………………………..…..4 2 Микроорганизмы для производства рекомбинантных белков…..………………..….7 3 Промышленное производство рекомбинантного инсулина……………….…………9 4 Описание технологического процесса производства ……………………………….14
Заключение…………………………………………...…………………………………..16
Список использованных источников…………………………………………………...17
ВВЕДЕНИЕ
Для получения коммерческих продуктов с помощью рекомбинантныхмикроорганизмов необходимо сотрудничество специалистов в двух областях: молекулярных биологов и биотехнологов. Задача молекулярных биологов заключается видентификации, изучении свойств, модификации нужных генов и создании эффективных систем их экспрессии в клетках микроорганизмов, которые можно будет использовать для промышленного синтеза соответствующего продукта, азадача биотехнологов — в обеспечении условийоптимального роста нужного рекомбинантногомикроорганизма с целью получения продукта снаибольшим выходом.
Биотехнология рекомбинантных белков
Для крупномасштабного культивирования рекомбинантных микроорганизмов в промышленных биореакторах (>1000 л) недостаточно просто экстраполировать условия роста в лабораторных ферментерах (0,1—1,0 л). При конструировании промышленных биореакторов необходимо учитывать такие параметры, кактемпература, рН, скорость и характер перемешивания, потребность аэробных организмов в кислороде, количество питательных веществ. Ферментацию можно проводить по-разному. При периодической ферментации посевной материал вводят в свежую культуральную среду и проводят культивирование, не добавляя субстрат до тех пор, пока количество нужного продукта не достигнет максимума. В этих условиях рост культуры проходит шесть этапов: латентную фазу, фазу ускорения, логарифмическую (log) фазу, фазу замедления, стационарную фазу и фазу отмирания. Больше всего белков синтезируется во время логарифмической фазы, а многие низкомолекулярные продукты — во время стационарной. При такомспособе ферментации необходимо тщательно следить за тем, чтобы клетки были собраны в нужноевремя. При периодической ферментации с добавлением субстрата в биореактор добавляют свежуюкультуральную среду через разные интервалы времени, как правило для того, чтобы продлить логарифмическую фазу. Непрерывная ферментация предполагает добавление свежей среды в течениевсего процесса и одновременное удаление клеток и отработанной среды.
Каждая из этих систем ферментации имеет свои недостатки и достоинства, которые нужноучитывать, применяя ее для промышленного синтеза рекомбинантных продуктов. Несмотря на точто непрерывная ферментация применяется в промышленном масштабе не очень широко, этотспособ имеет ряд преимуществ и в будущем, по-видимому, получит большее распространение. Один из подходов к увеличению количества рекомбинантного белкового продукта состоит вмаксимальном увеличении плотности культуры трансформированных клеток, синтезирующихданный продукт. Для достижения этой цели лучше всего использовать режим периодическойферментации с добавлением субстрата. Все биореакторы можно отнести к одному из трех основных типов: реакторы с механическим перемешиванием, барботажные колонны, эрлифтные реакторы. В настоящее время в промышленности чаще всего используются биореакторы первого типа, но появляется интерес и кэрлифтным биореакторам. Механическое перемешивание обеспечивается с помощью механической мешалки, а в эрлифтных биореакторах для аэрации и перемешивания используют газ(обычно воздух), который подается под давлением через разбрызгиватель в дне сосуда. Приэтом во всем объеме происходит непрерывная циркуляция жидкой среды. Барботажные колонны сходны с эрлифтными реакторами, но их недостатком является отсутствие циркуляциикультуральной среды. Для обеспечения стерильности, постоянства рН, температуры и другихпараметров используют разные способы в зависимости от дизайна биореактора. Для синтезарекомбинантных белков применяют двухступенчатые процессы ферментации, осуществляемые в тандемных эрлифтных биореакторах или в одном реакторе с механическим перемешиванием. Если синтезированный продукт накапливается в клетках, то их осаждают из культуральной среды центрифугированием или фильтрацией, затем разрушают ферментативными, химическими или механическими методами и выделяют нужный продукт. Если синтезируемый продукт секретируется в культуральную среду, то процедура его выделения и очистки значительно упрощается (рис. 1).
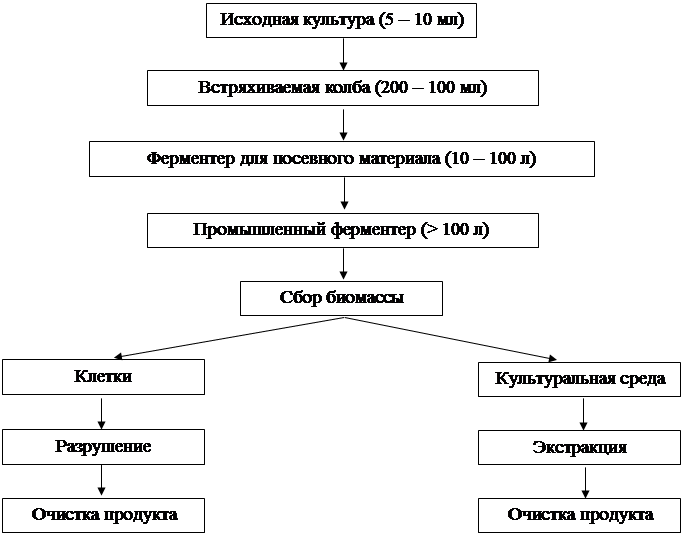
Рисунок 1 – Обобщенная схема процесса промышленной ферментации
