Качественные реакции на обнаружение наполнителей в меде
Аппаратура, материалы, реактивы. Весы лабораторные; водяная баня; электрическая плитка; цилиндры вместимостью на 5, 25, 100 см3; пипетки вместимостью 1 см3; воронки; колбы конические вместимостью 250 см3; фильтры; раствор йода в иодиде калия; ацетат свинца, х.ч.; раствор танина с массовой долей 5%; соляная кислота конц.
Обнаружение муки, крахмала и других порошкообразных веществ. Мед растворяют в трех-пятикратном объеме воды. При наличии примесей они оседают на дно. При добавлении в раствор меда 1-2 капель раствора йода в иодиде калия, он посинеет при наличии в нем муки или крахмала.
Обнаружение свекольной патоки. К 5 см3 раствора меда с массовой долей 20%прибавляют 2,5 г ацетата свинца и 22,5 см3 метилового спирта. Образование желтоватого осадка указывает на фальсификацию меда патокой.
Обнаружение крахмальной патоки. Метод основан на осаждении спиртом крахмальных декстринов. Растворяют 5 г меда в 10 см3 воды, нагревают на водяной бане и добавляют 0,5 см3 раствора таинина с массовой долей 5%, затем взбалтывают и фильтруют.
Для удержания в растворе медовых декстринов в раствор добавляют по 2 капли соляной кислоты (плотностью 1,19 г/см3) на каждый кубический сантиметр исследуемого медового раствора.
Помутнение жидкости от прибавления десятикратного количества этилового спирта указывает на присутствие крахмальной патоки.
РАЗДЕЛ 7. КОНТРОЛЬ ПРАВИЛЬНОСТИ ПРОВЕДЕНИЯ ТЕХНОЛОГИЧЕСКОГО ПРОЦЕССА
ОПРЕДЕЛЕНИЕ ЭФФЕКТИВНОСТИ ТЕПЛОВОЙ ОБРАБОТКИ МЯСНЫХ И РЫБНЫХ КУЛИНАРНЫХ ИЗДЕЛИЙ
Проба на пероксидазу
Метод основан на способности фермента пероксидазы принимать участие в процессах окисления за счет кислорода пероксида водорода. Присутствие пероксидазы устанавливают, используя реакции с гваяколом, бензидином, амидопирином (пирамидоном). При температуре 80°С пероксидаза инактивируется. Следовательно, если в исследуемом изделии пероксидаза обнаруживается, тепловая обработка считается недостаточной.
Аппаратура, материалы, реактивы.Весы лабораторные; пробирки химические диаметром 15мм; пробки корковые; штатив для пробирок; ступка фарфоровая диаметром 7-9 см; капельницы; часы песочные на 1,2 мин; воронки стеклянные диаметром 4-5 см; пипетки вместимостью 1 и20 см3; колбы конические вместимостью 50 и 100 см3; бумагафильтровальная; вата; гваякол, спиртовой раствор с массовой долей 1%(1 г гваякола растворяют этиловым спиртом в мерной колбе на 100 см3); бензидин, спиртовой раствор с массовой долей 0,02% (20мг бензидина растворяют в 100 см5 этилового спирта); амидопирин, спиртовой раствор с массовой долей 2%(2г амидопирина растворяют в 98 см3 этилового спирта); спирт этиловый; пероксид водорода (30-35%), раствор с массовок долей 10%; кислота уксусная ледяная; ацетат натрия безводный; вода дистиллированная.
Проведение испытания. Окислительно-восстановительные свойстве пероксидазы проявляются в строго определенном интервале рН. Наиболее интенсивная окраска наблюдается в интервале значений рН от 4,4 до 6,9; менее интенсивная при рН 3,4 и выше; не проявляется при рН выше 10,4.
При анализе используют ацетатный буферный раствор с рН 4,9.
Измельченную навеску, взятую из внутренней части жареного изделия в количестве 10 г и взвешенную с точностью до 0,01 г, растирают в ступке с 20 см3 дистиллированной воды и фильтруют через бумажный фильтр или слой ваты в коническую колбу. Затем отбирают е пробирку 0,5 см3 фильтрата, добавляют 0,5 см ацетатного буфера, 0,5 см3 спиртового раствора гваякола, 0,25 см3 свежеприготовленного раствора пероксида водорода и встряхивают. При достаточной термической обработке мясного изделия раствор остается бесцветным, при недостаточной, в зависимости от количества сохраненной пероксидазы, окраска может быть от светло-голубой до темно-синей и проявляется в течение 1 мин.
При использовании спиртового раствора бензидина или спиртового раствора амидопирина в пробирку отбирают 1 см3 фильтрата, добавляют 1 см3 одного из указанных растворов, а также 0,5 см3 раствора пероксида водорода и встряхивают. При наличии пероксидазы в течение 1 мин появляется соответственно сине-зеленое или сине-фиолетовое окрашивание. При достаточной тепловой обработке изменения цвета не происходит.
Учитывая, то в мясе больных животных и в несвежем мясе происходит инактивация фермента пероксидазы, для окончательного суждения о качестве тепловой обработки кулинарных изделий необходимо проверить наличие пероксидазы в мясном полуфабрикате. При отсутствии пероксидазы в полуфабрикате достаточность тепловой обработки определяют пробои на фосфатазу.
Проба на фосфатазу
Качественная реакция, метод основан на способности фермента фосфатазы расщеплять бариевую соль паранитрофенилфосфата при температуре 38°С, освобождая паранитрофенол, который окрашивает среду в желтый цвет.
Аппаратура, материалы, реактивы. Весы лабораторные; плитка электрическая; баня водяная; ступка фарфоровая .диаметром 7-9 см; цилиндр вместимостью 1 см3; воронка делительная вместимостью 250 см3; пробки корковые; капельница; воронки стеклянные диаметром 4-5 см; марля; бумага фильтровальная; вата стеклянная; бариевая соль паранитрофенилфосфата, насыщенный раствор; гидроксид натрия, раствор массовой концентрации 400 г/дм3(Д = 1,43 г/см3); хлорид магния, раствор массовой концентрации 5 г/дм3; ацетатный буфер рН 5,4; вода дистиллированная.
Проведение испытания. Измельченную навеску, взятую из внутренней части изделия в количестве 20 г и взвешенную с точностью до 0,01 г, переносят в ступку и растирают, добавляя постепенно 50 см3 дистиллированной воды. Полученную взвесь процеживают через двойной слой марли, а оставшуюся в марле навеску отжимают, затем вытяжку фильтруют через сухой складчатый фильтр и делят пополам. Одну часть (фильтрат 1) исследуют непосредственно, другую ( фильтрат 2 ) переносят в коническую колбу, доводят до кипения и снова фильтруют - эта честь фильтрата является контрольной.
Для проверки активности фосфатазы в пробирку отмеривают 1 см3 фильтрата 1, прибавляют 2 капли раствора хлорида магния массовой концентрации 5 г/дм3, 2 капли ацетатного буфера (рН 5,4) и 0,5 см3 раствора бариевой соли паранитрофенилфосфата.
Для контроля во вторую пробирку отмеривают 1 см3 фильтрата 2 и добавляют те же реактивы, что ж в первую. Обе пробирки помещают на 1 ч в водяную баню или термостат при температуре 37-38°С. Затем в обе пробирки добавляют по капле раствора гидроксида натра.
При достаточной тепловой обработке кулинарного изделия окраска в обеих пробирках не меняется. При недостаточной тепловой обработке раствор желтеет.
Определение остаточной активности кислой фосфатазы (количественное определение). Метод основан на фотометрическом определении в продукте интенсивности развивающейся окраски, зависящей от остаточной активности кислой фосфатазы, выраженной массовой долей фенола.
Аппаратура, материалы, реактивы. Весы лабораторные; потенциометр с погрешностью измерения ±0,06 рН; фотоэлектроколориметр или спектрофотометр для измерения в видимой области спектра; ультратер-мостат или водяная баня; воронки; колбы мерные вместимостью 500 и 1000 см3; пипетки градуированные на 1; 5; 10 см3; палочки стеклянные; пробирки; бумага фильтровальная; груша резиновая; кислота лимонная; цитрат натрия 5-водный; динатриевая соль фенилфосфорной кислоты, раствор массовой концентрации 2 г/дм3, свежеприготовленный; кислота трихлоруксусная, кристаллическая, растворы массовой концентрации 50 и200 г/дм3; гидроксид натрия, раствор С(NаОН) = 0,5 моль/дм3; вода дистиллированная; фенол; толуол; вольфрамат натрия; сульфат лития 1-водный; кислота ортофосфорная плотностью 1,72 г/см3; кислота соляная, плотностью 1,19г/см3; бром.
Подготовка к испытанию. Ацетатный буфер: в мерной колбе вместимостью 1000 см3 в дистиллированной воде растворяют 13,88 г цитрата натрия и 0,588 г лимонной кислоты, доливают водой до метки и перемешивают, рН буфера 6,5. Затем добавляют 1 см3 толуола. Раствор хранят в холодильнике при температуре 4 ± 1°С не более 12 сут.
Реактив Фолина: 100 г вольфрамата натрия и 25 г молибдата натрия растворяют в 700 см3 дистиллированной воды. К раствору добавляют 50 см3 ортофосфорной кислоты и 100 см3 соляной кислоты. Смесь осторожно кипятят в течение 10 ч в колбе вместимостью 2000 см3 с обратным холодильником, после чего охлаждают и добавляют 150 г сульфата лития, 50 см3 воды и несколько капель брома. Остаток брома отгоняют кипячением смеси без холодильника в вытяжном шкафу, охлаждают, переносят в мерную колбу вместимостью 1000 см3, доводят объем дистиллированной водой до метки, перемешивают и фильтруют. Реактив должен быть золотисто-желтого цвета без зеленого оттенка; его хранят в склянке с притертой пробкой в темном месте не более 6 мес.
Стандартный раствор: 2 г фенола (взвешивают с точностью до 0,001г) растворяют в воде в мерной колбе вместимостью 1000 см3, доводят объем до метки и перемешивают. Отбирают пипеткой с помощью резиновой груши 5 см3 раствора в колбу вместимостью 500 см3, добавляют около 300 см3 дистиллированной воды, вносят 25 г кристаллической трихлоруксусной кислоты. После растворения содержимое колбы доводят до метки дистиллированной водой и перемешивают. Полученный раствор содержит 20 мкг фенола в 1 см3.
Построение градуировочного графика. В пробирки вносят следующие объемы стандартного раствора: 0; 0,25; 0,5; 1,0; 1,5; 2,0 см3; что соответствует массе фенола: 0; 5; 10; 20; 30; 40 мкг. Доводят объем каждой пробирки до 2,5 см3, добавляя соответствующий объем раствора трихлоруксусной кислоты массовой концентрации 50 г/дм3 (2,5; 2,25; 2,0; 1,5; 1,0; 0,5 см3) и перемешивают. В каждую пробирку добавляют 5 см3 раствора гидроксида натрия, перемешивают, выдерживают 10 мин, добавляют 1,5 см3 реактива Фолина, разведенного дистиллированной водой в соотношении 1:2 и перемешивают.
Через 30 мин измеряют оптическую плотность растворов по отношению к раствору трихлоруксусной кислоты массовой концентрации 50 г/дм3 на фотоэлектроколориметре с применением светофильтра с длиной волны 600 ± 10 нм в кювете с расстоянием между рабочими гранями 10 мм или спектрофотометра при длине волны 600 нм в кювете аналогичного размера.
По полученным средним данным по трем стандартным растворам на миллиметровой бумаге размером 20×20 см строят градуировочный график. На оси абсцисс откладывают значение массовой доли фенола (микрограмм в 9 см3 окрашенного раствора); на оси ординат – значение соответствующей оптической плотности (Д). Градуировочный график должен проходить через начало координат (рис.5).
Рисунки должны быть выполнены сначала на миллиметровке и затем на кальке.
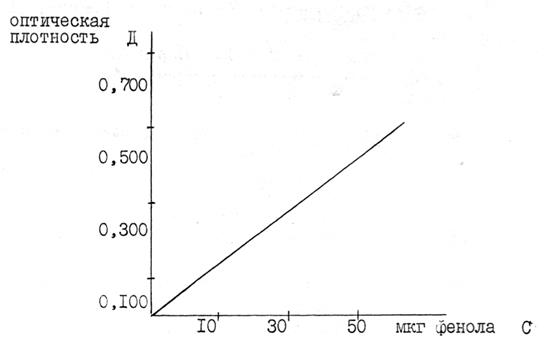
Рис. 5 .Градуировочный график для определения массовой доли фенола с помощью фотоэлектроколориметра (пример)
Проведение испытания. От объединенной пробы, подготовленной к испытанию, берут 2 навески массой по 1 г (с точностью до 0,001 г)и переносят в две пробирки (контрольную и опытную).
В пробирки вносят по 10 см3 ацетатного буфера рН 6,5, тщательно перемешивают стеклянной палочкой и настаивают в течение 20 мин при температуре 20°С, периодически перемешивая.
В контрольную пробирку добавляют 5 см3 200 г/дм3 раствора три-хлоруксуснои кислоты, перемешивают и добавляют 5 см3 2 г/дм3 раствора динатриевой соли фенилфосфорной кислоты, выдерживают 10 мин и фильтруют.
В опытную пробирку добавляют 5 см3 2 г/дм3 раствора динатрие-вой соли фенилфосфорной кислоты и помещают в ультратермостат при температуре 39 ± 1°С на 1 ч, затем добавляют 5 см3 200 г/дм3 раствора трихлоруксусной кислоты, выдерживают 10 мин и фильтруют.
Для проведения цветной реакции из контрольной и опытной пробирок отбирают по 2,5 см3 безбелкового фильтрата. Цветную реакцию проводят по методу, описанному на с. 235.
Массу фенола в навеске определяют по градуировочному графику.
Обработка результатов. Массовую долю фенола (Х,%) вычисляют по формуле
X = 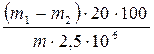 , (100)
, (100)
где m1 - масса фенола в опытной пробирке, найденная по граду-ировочному графику, мкг;
m2 - масса фенола в контрольной пробирке, найденная по градуировочному графику, мкг;
m - масса анализируемой пробы, г;
10 - коэффициент пересчета;
20 - разведение;
2,5 - объем фильтрата, отобранный для цветной реакции,см3.
Вычисление проводят до 0,0001.
За окончательный результат испытания принимают среднее арифметическое результатов двух параллельных определений, допустимое расхождение между которыми при Р = 0,95 не должно превышать 10% по отношению к среднему арифметическому.
Окончательный результат определяют до 0,001.
