Задачи для самостоятельного решения. 1.1. Константа диссоциации масляной кислоты C3H7COOH 1,5∙10–5
1.1. Константа диссоциации масляной кислоты C3H7COOH 1,5∙10–5. Вычислить степень её диссоциации в 0,005 М растворе.
1.2. Найти степени диссоциации в 0,2 н. растворах: а) HClO; б)HF; в)HCN; г)CH3COOH.
1.3. Степень диссоциации муравьиной кислоты HCOOH в 0,2 н. растворе равна 0,03. Определить константу диссоциации кислоты и значение рК.
1.4. Степень диссоциации угольной кислоты H2CO3 по первой ступени в 0,1 н. растворе равна 2,11∙10–3. Вычислить К1.
1.5. При какой концентрации раствора степень диссоциации азотистой кислоты HNO2 будет равна 0,2?
1.6. В 0,1 н. растворе степень диссоциации уксусной кислоты равна 1,32∙10–2. При какой концентрации азотистой кислоты HNO2 ее степень диссоциации будет такой же?
1.7. Сколько воды нужно прибавить к 300 мл 0,2 М раствора уксусной кислоты, чтобы степень диссоциации кислоты удвоилась?
1.8. Чему равна концентрация ионов водорода H+ в водном растворе муравьиной кислоты, если степень диссоциации α = 0,03?
1.9. Вычислить [H+] в 0,02 М растворе сернистой кислоты. Диссоциацией кислоты по второй ступени пренебречь.
1.10. Вычислить [H+], [HSe–] и [Se2–] в 0,05 М растворе H2Se.
1.11. Во сколько раз уменьшится концентрация ионов водорода, если к 1 л 0,005 М раствора уксусной кислоты добавить 0,05 моля ацетата натрия?
1.12. Рассчитать концентрацию ионов CH3COO– в растворе, 1 л которого содержит 1 моль CH3COOH и 0,1 моля HCl, считая диссоциацию последнего полной.
СИЛЬНЫЕ ЭЛЕКТРОЛИТЫ. ВЫЧИСЛЕНИЕ СТЕПЕНИ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ
Примеры решения задач
Пример 1.
Раствор, содержащий 8г NaOH в 1000 г H2O, кипит при 100,184 ºС. Определите изотонический коэффициент (i) (для воды Kэ=0,516 ºС).
Решение:
Второй закон Рауля для растворов электролитов выражается уравнением
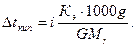 , где g – масса растворенного вещества (г); G - масса растворителя (г); Мr – молекулярная масса растворенного вещества.
, где g – масса растворенного вещества (г); G - масса растворителя (г); Мr – молекулярная масса растворенного вещества.
Молярная масса NaOH равна 40,0. Изотонический коэффициент равен
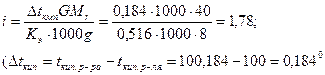
Пример 2. Изотонический коэффициент 0,2 н. раствора нитрата кальция равен 2,48. Вычислите кажущуюся степень диссоциации этого электролита.
Решение:
В случае сильных электролитов кажущуюся степень диссоциации определяют экспериментально, она всегда меньше истинной степени диссоциации, которая близка к единице. Степень диссоциации и изотонический коэффициент электролита связаны между собой соотношением
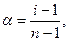
где n- число ионов, образующихся при диссоциации одной молекулы вещества.
При диссоциации Сa(NO3)2 образуется три иона. Кажущаяся степень диссоциации этого электролита равна
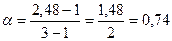 (или 74 %).
(или 74 %).
Пример 3Давление пара водного раствора NaNO3 (ω=8%) равно 2268,8 Па при 20ºС. Давление паров воды при этой температуре равно 2337,8 Па. Найдите кажущуюся степень диссоциации нитрата натрия в этом растворе.
Решение:
С помощью первого закона Рауля для электролитов 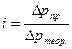 вычисляем значение изотонического коэффициента для NaNO3:
вычисляем значение изотонического коэффициента для NaNO3:
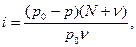 где υ-число молей растворенного вещества; N-число молей растворителя; Р0, Р –давл. паров воды над чистым растворителем и раствором соответственно
где υ-число молей растворенного вещества; N-число молей растворителя; Р0, Р –давл. паров воды над чистым растворителем и раствором соответственно
M (NaNO3) =85,00 г/моль; n= 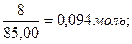
M (H2O)=18,02 г/моль; N= 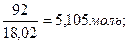
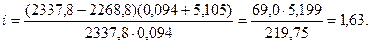
Кажущаяся степень диссоциации NaNO3 в этом растворе равна
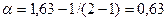 (или 63 %).
(или 63 %).
Пример 4Вычислить осмотическое давление при 270 С раствора сахара С12Н22О11, один литр которого содержит 91 г растворенного вещества.
Решение:
Росм=См∙RT, где См-молярная концентрация, моль/л; R= 8,31 Дж/моль∙К; Т-температура по Кельвину.
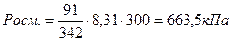
Численное значение R зависит от единиц объема и давления:
Росм кПа; R= 8,31 Дж/моль∙К;
Росм мм Hg ст.; R= 62,32 л∙мм.рт.ст./град. ∙ моль;
Росм. атм.; R= 0,082 л∙атм./град. ∙ моль.
