Ионное произведение воды. Водородный показатель
При изучении этой темы необходимо выучить: что такое ионное произведение воды и водородный показатель, как меняется водородный показатель при изменении среды и как определяют качественную реакцию среды.
Вода является очень слабым электролитом. В ничтожно малой степени молекулы воды диссоциируют на ионы водорода (Н+) и гидроксида (ОН-) :
Н2ОD Н+ + ОН-
Произведение концентраций этих ионов в чистой воде, а также в любом водном растворе, есть величина постоянная, и называется ионное произведение воды.
При температуре 25 0С: [Н+] [ОН-]=10-14.
В чистой воде 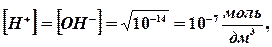
 среда нейтральная.
среда нейтральная.
Для удобства оценки изменения концентрации ионов водорода (а, следовательно, и гидроксид ионов) ввели водородный показатель среды 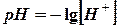 . Тогда, если концентрация ионов водорода больше
. Тогда, если концентрация ионов водорода больше 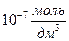 , то рН ‹ 7 – среда кислая; если концентрация ионов водорода меньше
, то рН ‹ 7 – среда кислая; если концентрация ионов водорода меньше 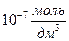 (а концентрация гидроксид ионов больше
(а концентрация гидроксид ионов больше 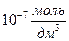 ), то рН › 7 – среда щелочная.
), то рН › 7 – среда щелочная.
Качественную реакцию среды определяют при помощи индикаторов – веществ, окраска которых зависит от величин рН.
Упражнение по теме 3
1. рН раствора равна 4. Что надо прибавить к раствору, чтобы приблизить рН к 7?:
а) кислоту; б) воду; в) щелочь.
2. Концентрация гидроксид ионов в растворе 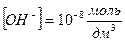 . Чему равно рН среды в этом растворе?
. Чему равно рН среды в этом растворе?
Лабораторная работа 3
Определение реакции среды при помощи индикаторов
К заранее приготовленным растворам кислоты, щелочи и чистой воды добавляют соответствующие индикаторы. По изменению окраски определяют, что за раствор.
Результаты заносят в таблицу.
| Индикатор | Окраска | Интервал перехода, pH | ||
| В кислой среде | В нейтральной среде | В щелочной среде | ||
| Метилоранж | 3,1-4,4 | |||
| Фенолфталеин | 8,2-10,0 | |||
| Универсальная индикаторная бумага | Шкала цветности |
Гидролиз солей
При изучении этой темы необходимо повторить принцип смещения химического равновесия при внешнем воздействии (Ле Шателье-Брауна). Разобраться с физическим смыслом гидролиза солей. Научиться составлять уравнения реакций гидролиза различных солей.
Молекулы воды в ничтожно малой степени диссоциируют на катионы водорода и гидроксид – ионы:
Н2О D Н+ + ОН-
При растворении соли в воде это равновесие может нарушаться. Куда при этом сместится равновесие можно определить, пользуясь принципом Ле Шателье – Брауна: если на равновесие оказывается внешнее воздействие, то равновесие смещается в сторону той реакции, которая противодействует этому внешнему воздействию.
Растворим в воде соль, образованную сильным основанием (например, NaOH) и слабой кислотой (например, CH3COOH). Соль – сильный электролит, поэтому все молекулы ацетата натрия (CH3COONa) распадутся на ионы. Но ионы CH3COO- будут связывать ионы Н+ в молекулы CH3COOH, так как эта кислота слабая и предпочитает в воде находиться в виде молекул. Концентрация ионов Н+ в воде уменьшится, поэтому равновесие в диссоциации Н2О на ионы сместится в сторону той реакции, которая увеличит концентрацию ионов Н+, т.е. прямой реакции. Но ионы Н+ будут связываться ионами СН3СОО-, поэтому в воде будут накапливаться ионы ОН- . Среда будет щелочной, рН › 7.
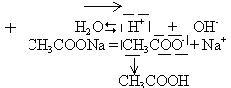
__
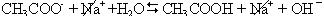
CH3COO- + H2O D CH3COOH + OH-
Т.е., если в воде появились анионы слабой кислоты, то в воде накапливаются гидроксид – ионы. Среда щелочная.
Растворим в воде соль, образованную слабым основанием (например, NH4OH) и сильной кислотой (например, HCl). Все молекулы хлорида аммония (NH4Cl) распадутся на ионы. Теперь ионы ОН - будут связываться ионами NH4+ в молекулы NH4OH. Для компенсации уменьшившейся концентрации ионов ОН - равновесие опять сместится в сторону прямой
реакции. Но теперь будут накапливаться в растворе ионы Н+. Среда будет кислой, рН ‹ 7.
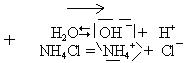
↓
NH4OH
___________________________
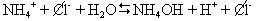
NH4+ + H2O D NH4OH + H+
Т.е., если в воде появились катионы слабого основания, то в воде накапливаются ионы водорода. Среда кислая.
Растворим в воде соль образованную слабой кислотой и слабым основанием, например ацетат аммония (CH3COONH4). Все молекулы CH3COONH4 распадутся на ионы. Но теперь и ионы Н+ и ионы ОН- будут связываться в молекулы. Равновесие опять будет смещаться в сторону прямой реакции, но соотношение концентрации ионов Н+ и ОН- практически не будет изменяться. Среда будет близкой к нейтральной, рН ≈ 7.
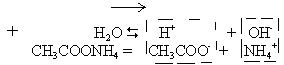
↓ ↓
CH3COOH NH4OH
________
CH3COO- + NH4+ + H2O D CH3COOH + NH4OH
Т.е., если в воде появились катионы слабого основания и анионы слабой кислоты, то гидролиз идет, но соотношение концентрации Н+ и ОН- практически не меняется. Среда близкая к нейтральной.
Теперь растворим соль, образованную сильной кислотой и сильным основанием, например, хлорид натрия (NaCl). Все молекулы NaCl распадутся на ионы. Но теперь ионы Н+ и ОН- не будут связываться в молекулы, т.к. и NaOH, и HCl – сильные электролиты и предпочитают находиться в растворе в виде ионов. Равновесие не нарушается. Гидролиз соли отсутствует. Среда нейтральная, рН=7.
Примеры продуктов гидролиза различных солей представлены в таблице.
Таблица
| Характер соли | Примеры соли | Продукты гидролиза | Реакция среды |
| Соль образована сильным основанием и слабой кислотой | а) анион однозарядный: KCN, CH3COONa | Щелочь и слабая кислота | рН›7 |
| б) анион многозарядный: K2S, Na3PO4 | Щёлочь и кислая соль | рН›7 | |
| Соль образована сильной кислотой и слабым основанием | а) катион однозарядный: NH4Cl, AgNO3 | Кислота и слабое основание | рН‹7 |
| б) катион многозарядный: Pb(NO3)2, CrCl3 | Кислота и основная соль | рН‹7 |
Примеры составления уравнений гидролиза солей:
K2S + H2ODKHS + KOH
S2- + H2ODHS- + OH- рН›7
AlCl3 + H2ODAlOHCl2 + HCl
Al3+ + H2ODAlOH2+ + H+ рН‹7
Упражнение по теме 4
1. Какая из приведенных солей при растворении в воде не подвергается гидролизу:
а) K2S; б) NaNO3; в) CrCl3.
2. Какая реакция среды будет при растворении в воде соли Fe (NO3)3:
а) кислая; б) нейтральная; в) щелочная.
3. Какая из приведенных солей при гидролизе образует кислую соль:
а) ZnSO4; б) Na3PO4; в) NH4Cl.
4. Составьте молекулярные и ионные уравнения реакций гидролиза солей: K2SO3; Сu(NO3)2.
Лабораторная работа 4
