Определение содержания компонентов в смеси веществ
Имеется смесь карбоната и гидрокарбоната натрия массой 180 г. При прокаливании этой смеси выделилось 8,1 г воды. Определите массу и массовую долю карбоната натрия в исходной смеси.
Дано: m(смеси) =180г m(H2O)= 8,1г
Найти: m(Na2CO3)=? ω(Na2CO3) =?
М(NaHCO3)=84 г/моль
М(Н2О)=18 г/моль
Решение.
1. Так как смесь содержит 2 компонента, составим 2 уравнения реакции термического разложения солей
Na2CO3≠ (1)
X 0,45моль
2NaHCO3= Na2CO3 + H2O +CO2 ↑ (2)
2моль 1моль
2. Определим количество вещества воды
ν(H2O)= 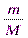 =
= 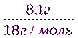 = 0,45 моль
= 0,45 моль
3. Определим по уравнению реакции количество вещества и массу гидрокарбоната натрия – одного из компонентов смеси.
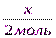 =
= 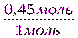 ; x= 0,9 моль
; x= 0,9 моль
m(NaHCO3)= ν·M=0,9моль · 84г/моль=
= 75,6 г
4. По разности определим массу второго компонента смеси
m(Na2CO3) = m(смеси) – m(NaHCO3) =
= 180г – 75,6г = 104,4г
5. Рассчитаем массовую долю карбоната натрия в исходной смеси
ω(Na2CO3)= 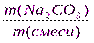 =
= 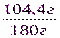 =
= 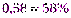
Ответ: ω(Na2CO3) = 58%
Расчет по уравнениям последовательно протекающих реакций
К 200 г раствора сульфата меди (II) с массовой долей CuSO4 4% прилили гидроксид калия до полного осаждения синего осадка. Осадок прокалили. Над образовавшимся черным порошком пропустили (при нагревании) газообразный аммиак. Рассчитайте массу образовавшегося при этом красного вещества с металлическим блеском.
Дано: m(раствора)= 200г ω(CuSO4) = 4%
Найти: m(продукта) =?
М(CuSO4)=160г/моль
Решение.
1.Составим уравнения протекающих
реакций в соответствии с условием задачи
0,05моль X
CuSO4 + 2KOH = Cu(OH)2↓ + K2SO4 (1)
1моль 1моль
0,05моль Y
Cu(OH)2 = CuO + H2O (2)
1моль 1моль
0,05моль Z
3CuO +2NH3 = 3Cu + N + 3H2O (3)
3моль 3моль
2. Определим массу CuSO4 в растворе и его количество вещества
m (CuSO4)= ω·m(раствора)= 0,04·200г=8 г
ν(CuSO4)= 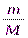 =
= 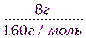 =
= 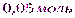
3. По уравнению (1) находим количество
вещества Cu(OH)2 :
ν(Cu(OH)2)= 0,05моль
4. По уравнению (2) находим количество
вещества CuO (черный порошок, полученный после прокаливания):
Y = ν(CuO) = 0,05 моль
5. По уравнению (3) определяем количество вещества и массу образовав-
шегося красного металла – меди.
Z= ν(Cu)= 0,05 моль
m(Cu)= ν·M= 0,05 моль· 64г/моль= 3,2г
Ответ: m(Cu)= 3,2 г
СОСТАВЛЕНИЕ УРАВНЕНИЙ РЕАКЦИЙ ПО СХЕМЕ ПРЕВРАЩЕНИЙ
ЗАДАНИЕ № 1.
Составьте уравнения реакций, соответствующие следующей схеме. Назовите продукты реакции:
- Pb(NO3)2à NO2à HNO3à NH4NO3à N2O
- S i à Mg2S i à SiH4à SiO2à Na2SiO3
- KClO3à O2à P2O5à HPO3à Ca(PO3)2
- Al2S3à H2S à HCl à Cl2à NaClO
ЗАДАНИЕ № 2.
Подберите вещества, соответствующие буквам в цепочках превращений, запишите уравнения реакций. Назовите продукты реакций. Укажите тип химической реакции.
+ C + CuO + NaOH +CO2 + NaOH
1. CO2à A à B à C à D à E
to + NO + NaOH
2. NaNO3 à Xгаз à Y à Z
