Контроль диазотирования
При диазотировании тщательно контролируют избыток азотистой кислоты и, как только будет обнаружено, что она присутствует в растворе и больше уже не расходуется, приливание водного раствора нитрита прекращают.
Наиболее совершенным способом определения содержания свободной азотистой кислоты в реакционной массе в лабораторных условиях и на производстве является измерение окислительно-восстановительного потенциала системы с помощью платинового индикаторного электрода в паре с каломельным или хлорсеребряным электродом сравнения.
Более простой способ контроля – проба по йодкрахмальной бумажке, которая представляет собой полоску фильтровальной бумаги, пропитанную йодистым калием и водорастворимым крахмалом. Если в растворе присутствует свободная азотистая кислота, она окисляет иодид калия, и выделяющийся молекулярный йод, взаимодействуя с крахмалом, окрашивает индикаторную бумагу в синий цвет:
2 KI + 2 HNO2 + H2SO4 = I2 + K2SO4 + 2 H2O + 2 NO
Реакция диазотирования проходит сравнительно медленно, поэтому пробу на присутствие избытка азотистой кислоты следует делать не тотчас же после прибавления последней порции нитрита, а спустя 5 – 10 мин после этого.
Если после диазотирования в реакционном растворе остается небольшой избыток азотистой кислоты, его уничтожают, вводя в раствор вещества, легко реагирующие с НNО2. Обычно используют мочевину (H2N-CO-NH2) или сульфаминовую кислоту (H2N-SO3H):
H2N-CO-NH2 + 2 HNO2 = 2 N2 + CO2 + 3 H2O
H2N-SO3H + HNO2 = H2SO4 + N2 + H2O
В процессе диазотирования необходимо проверять наличие минеральной кислоты в реакционной массе по индикаторной бумажке.
Как правило, соли диазония с такими анионами как Сl-, НSО4-, Вr- и т.п. в свободном виде не выделяют, так как в сухом виде они являются взрывчатыми веществами (во влажном состоянии не опасны). Гораздо большей термической устойчивостью обладают тетрафторбораты диазония [ArN2]+[BF4]-. Они могут быть получены в сухом состоянии и храниться продолжительное время. Значительной устойчивостью обладают также двойные соли диазония и ряда металлов. Например, практическое значение имеют двойные соли диазония с хлористым цинком ArN2+·ZnCl3-, которые могут быть выделены в сухом состоянии. Диазосоединения иногда выделяют из реакционных смесей в виде их устойчивых форм – диазотатов Ar-N=N-ONa.
Формы диазосоединений
При добавлении щелочи к раствору соли диазония гидроксильный ион связывается с крайним атомом азота и образуется диазогидрат, обладающий слабыми кислотными свойствами. Диазогидрат нейтрализует еще один гидроксильный ион, превращаясь в диазотат:
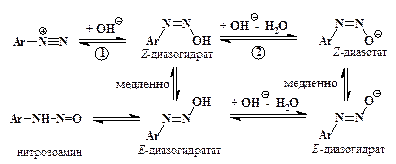
Константы равновесия реакций (1, 2) почти одинаковы и обычно имеют величину 10-9 ¸ 10-10 л/моль. Поэтому диазогидрат ни при каких условиях не бывает доминирующей формой. В кислых растворах диазосоединения существуют в основном в виде катионов диазония, в щелочных при рН > 10 – в форме диазотат-анионов. Максимальная доля диазогидрата (≤ 25 %) достигается в интервале рН от 9 до 10.
Если только что полученный раствор диазотата снова подкислить, то он быстро превратится в исходную соль диазония. Однако, когда этот раствор постоит или если его нагреть со щелочью, то диазотат превращается в более стабильную форму, которая при подкислении лишь очень медленно переходит в соль диазония. Это явление объясняется тем, что образующийся вначале анион диазотата имеет Z-конфигурацию, а более стабильный продукт его изомеризации представляет собой E-изомер. (обозначения Z и E рекомендованы ИЮПАК вместо устаревших цис-транс- и син-анти-).
Обратное превращение Е-изомера в Z- осуществляется лишь в специальных условиях при действии ультрафиолетового света. Превращение Е-диазотата в соль диазония при подкислении проходит через стадию образования нитрозоамина Ar-NH-NO.
Е-диазотаты – стабильные соединения, не способные вступать в реакцию азосочетания. Они используются в технике как удобный для хранения и транспортировки источник получения солей диазония.
Превращения диазосоединений
Азосочетание
Реакция азосочетания приводит к образованию азокрасителей – очень важного класса соединений. В лабораторной практике часто восстановлением азокрасителей получают окси-амино- и диаминосоединения. Таким образом, здесь азокраситель выступает в качестве промежуточного продукта.
Из всех приведенных выше форм диазосоединений единственной, способной вступать в реакцию азосочетания, является катион диазония.
Азосочетание является типичной реакцией электрофильного замещения. Те соединения, у которых возможно замещение атома водорода, связанного с углеродным атомом, на группу -N=N-Аr, называются азосоставляющими. Первичные ароматические амины, из которых получают соли диазония, принято называть диазосоставляющими.
В тех условиях, в которых обычно проводится реакция азосочетания (водная среда, низкая температура) катионы диазония являются слабыми электрофилами. Они могут вступать в реакцию только с такими ароматическими соединениями, которые содержат в ароматическом ядре наиболее сильные электронодонорные заместители, такие как -ОН, -NН2, -NНR, -NR2, где R - алкил. Реакции азосочетания могут быть записаны в виде следующих схем:

Азосочетание с аминами проводят в слабокислой среде, а с фенолами – в слабощелочной. В последнем случае образуются фенолят-ионы, которые являются гораздо более активными азосоставляющими, чем сами фенолы. Скорости сочетания фенолятов с катионом диазония в 1010 - 1012 раз больше, чем исходных неионизированных фенолов.
В реакцию азосочетания вступают свободные амины, а не их соли. В сильнокислой среде большая часть амина находится в инертной форме Ar-NH3+. В сильнощелочных растворах катион диазония превращается в диазотат-ион, и это также уменьшает скорость реакции. На рис. 23 схематически показан характер изменения скоростей азосочетания с аминами и фенолами при увеличении рН.
