Пятичленный ароматический гетероцикл с одним гетероатомом

Пиррол – бесцветная жидкость с приятным запахом. Температура кипения пиррола (130-1310С) значительно превышает температуры кипения фурана (320С) и тиофена (840С), что обусловлено его ассоциацией за счет образования водородных связей.

Пиррол может быть отнесён к ароматическим соединениям, так как его молекулы содержат циклическую сопряженную систему, включающую 6 p-электронов.
Кислотные свойства пиррола
Пиррол является слабой NH-кислотой (рКа=17,5). По кислотности он превосходит амины и близок к спиртам. Соли пиррола получают взаимодействием пиррола с металлами, амидами металлов, металлоорганическим соединениями.
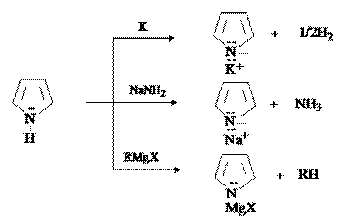

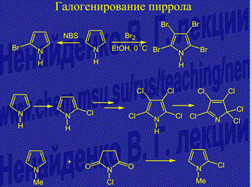
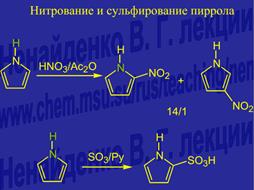
57 Шестичленные ароматические гетероциклы: пиридин, пиримидин. Доказательство ароматичности. SЕ-реакции пиридина. Сульфирование, нитрование, алкилирование


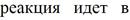
Это соединение является основой пиримидиновых оснований, входящих в состав природных высокомолекулярных веществ - нуклеиновых кислот.
Алкилирование. При взаимодействии с алкирирующими агентами – алкилгалогенидами или алкилсульфатами – атом азота проявляет нуклеофильные свойства и образует ковалентную связь с электрофильным атомом углерода реагента. Получаемые при этом N-алкилпиридиниевые соли сохраняют ароматический характер, так как в результате реакции ароматический секстет электронов не нарушается.
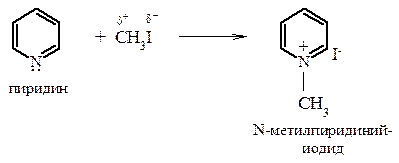
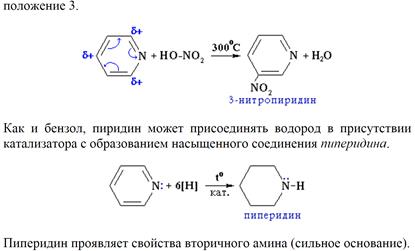
Нитрование. Пиридин нитрируется в ядро в очень жестких условиях. Классический вариант проведения реакции с использованием «нитрирующей смеси» приводит к образованию 3-нитропиридина с выходом более 6% (при температуре 3000С). Несколько лучшие результаты дает замена азотной кислоты на нитрат калия:
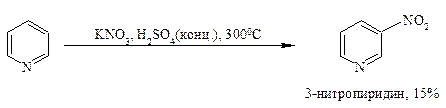
При наличии алкильных заместителей нитрование облегчается, но необходимо присутствие в ядре не менее двух алкильных групп, чтобы окисление боковых цепей не составляло конкуренцию реакции нитрования. Так, сим-коллидин нитруется с высоким выходом в значительно более мягких условиях:
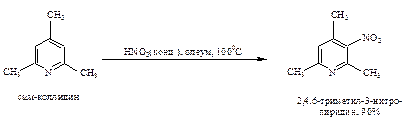
Сульфирование. Пиридин очень устойчив к действию концентрированной серной кислоты и олеума. Даже длительное нагревание при температуре 3200С приводит к образованию пиридин-3-сульфоновой кислоты с очень низким выходом. Сульфирование протекает значительно легче в присутствии каталитических количеств солей ртути (II) или хлорида алюминия. Роль катализатора точно не установлена.
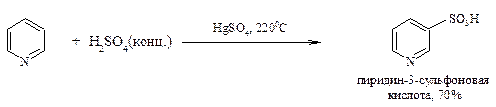
58 SN-реакции пиридина. Гидроксилирование, алкилирование реактивами Гриньяра. Кислотно-основные свойства пиридина
По способности вступать в реакции нуклеофильного замещения в ядре пиридин и его производные резко отличаются от соединений бензольного ряда. В общем виде реакцию можно представить следующим образом:
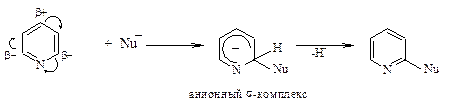 При определенном сходстве в механизмах электрофильного и нуклеофильного замещения водорода в ароматических системах следует отметить принципиальную разницу в этих реакциях. Если при электрофильном замещении водород отщепляется на последней стадии достаточно легко в виде протона, то при нуклеофильном замещении реакция завершается удалением гидрид-иона. Этот этап труднее осуществим и часто требует присутствия окислителя, который играет роль акцептора гидрид-иона.
При определенном сходстве в механизмах электрофильного и нуклеофильного замещения водорода в ароматических системах следует отметить принципиальную разницу в этих реакциях. Если при электрофильном замещении водород отщепляется на последней стадии достаточно легко в виде протона, то при нуклеофильном замещении реакция завершается удалением гидрид-иона. Этот этап труднее осуществим и часто требует присутствия окислителя, который играет роль акцептора гидрид-иона.
К реакции нуклеофильного замещения относятся реакции аминирования, гидроксилирования и алкилирования (арилирования), т.е. непосредственного введения нуклеофильных групп в кольцо пиридина или его гомологов.
Гидроксилирование. Пиридин склонен вступать в еще одну реакцию, не свойственную бензолу, - прямого введения гидроксильной группы в ядро. Реакция протекает в очень жестких условиях и с низким выходом продукта, поскольку нуклеофильность гидроксид-иона ниже, чем амид-иона.
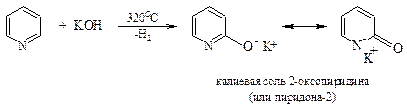
Алкилирование и арилирование. Такие сильные нуклеофильные реагенты, как литийорганические соединения, легко присоединяются к пиридину, образуя соли 1,2-дигидропиридина, которые иногда даже могут быть выделены в индивидуальном состоянии. Возврат к ароматической системе путем отщепления гидрид-иона достигается термически или действием окислителя.
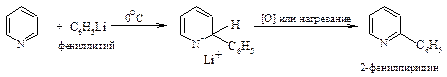
Основные свойства
Неподеленная пара электронов атома азота в пиридине находится на sp2 – гибридной орбитали и не участвует в сопряжении, поэтому пиридин проявляет основные свойства и с сильными кислотами образует кристаллические пиридиниевые соли.
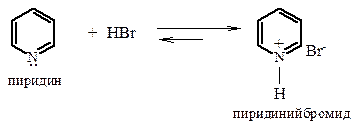
Соли пиридиния сохраняют ароматический характер, так как протонирование осуществляется за счет неподеленной пары электронов, не участвующих в образовании ароматического секстета.
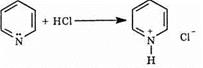
Пиридин является основанием и при взаимодействии с сильными кислотами образует соль.
Высокомолекулярные соединения (ВМС), полимеры. Классификация ВМС по происхождению. Отдельные представители (полиэтилен, полипропилен, поливинилхлорид, полистирол, натуральные и синтетические каучуки, тефлон, лавсан, капрон, полиметилметакрилат, крахмал, целлюлоза, полипептиды).


По происхождению высокомолекулярные соединения подразделяют на:
1. Природные (натуральные или естественные). Характерными представителями таких соединений являются природные белки, натуральный каучук, шелк, шерсть и др.
2. Искусственные, получаемые путем химической обработки натуральных высокомолекулярных соединений. К числу таких материалов относятся: нитроцеллюлоза (используемая для получения целлулоида и этрола), ксантогенат целлюлозы (вискоза), ацетат целлюлозы.
3. Синтетические, представляющие собой продукты процессов полимеризации или поликонденсации низкомолекулярных соединений. К этому наиболее важнейшему классу высокомолекулярных соединений относятся полиэтилен, поливинилхлорид, полиамиды, полистиролы, феноло-формальдегидные смолы, полиуретаны и многие другие соединения.
Полиэтиле́н — термопластичный полимер этилена, относится к классу полиолефинов. Является органическим соединением и имеет длинные молекулы …—CH2—CH2—CH2—CH2—…, где «—» обозначает ковалентные связи между атомами углерода. Самая распространённая в мире пластмасса.
Представляет собой массу белого цвета (тонкие листы прозрачны и бесцветны). Химически- и морозостоек, диэлектрик, не чувствителен к удару (амортизатор), при нагревании размягчается (80—120°С),адгезия (прилипание) — чрезвычайно низкая. Иногда в народном сознании отождествляется с целлофаном
Для полиэтилена сырьем является газ этилен. Путем полимеризации этилена при низких и высоких давлениях, получается полиэтилен. Зачастую полиэтилен производится в виде гранул (ø 2-5 мм.), реже - в виде порошка.
Полипропилен (ПП) — это термопластичный полимер пропилена (пропена).
Полипропилен получают полимеризацией пропилена в присутствии металлокомплексных катализаторов, например, катализаторов Циглера—Натта (например, смесь TiCl4 и AlR3):
nCH2=CH(CH3) → [-CH2-CH(CH3)-]n
Параметры, необходимые для получения полипропилена близки к тем, при которых получают полиэтилен низкого давления. При этом, в зависимости от конкретного катализатора, может получаться любой тип полимера или их смеси.
Полипропилен выпускается в виде порошка белого цвета или гранул с насыпной плотностью 0,4—0,5 г/см³. Полипропилен выпускается стабилизированным, окрашенным и неокрашенным.
Поливинилхлорид (ПВХ, полихлорвинил, винил, вестолит, хосталит, виннол, корвик, сикрон, джеон, ниппеон, сумилит, луковил, хелвик, норвик и др.) — бесцветная, прозрачная пластмасса, термопластичный полимер винилхлорида. Отличается химической стойкостью к щелочам, минеральным маслам, многим кислотам и растворителям. Не горит на воздухе и обладает малой морозостойкостью (−15 °C). Нагревостойкость: +65 °C.
Химическая формула: [-CH2-CHCl-]n.Международное обозначение — PVC.
Получается суспензионной или эмульсионной полимеризацией винилхлорида, а также полимеризацией в массе.
Полистирол (ПС) — cинтетический полимер класса термопластов, продукт полимеризациистирола(винилбензола); твердое стеклообразное вещество.
Имеет химическую формулу вида: [-СН2-СН(С6Н5)-]n—
Промышленное производство полистирола основано на радикальной полимеризации стирола. Различают 3 основных способа его получения:
- Эмульсионный (ПСЭ); - Суспензионный (ПСС);
- Блочный или получаемый в массе (ПСМ).
Полиэтиле́нтерефтала́т (ПЭТФ, ПЭТ, лавсан) — термопластик, наиболее распространённый представитель класса полиэфиров, известен под разными фирменными названиями. Продукт поликонденсации этиленгликоля с терефталевой кислотой; твёрдое, бесцветное, прозрачное вещество в аморфном состоянии и белое, непрозрачное в кристаллическом состоянии. Переходит в прозрачное состояние при нагреве до температуры стеклования и остаётся в нём при резком охлаждении и быстром проходе через т. н. «зону кристаллизации». Одним из важных параметров ПЭТ является характеристическая вязкость определяемая длиной молекулы полимера. С увеличением присущей вязкости скорость кристаллизации снижается. Прочен, износостоек, хороший диэлектрик.
Капрон (поли-ε-капроамид, найлон-6, полиамид 6)— синтетическое полиамидное волокно, получаемое из нефти, продукт полимеризации капролактама. Формула полимера имеет вид:[—HN(CH2)5CO—]n
