Способы выражения состава растворов
Общая характеристика растворов. Растворённое вещество, растворитель. Массовая доля, молярность, молярная концентрация эквивалента (нормальность), моляльность, мольная доля. Физическая и химическая теории растворов. Сольватация, гидратация. Растворимость газов, жидкостей и твёрдых веществ в воде. Ненасыщенные, насыщенные и пересыщенные растворы
1. С повышением температуры растворимость твёрдых веществ … .
1) как правило, уменьшается 2) уменьшается
3) не изменяется 4) как правило, увеличивается
2. При повышении температуры растворимость газообразных веществ … .
1) увеличивается 2) уменьшается
3) не изменяется 4) становится неограниченной
3. При повышении давления растворимость газообразных веществ … .
1) уменьшается 2) увеличивается
3) не изменяется 4) становится неограниченной
4. В равновесии с кристаллами растворяемого вещества находится … раствор.
1) ненасыщенный 2) насыщенный
3) сильно разбавленный 4) пересыщенный
5. Массовую долю растворённого вещества можно рассчитать по формуле … .
1) 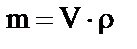 2)
2) 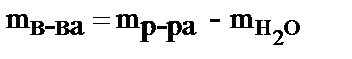
3) 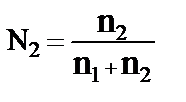 4)
4) 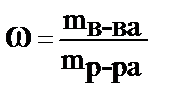
6. Выражение "раствор с массовой долей 6 %" означает, что в ... .
1) 100 г воды растворено 6 г вещества
2) 100 мл раствора содержится 6 г растворённого вещества
3) 100 г раствора содержится 6 г растворённого вещества
4) 106 г раствора содержится 6 г растворённого вещества
7. Для приготовления 10 %-ного (по массе) водного раствора гидроксида натрия надо взять … .
1) 100 г воды и 10 г едкого натра 2) 110 г воды и 10 г NaOH
3) 90 г воды и 10 г едкого натра 4) 100 мл воды и 10 г NaOH
8. Единица измерения молярной концентрации – … .
1) г/моль 2) моль/л 3) % 4) моль/кг
9. В 1 л децимолярного раствора содержится … моль растворённого вещества.
1) 0,2 2) 1,0 3) 0,1 4) 0,01
10. В 1 л сантимолярного раствора содержится … моль растворённого вещества.
1) 100 2) 1,0 3) 0,01 4) 0,1
11. Мольную долю растворённого вещества можно рассчитать по формуле … .
1) 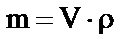 2)
2) 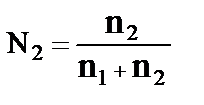
3) 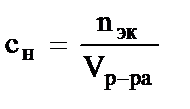 4)
4) 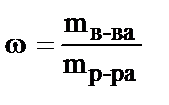
12. Молярную концентрацию эквивалента (нормальность) раствора можно рассчитать по формуле … .
1) 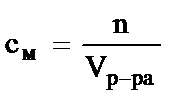 2)
2) 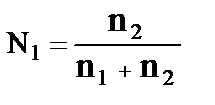
3) 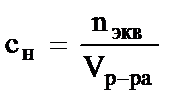 4)
4) 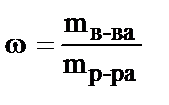
13. Эквивалентная (или нормальная) и молярная концентрации раствора … равны.
1) СаСl2 2) ZnSО4 3) Н2SО4 4) КNО3
14. В одном литре 1 н. раствора хлороводородной (соляной) кислоты содержится … г НСl.
1) 365 2) 36,5 3) 3,65 4) 0,365
15. Массовая доля ацетата натрия в растворе, полученном при растворении 40 г СН3СООNа в 200 г воды, равна … %.
1) 8,34 2) 16,67 3) 10,0 4) 20,0
16. Если растворимость нитрата калия при 20 0С равна 34,1 г в 100 г воды, то его массовая доля в насыщенном растворе при этой температуре составляет … %.
1) 12,5 2) 25,4 3) 37,5 4) 50,5
17. Масса растворённого вещества в 500 мл 25 %-ного раствора ортофосфорной кислоты (ρ = 1,2 г/мл) равна … г.
1) 100 2) 150 3) 104 4) 250
18. Для приготовления 500 г 10 %-ного раствора сульфата калия необходимую навеску соли следует растворить в … г воды.
1) 475 2) 450 3) 400 4) 50
19. Масса соли, необходимая для приготовления 200 мл 10 %-ного раствора хлорида натрия (ρ = 1,1 г/мл) равна … г.
1) 22 2) 20 3) 44 4) 40
20. Для приготовления 10 %-ного (по массе) раствора в 50 г воды необходимо растворить … г щёлочи.
1) 5,56 2) 10,0 3) 6,25 4) 12,5
21. Масса кристаллогидрата СаСl2 · 6Н2О, требуемая для приготовления 355 г 2,5 %-ного (по массе) раствора хлорида кальция, равна … г.
1) 0,08 2) 8,88 3) 17,51 4) 35,00
22. В 50 г 3,65 %-ного раствора НСl растворено … молекул хлороводорода.
1) 1,75 · 1023 2) 3,01 · 1023 3) 3,01 · 1024 4) 3,01 · 1022
23. В 50 г 10 %-ного раствора NаСl содержится … молекул воды.
1) 6,02 · 1024 2) 3,01 · 1024 3) 3,01 · 1023 4) 1,505 · 1024
24. Если при упаривании 20 кг 5 %-ного (по массе) раствора некоторой соли его масса уменьшилась на 4 кг, то массовая доля этой соли в полученном растворе будет равна … %.
1) 1,25 2) 4,20 3) 6,25 4) 20,8
25. Массовая доля соли в растворе, полученном при смешении 150 г
2 %-ного и 350 г 4 %-ного растворов, составляет … %.
1) 6,8 2) 1,7 3) 3,4 4) 3
26. Если смешать 0,5 л 10 %-ного (ρ = 1,11 г/мл) и 2 л 20 %-ного
(ρ = 1,22 г/мл) растворов NаОН, то массовая доля гидроксида натрия в полученном растворе будет равна … %.
1) 1,2 2) 15,6 3) 18,1 4) 52,8
27. Если к 400 г 18 %-ного (по массе) раствора гидроксида калия добавить 100 г раствора, содержащего 0,5 моль КОН, то массовая доля растворённого вещества в полученном растворе будет равна … %.
1) 20 2) 25 3) 30 4) 40
28. Масса воды, которую надо добавить к 400 г 15 %-ного (по массе) раствора некоторой соли для получения её 5 %-ного раствора, равна … г.
1) 100 2) 200 3) 400 4) 800
29. Масса 25 %-ного (по массе) раствора некоторой соли, необходимая для приготовления 600 г её 10 %-ного раствора, равна … г.
1) 15 2) 60 3) 240 4) 400
30. Молярная концентрация раствора, в 2 л которого содержится 19,6 г серной кислоты, равна … моль/л.
1) 0,2 2) 0,5 3) 1,0 4) 0,1
31. Масса соли, необходимая для приготовления 2 л 0,2 М раствора сульфата магния равна … г.
1) 72 2) 48 3) 96 4) 24
32. В 400 мл 0,5 М раствора нитрата натрия содержится … г соли.
1) 17 2) 34 3) 68 4) 85
33. Объём 36 %-ного раствора НСl (ρ = 1,18 г/мл), необходимый для приготовления 500 мл 0,1 М раствора, равен … мл.
1) 86 2) 4,3 3) 8,6 4) 43
