Число частиц, подвергшихся первичному фотохимическому превращению равно числу поглощенных ими квантов света
Для суждения о том, применим ли к данной фотохимической реакции закон эквивалентности Эйнштейна, пользуются понятием о квантовом выходе реакции:
Квантовым выходом γ называется отношение числа N частиц, претерпевших химическое превращение, к числу поглощенных квантов:
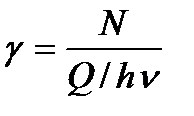
Q- энергия поглощенного излучения.
Квантовый выход не для всех фотохимических реакций равен единице. Он может быть больше или меньше единицы.
Значение больше единицы объясняется тем, что вслед за собственно фотохимической реакцией происходят вторичные реакции, в результате чего на один поглощенный фотон приходится не одна, а несколько молекул продукта реакции.
Например: 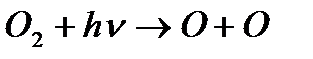 - первичная реакция.
- первичная реакция.
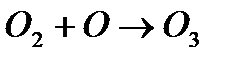
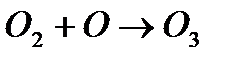
Один квант вызывает превращение трех молекул кислорода.
Причиной значения γ < 1 является наличие примесей, которые поглощают фотоны. В некоторых случаях пониженный квантовый выход объясняется обратимостью химической реакции.
К фотохимическим реакциям относятся фотосинтез, зрительный процесс, образование загара кожи.
Цепные реакции.При образовании хлороводорода квантовый выход очень велик и составляет 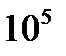 , в связи с этим М.Боденштейн предложил цепной механизм подобных реакций, при котором фотохимическая реакция только начинает цепь и в дальнейшем не играет никакой роли. Например,
, в связи с этим М.Боденштейн предложил цепной механизм подобных реакций, при котором фотохимическая реакция только начинает цепь и в дальнейшем не играет никакой роли. Например,
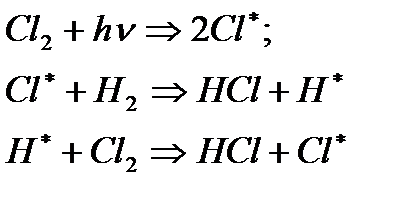
и т.д.
Зарождение цепи реакций происходит не только под влиянием света, но и под действием радиоактивного излучения, введение свободных атомов.
Например, введение паров Na инициирует смесь H2 и Cl2
Na + Cl 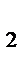 →NaCl+Cl
→NaCl+Cl 
Из сказанного следует, что первая стадия цепных реакций может быть вызвана самыми различными способами.
Вторая стадия- рост цепи- может носить простой и разветвленный характер. Взаимодействие H2 и Cl2 является примером простой цепной реакции.
В реакциях с разветвленной цепью на каждый исчезающий активный центр, возникает несколько новых. Схематично это можно представить следующим образом:

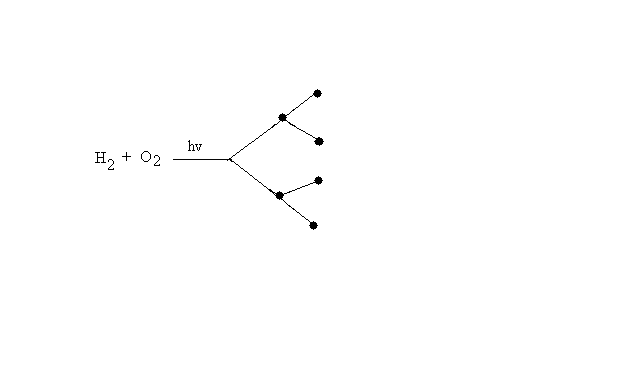
Многие реакции, протекающие в организме под действием ферментов, носят цепной характер. Рассмотрим перекисное окисление липидов.
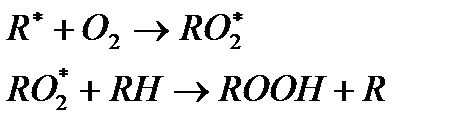
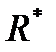 - органический радикал;
- органический радикал;
 - липид;
- липид;
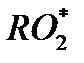 - пероксидный радикал;
- пероксидный радикал;
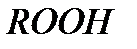 - органический пероксид.
- органический пероксид.
Третья стадия представляет собой процесс гибели активных частиц.
Явление обрыва цепи было рассмотрено в опытах Н.Н.Семенова.
Причины обрыва цепи :
- добавление инертного газа;
- взаимодействие активных частиц со стенками сосудов;
- образование неустойчивых соединений типа HO2, соответствующего тетраокисям металлов NaO2, KO2;
