Ответ: теплота образования метанола равна 153,57 кДж/моль
Задание 160. Определите, при какой температуре начинается реакция восстановления оксида кальция углем:
СаО + 3С = СаС2 + СО.
Решение. Используем табличные данные:
| Вещество | DН0 обр., кДж/моль | S0, Дж/моль×К | DG0, кДж/моль |
| С (графит) | 5,7 | ||
| СО (г) | - 110,5 | 197,5 | - 137,1 |
| СаО (кр) | - 635,5 | 39,7 | - 604,2 |
| СаС2 (кр) | - 62,8 | 70,2 | - 67,8 |
СаО + 3С = СаС2 + СО. Рассчитаем стандартное изменение энтальпии реакции: 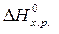 = å(n
= å(n 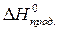 )– å(m
)– å(m 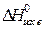 ) =
) = 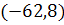 + (-110,5) –(- 635,5)= =462,2 кДж ,
+ (-110,5) –(- 635,5)= =462,2 кДж , 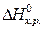
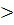 0 – эндотермическая реакция. Рассчитаем стандартное изменение энтропии реакции:
0 – эндотермическая реакция. Рассчитаем стандартное изменение энтропии реакции:
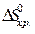 =å(n
=å(n 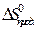 ) – å (m
) – å (m 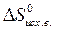 )= (197,5+70,2) – (39,7+3
)= (197,5+70,2) – (39,7+3 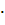 5,7) =210,9
5,7) =210,9 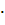 10-3Дж/К
10-3Дж/К
Рассчитаем стандартное изменение энергии Гиббса реакции:
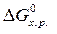 =
= 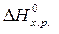 –
– 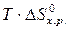 = )= 462,2 –298×(210,9
= )= 462,2 –298×(210,9  10-3) = 399,35 кДж.
10-3) = 399,35 кДж.
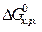
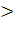 0, при Т = 298 К прямая реакция не возможна.
0, при Т = 298 К прямая реакция не возможна.
Определим температуру, при которой устанавливается химическое равновесие. Если пренебречь зависимостями 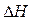 и DS от температуры и считать их постоянными, можно рассчитать энергию Гиббса при нестандартной температуре Т:
и DS от температуры и считать их постоянными, можно рассчитать энергию Гиббса при нестандартной температуре Т:
DG=DН – Т×DS » 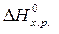 –
– 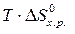
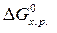 =
= 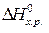 –
– 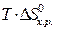 = 0
= 0
Т = 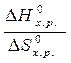 =462,2 /210,9
=462,2 /210,9  10-3= 2191,6 К
10-3= 2191,6 К
Ответ: При нормальных условиях реакция невозможна. Данная реакция начнется при температуре 2079,2 К.
Задание 210. В каком направлении произойдет смещение равновесия в системе: CO(г) + Cl2(г)«COCl2(г), если а) увеличить объем системы, б) увеличить концентрацию СО?
Ответ.
Направление смещения химического равновесия определяется принципом Ле Шателье: если на систему, находящуюся в равновесии, оказывается внешнее воздействие, путем изменения давления, объема, температуры, концентрации, то равновесие смещается в том направлении, которое ослабляет внешнее воздействие.
а) Понижение давления (расширение системы) в сторону веществ, занимающих больший объем, то есть в нашем случае в сторону обратной реакции( в сторону исходных веществ); б) увеличение концентрации исходных веществ увеличивают выход продуктов реакции (сдвигают равновесие в сторону прямой реакции).
Задание185. Вычислить, во сколько раз изменится скорость реакции, протекающей в газовой фазе,
N2 + 3H2 = 2NH3, если
а) давление системы уменьшить в 2 раза;
б) увеличить концентрацию водорода в 3 раза?
Ответ. Используем закон действия масс: скорость элементарной химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ с учетом стехиометрических коэффициентов.
а)Согласно условию при уменьшении давления в два раза, концентрация реагирующих веществ также уменьшится в 2 раза. Запишем выражение скорости реакции по начальным данным и после повышения концентрации:
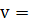 k
k 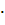 c(N2)
c(N2) 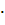 c(H2)3, после уменьшения концентрации
c(H2)3, после уменьшения концентрации
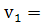 k
k 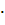 c(N2)
c(N2) 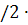 c(H2)3/23, тогда скорость реакции уменьшится
c(H2)3/23, тогда скорость реакции уменьшится
v1=k 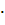 4c(CO)
4c(CO) 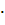 4c(Cl2),тогда скорость реакции уменьшится
4c(Cl2),тогда скорость реакции уменьшится 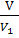 = 23
= 23 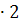 = 16 раз.
= 16 раз.
Б) при увеличении концентрации водорода в 3 раза: 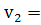 k
k 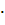 c(N2)
c(N2) 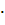 c(H2)3
c(H2)3 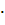 33, найдем соотношение скоростей реакции
33, найдем соотношение скоростей реакции 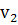 /
/ 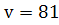 раз.
раз.
Ответ: а) при уменьшении давления в системе в 2 раза, скорость реакции уменьшится в 16 раз; при увеличении концентрации водорода в 3 раза, скорость реакции увеличится в 81 раз.
Задание 235. Составьте схему элемента с концентрацией ионов серебра 10-2 моль/л у одного электрода и 10-4 моль/л у другого электрода. Укажите, какой из электродов будет катодом, а какой – анодом, как называется этот элемент. Рассчитайте электродвижущую силу элемента.
Ответ.
Дано:
С1(AgNO3)=0,01М
С2(AgNO3)=0,0001М
ЭДС-?
По условию имеем концентрационный гальванический элемент.
Концентрационный элемент – это гальванический элемент, состоящий из двух одинаковых металлических электродов, опущенных в растворы соли этого металла с различными активностями (концентрациями) а1 > а2. Катодом в этом случае будет являться электрод с большей концентрацией. Т.к. стандартные электродные потенциалы обоих электродов равны, для ЭДС концентрационного гальванического элемента получаем для ЭДС из уравнения Нернста Е = (RT/zF)•ln(a1/a2),где R - универсальная газовая постоянная, Т - температура, в К, z - заряд катиона металла, F - число Фарадея.
Иногда различием в активностях и концентрациях пренебрегают, тогда вместо а1 и а2 подставляем концентрации С1 и С2.
Таким образом, подставляя Т=298 К, величины констант, и переведя натуральный логарифм в десятичный, получаем для ЭДС
ЭДС = (2,3•8,31•298/1•96500)•lg(0,01/0,0001) = 0,118 В
Схема концентрационного свинцового гальванического элемента:
А(-)Аg | Аg + (0,001 M) || Аg + (0,01 M)| Аg (+)K
Схема электродных процессов:
А: Аg0 – ē = Аg+ |1| - окисление
К: Аg+ + ē = Аg0 |1| - восстановление
Можно решить и следующим образом:
Определим потенциал серебряного анода по уравнению Нернста:
E(анод) = E0(Аg+/Аg) + (0,059/1) 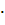 lg[Аg+] = 0,80 + (0,059/1)
lg[Аg+] = 0,80 + (0,059/1) 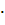 lg(0,0001) = 0,564 B
lg(0,0001) = 0,564 B
Определим потенциал серебряного катода по уравнению Нернста:
E(катод) = 0,8 + (0,059/1) 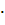 lg(0,01) = 0,682B
lg(0,01) = 0,682B
ЭДС гальванического элемента:
ЭДС = E(катод) - E(анод) = 0,682 - 0,564 = 0,118 В
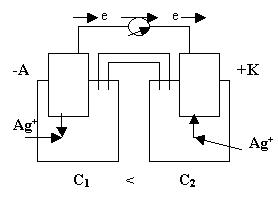
Электроны перемещаются от анода С2(AgNO3)=0,0001М к катоду С1(AgNO3)=0,01М.
Ответ: 0,118В.
