Окислительно-восстановительное титрование
Методы редоксометрии основаны на реакциях окисления-восстановления. Разработано очень много методов. Их классифицируют в соответствии с применяемым стандартным (рабочим, титрантом) раствором. Наиболее часто применяются следующие методы:
Перманганатометрия - метод, который основан на окислительной способности рабочего раствора перманганата калия KМnO4. Титрование ведется без индикатора. Применяется для определения только восстановителей при прямом титровании.
Иодометрия – метод, в котором рабочим титрованным раствором служит раствор свободного иода в КI. Метод позволяет определять как окислители, так и восстановители. Индикатором служит крахмал.
Дихроматометрия основана на использовании в качестве рабочего раствора дихромата калия K2Cr2O7. Метод может применяться как для прямых так и косвенных определений восстановителей.
Броматометрия основана на использовании в качестве титранта бромата калия KBrO3 при определении восстановителей.
Иодатометрия применяет в качестве рабочего раствора раствор иодата калия KIO3 при определении восстановителей.
Ванадатометрия дает возможность использовать окислительную способность ванадата аммоноя NH4VO3. Кроме перечисленных методов в лабораторной практике используются и такие методы как цериметрия (Ce4+), титанометрия и другие.
Для вычисления молярной массы эквивалента окислителей или восстановителей учитывается число электронов, принимающих участие в окислительно-восстановительной реакции (Мэ = М/ne , где n – число электронов е). Для определения числа электронов необходимо знать начальную и конечную степень окисления окислителя и восстановителя.
Из большого числа окислительно-восстановительных реакций для химического анализа используют только те реакции, которые:
· протекают до конца;
· проходят быстро и стехиометрично;
· образуют продукты определенного химического состава (формулы);
· позволяют точно фиксировать точку эквивалентности;
· не вступают в реакцию с побочными продуктами, присутствующими в исследуемом растворе.
Наиболее важными факторами, оказывающими влияние на скорость реакции, являются:
· концентрация реагирующих веществ;
· температура;
· значение рН раствора;
· присутствие катализатора.
В большинстве случаев скорость реакции находится в прямой зависимости от температуры и рН раствора. Поэтому многие определения методом окислительно-восстановительного титрования следует проводить при определенном значении рН и при нагревании.
Индикаторы окислительно-восстановительного титрования.
При анализе методами окислительно-восстановительного титрования используется прямое, обратное и заместительное титрование. Точка эквивалентности окислительно-восстановительного титрования фиксируется как с помощью индикаторов, так и безиндикаторным способом. Безиндикаторный способ применяется в тех случаях, когда окисленная и восстановленная формы титранта отличаются. В точке эквивалентности, при введении 1 капли избытка раствора титранта изменит окраску раствора. Безиндикаторным способом можно проводить определения перманганатометрическим методом, т.к. в точке эквивалентности от одной капли раствора перманганата калия титруемый раствор окращивается в бледнорозовый цвет.
При индикаторном способе фиксирования точки эквивалентности применяют специфические и редоксиндикаторы. К специфическим индикаторам относится крахмал в иодометрии, который в присутствии свободного иода окрашивается в интенсивно-синий цвет вследствие образования адсорбционного соединения синего цвета. Редокс-индикаторы – это вещества, у которых окраска меняется при достижении определенного значения окислительно-восстановительного (редокспотенциала). К редокс-индикаторам относится, например, дифениламин NH(C6H5)2. При действии на бесцветные растворы его окислителями он окрашивается в сине-фиолетовый цвет.
Редокс-индикаторам предъявляют следующие требования:
· окраска окисленной и восстановленной формы должна быть различна;
· изменение цвета должно быть заметно при небольшом количестве индикатора;
· индикатор должен реагировать в точке эквивалентности с весьма небольшим избытком восстановителя или окислителя;
· интервал действия его должен быть как можно меньше;
· индикатор должен быть устойчив к воздействию компонентов окружающей среды (О2, воздуха, СО2, света и т.п.).
Интервал действия редокс-индикатора рассчитывается по формуле:
Е = Ео ± 0,058/n
где Ео - нормальный окислительно-восстановительный потенциал индикатора (в справочнике), n - число электронов, принимающих в процессе окисленияили восстановления индикатора.
Иодометрия.
Иодометрический метод титриметрического анализа основанный на реакциях окисления-восстановления(разновидность оксидиметрии) с участием иода или иодида:
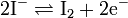
Иодометрически определяют кислоты:
IO3− + 5I− + 6Н+ = 3I2 + ЗН2О
О количестве определяемого вещества судят по количеству поглощенного или выделенного иода. Вещества, окислительно-восстановительный потенциал которых ниже 0,545 В, будут являться восстановителями (SO2, Na2S2O3, SnCl2 и др.) и, следовательно, будет протекать реакция с поглощением иода. Равновесие будет смещено вправо. Вещества, окислительно-восстановительный потенциал которых будет больше 0,545 В, будут окислителями (KMnO4, MnO2, K2Cr2O7, Cl2, Br2 и др.) и направлять реакцию влево, в сторону выделения свободного йода.
В связи с этим иодометрический метод применяется как для определения восстановителей, так и окислителей. Иодометрические определения проводятся в кислой среде, так как в щелочной среде может образоваться гипоиодид ион, окислительная способность которого выше, чем иода, что может способствовать протеканию побочных процессов, в частности окислять тиосульфат ион до сульфата и результаты будут искажены.
При определении сильных восстановителей (Ео намного больше 0,545 В) применяется прямое титрование, а слабых (Ео близко к 0,545 В) - обратное титрование. Рабочим раствором (титрант) служит раствор I2 Окислители определяются только способом заместительного титрования, т.к. при использовании в качестве рабочего раствора иодида калия невозможно зафиксировать точку эквивалентности (момент прекращения выделения иода). В качестве титранта при определении окислителей применяется раствор тиосульфата натрия, который взаимодействует с выделившимся йодом (заместитель) в эквивалентном количестве.
В качестве индикатора в йодометрии применяют свежеприготовленный 1%-ный раствор крахмала. При взаимодействии крахмала с иодом протекают 2 процесса - комплексообразование и адсорбция, в результате которых образуется соединение синего цвета. Чувствительность реакции с крахмалом велика, но резко падает с повышением температуры.
