Физико-химические основы горения и взрыва. Горение, виды горения
1. Горение - это химическая реакция окисления, сопровождающаяся выделением большого количетва тепла и свечением.
2. В зависимости от скорости протекания процесса, горение может происходить в форме собственно горения и взрыва.
3. Взрыв - это частный случай горения, протекающего мгновенно с кратковременным выделением значительного
количества тепла и света.
4. Для процесса горения необходимо:
1) наличие горючей среды, состоящей ив горючего вещества и окислителя; 2) источника воспламенения.
Чтобы возник процесс горения, горючая среда должна быть нагрета до определенной температуры при помощи источника воспламенения (пламя, искра электрического или механического происхождения, накаленные тела, тепловое проявление химической, электрической или механической энергий).
5. После возникновения горения постоянным источником воспламенения является зона горения. Возникновение и
6. продолжение горения возможно при определенном количественном соотношении горючего вещества и кислорода, а также при определенных температурах и запасе тепловой энергии источника воспламенения. Наибольшая
скорость стационарного горения наблюдается в чистом кислороде, наименьшая - при содержании в воздухе 14 - 15% кислорода. При меньшем содержании кислорода в воздухе горение большей части веществ прекращается.
6. Различают следующие виды горения:
- полное - горение при достаточном количестве или избытке кислорода;
- неполное - горение при недостатке кислорода.
При полном горении продуктами сгорания являются двуокись углерода (CO2), вода (H2O), азот (N), сернистый ангидрид (SO2), фосфорный ангидрид. При неполном горении обычно образуются едкие, ядовитые горючие и взрывоопасные
продукты: окись углерода, спирты, кислоты, альдегиды.
7. Горение веществ может протекать не только в среде кислорода, но также в среде некоторых веществ, не содержащих кислорода, хлора, паров брома, серы и т.д.
8. Горючие вещества могут быть в трех агрегатных состояниях:
жидком, твердом, газообразном. Отдельные твердые вещества при нагревании
плавятся и испаряются, другие - разлагаются и выделяют газообразные продукты и твердый остаток в виде угля и шлака, третьи не разлагаются и не плавятся. Большинство горючих веществ независимо от агрегатного состояния при
нагревании образуют газообразные продукты, которые при смешивании с кислородом воздуха образуют горючую среду.
По агрегатному состоянию горючего и окислителя различают;
- гомогенное горение - горение газов и горючих парообразующих веществ в среде газообразного окислителя;
- горение взрывчатых веществ и порохов;
- гетерогенное горение - горение жидких и твердых горючих веществ в среде газообразного окислителя;
- горение в системе «жидкая горючая смесь - жидкий окислитель»
9. Важнейшим вопросом теории горения является распространение пламени (зоны резкого возрастания температуры и интенсивной реакции). Различают следующие режимы распространения пламени (горения):
- нормальный режим горения;
- дефлеграционное горение;
- детонация.
а) Нормальный режим горения наблюдается при спокойном гетерогенном двухфазном диффузионном горении. Скорость горения будет определяться скоростью диффузии кислорода к горючему веществу в зону горения.
Распространение пламени происходит от каждой точки фронта пламени по нормали к его поверхности. Такое горение и скорость распространения пламени по неподвижной смеси вдоль нормали к его поверхности называют нормальным
(ламинарным).
Нормальные скорости горения невелики. В этом случае повышения давления и образования ударной волны не
происходит.
б) В реальных условиях вследствие протекания внутренних процессов и при внешних осложняющих факторах происходит искривление фронта пламени, что приводит к росту скорости горения. При достижении скоростей
распространения пламени до десятков и сотен метров в секунду, но не превышающих скорости звука в данной среде (300 – 320м/сек) происходит взрывное (дефлеграционное) горение.
При взрывном горении продукты горения нагреваются до 1.5-3.0 тысяч °С, а давление в закрытых системах
увеличивается до 0.б-0.9МПа.
Продолжительность реакции горения до взрывного режима составляет для газов ~0.1 сек, паров ~0.2 – 0.3 сек, пыли ~0.5 сек.
Применительно к случайным промышленным взрывам под дефлебрацией обычно понимают горение облака с видимой скоростью порядка 100 - 300 м/сек, при которой генерируются ударные волны с максимальным давлением 20 - 100 кПа.
в) В определенных условиях взрывное горение может перейти в детонационный процесс,
при котором скорость распространения пламени превышает скорость распространения звука и достигает 1 - 5 км/сек. Это происходит при сильной турбулизации материальных потоков,
вызывающей значительное искривление фронта пламени большое увеличение его поверхности.
При этом возникает ударная волна, во фронте которой резко повышается плотность, давление температура смеси. При
возрастании этих параметров смеси до самовоспламенения горячих веществ возникает детонационная волна, являющаяся результатом сложения ударной волны и образующейся зоны сжатой быстрореагирующей (самовоспламеняющейся) смеси.
Избыточное давление в пределах детонирующего облака смеси может достигать 2 МПа.
Процесс химического превращения горючих веществ, который вводится ударной волной и сопровождается быстрым выделением энергии, называется детонацией.
При детонационном режиме горения облака ГВ большая часть энергии взрыва переходит в воздушную ударную волну, при дефлеграционном горении со скоростью распространения пламени ~200 м/сек переход энергии в волну составляет от 30 до 40%.
Основные понятия о процессах горения и взрыва. Особенности горения веществ в различных агрегатных состояниях.
Пожарная безопасность – это состояние помещения в котором с установленной вероятностью исключается возможность возникновения пожара.
Пожар – это неконтролируемое горение в результате которого повреждаются материальные ценности и создаётся угроза жизни человека.
Горение – это быстро протекающая реакция окисления в результате которой выделяется большое количество тепла.
Горение различают по скорости:
- горение;
- взрыв;
- детонация.
Все горючие вещества обладают определёнными характеристиками, которые объясняют их опасность:
Вспышка – это быстрое сгорание горючей смеси, не сопровождающие образование сжатых газов.
Температура вспышки (основная характеристика горючих жидкостей) – это наименьшая температура, при которой происходит процесс вспышки, но нет устойчивого горения.
Температура воспламенения – это температура, при которой начинается процесс горения вещества.
Нижний концентрационный придел воспламенения (основная характеристика воспламенения пыли) – это минимальное содержание горючего вещества в воздухе при котором начинается процесс воспламенения.
Из группы горючих веществ выделяют легко воспламеняющие вещества:
- жидкости;
- газы;
- твёрдые.
В зависимости от агрегатного состояния исходного вещества и продуктов Г. различают три основных типа Г.: гомогенное Г., Г. взрывчатых веществ и порохов, гетерогенное Г. Гомогенное горение. Исходные вещества и продукты при таком Г. находятся в одинаковом агрегатном состоянии. К этому типу относится Г. газовых смесей (природного газа, водорода и т. п. с окислителем - обычно кислородом воздуха), Г. негазифицирующихся конденсиров. веществ (напр., термитов - смесей алюминия с окислами разл. металлов) и изотермическое Г.- распространение цепной разветвлённой реакции в газовой смеси без значит. разогрева. На рис. изображена структура фронта Г. в смеси газообразных горючего и окислителя. Хим. реакция происходит в очень узкой зоне (10-5 м) при темп-ре, близкой к темп-ре Г.: 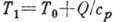 (T0 - темп-pa исходной смеси, Q - теплота сгорания, ср - теплоёмкость газа при пост. давлении). В зоне подогрева темп-pa газа растёт за счёт тепла, выделившегося при Г. предыдущих порций смеси. В этой зоне происходит также убывание (вследствие диффузии) концентрации исходного вещества, хим. реакция идёт в очень обеднённой смеси. Скорость тепловыделения
(T0 - темп-pa исходной смеси, Q - теплота сгорания, ср - теплоёмкость газа при пост. давлении). В зоне подогрева темп-pa газа растёт за счёт тепла, выделившегося при Г. предыдущих порций смеси. В этой зоне происходит также убывание (вследствие диффузии) концентрации исходного вещества, хим. реакция идёт в очень обеднённой смеси. Скорость тепловыделения 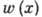 имеет резкий максимум, связанный с тем, что в начале реакции низка темп-pa, а в конце её нет горючего. Скорость Г.
имеет резкий максимум, связанный с тем, что в начале реакции низка темп-pa, а в конце её нет горючего. Скорость Г. 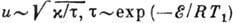 , где
, где 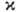 - коэффициенттемпературопроводности, а
- коэффициенттемпературопроводности, а 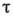 - характерное время хим. реакции в зоне Г., к-рое определяется в основном энергией активации
- характерное время хим. реакции в зоне Г., к-рое определяется в основном энергией активации 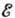 и темп-рой Г. (R - универсальная газовая постоянная).
и темп-рой Г. (R - универсальная газовая постоянная).
Гетерогенное горение. Исходные вещества при этом находятся в разных агрегатных состояниях. Важнейшие техн. процессы гетерогенного Г.: Г. угля, частиц металлов, сжигание жидких топлив в нефтяных топках, нек-рых двигателях внутр. сгорания, камерах сгорания ракетных двигателей. Процесс гетерогенного Г. обычно очень сложен. Хим. превращение сопровождается дроблением и испарением капель и частиц, образованием окисных плёнок на частицах металла, турбулизацией газовой смеси и т. п.
Горение взрывчатых веществ и пороков. Mн. конденсиров. взрывчатые вещества (BB), кроме быстрого (взрывного) протекания реакции (см. Взрыв, Детонация), способны к значительно более медленному хим. превращению путём Г. В отличие от обычных твёрдых и жидких топлив при горении BB не требуется подводить извне окислитель, т. к. горючее и окислитель во BB перемешаны на молекулярном уровне.
Г. BB связано с переходом вещества из конденсиров. состояния в газ. При этом на поверхности раздела фаз происходит сложный физико-хим. процесс, при к-ром в результате хим. реакции выделяется теплота и горючие газы, догорающие в зоне Г., отстоящей от поверхности на нек-ром расстоянии. Процесс Г. усложняется явлением диспергирования - переходом части конденсиров. вещества в газовую фазу в виде небольших частичек или капель.
Важной особенностью процесса Г. является наличие критич. условий. Распространение Г. возможно лишь в нек-рых интервалах изменения состава смеси, темп-ры и давления, условий теплоотвода во внеш. среду. Критич. значения этих параметров наз. пределами Г. Скорость Г. на пределе отлична от нуля, а при переходе через предел Г. прекращается.
При эксперим. исследовании Г. изучается зависимость скорости Г. от разл. параметров Г.: состава смеси, дисперености компонентов, структуры фронта Г., скорости хим. реакций, пределов Г. При этом используются оптич. методы (высокоскоростная киносъёмка, голография), микротермопары (толщина их измеряется микронами), манометрические и калориметрич. бомбы.
