Способы выражения концентрации растворов
Содержание растворенного вещества в растворе может быть выражено несколькими способами:
Массовая доля растворенного вещества: отношение массы растворенного вещества к массе раствора:
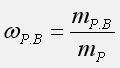
где 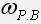 – массовая доля растворенного вещества,
– массовая доля растворенного вещества, 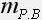 – масса растворенного вещества,
– масса растворенного вещества, 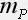 – масса раствора. Это частный случай определения массовой доли.
– масса раствора. Это частный случай определения массовой доли.
Концентрация (молярная концентрация, молярность): отношение количества растворенного вещества 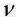 к объему раствора V:
к объему раствора V:
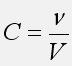
Молярная концентрация имеет принятую в химии размерность [моль/л], которая часто обозначается М и называется молярностью. Например, концентрация раствора 5 моль/л может быть записана как 5 М и такой раствор называется пятимолярным.
Молярная концентрация эквивалента (нормальность) показывает, какое количество моль эквивалентов растворенного вещества содержится в 1 л раствора.
Молярную концентрацию эквивалента Сэк(В) находят как отношение количества эквивалентов вещества nэк(В) к объему раствора Vp
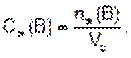
Размерность молярной концентрации эквивалента: моль×л. Сокращенная форма записи единицы молярной концентрации эквивалента – н. Например, 2н. означает, что в 1 л раствора содержится 2 моль эквивалента растворенного вещества.
Зная массу растворенного вещества m(B) и его молярную массу эквивалента Мэк(В), можно найти количество эквивалента вещества:
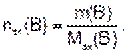
Молярная масса эквивалента вещества равна произведению фактора эквивалентности fэк(В) на молярную массу вещества М(В)
Мэк(В) = fэк(В)×М(В).
Эквивалент – это реальная или условная частица вещества, соответствующая в реакциях обмена одному атому или иону водорода (Н или Н+), а в окислительно-восстановительных реакциях – одному электрону.
Фактор эквивалентности – число, показывающее, какую часть от реальной частицы (молекулы, атома, иона и т.д.) вещества составляет эквивалент этого вещества.
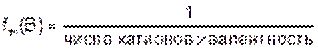 .
.
Например, для Na3PO4 заряд катиона Na+ равен 1, число катионов – 3, тогда
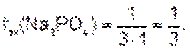
Пример. Вычислите молярную концентрацию эквивалента хлорида железа (III) в растворе, полученном при растворении 40 г FeCl3 в 200 мл воды. Плотность раствора 1,182 г/мл.
Решение.
Молярная масса хлорида железа (III):
M(FeCl3) = 162 г/моль.
Фактор эквивалентности fэк = 1/3.
Молярная масса эквивалента
Mэк(FeCl3) = fэк(FeCl3)×M(FeCl3) = 162 × (1/3) = 54 г/моль.
Количество эквивалента вещества, содержащегося в 40 г хлорида железа (III), составляет:
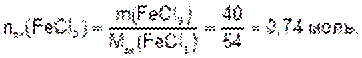
Масса раствора:
mp = m(FeCl3) + m(H2O);
ρ(H2O) = 1 г/мл; m(H2O) = 200 × 1 = 200 г;
mp = 40 + 200 = 240 г.
Объем раствора: 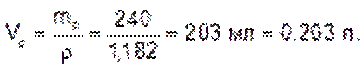
Находим молярную концентрацию эквивалента раствора хлорида железа (III):
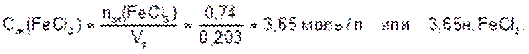
Моляльная доля растворенного вещества (Моляльность) [моль/кг] - безразмерная величина, равная отношению количества растворенного вещества к общему количеству веществ в растворе:
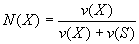
где N(Х) - мольная доля растворенного вещества X; v(Х) - количество растворенного вещества X, моль;
v(S) - количество вещества растворителя S, моль.
