Работа 2. «Определение содержания кальция в воде»
Определение основано на взаимодействии ионов кальция, находящихся в анализируемом растворе, с трилоном Б по уравнению реакции:
Са2+ + H2Y2- « СаY 2- + 2H+
Так как комплексонат кальция относительно малоустойчив (lgK = 10,7), создание щелочной среды при анализе необходимо для сдвига реакции взаимодействия вправо. Для определения конечной точки титрования применяется металлохромный индикатор мурексид.
Ход работы:
С помощью пипетки на 25 мл в конические колбы для титрования отбирают аликвотные пробы, добавляют 2,5 мл 2Н раствора NaOH, сухую индикаторную смесь «мурексид» (на кончике шпателя) до красной окраски и титруют раствором трилона Б до перехода окраски в фиолетовую. По показаниям бюретки определяют объём раствора трилона Б, пошедший на титрование, и полученные результаты заносят в таблицу 3:
Таблица 3
Результаты опыта
| № п/п | Vтрилона Б | Стрилона Б | Vводы | m(Ca) |
| среднее |
По результатам титрований рассчитывают массу кальция в анализируемом растворе:
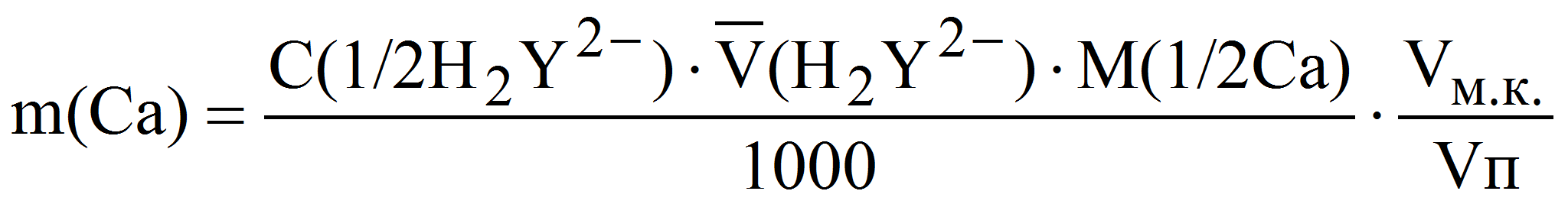


Задачи для самостоятельного решения
Пример 1.
Вычислить массовую долю (%) CaCO3 и MgCO3 в известняке, если после растворения 1,000 г его получили 100,0 мл раствора, на титрование 20,00 мл которого для определения суммы Ca и Mg израсходовали 19,25 мл 0,05140 М ЭДТА, а на титрование Ca с мурексидом в отдельной пробе затратили 6,25 мл того же раствора ЭДТА.
Решение.
Если через ω(CaCO3) обозначить массовую долю (%) CaCO3, то по результатам титрования пробы на содержание кальция с мурексидом можно записать
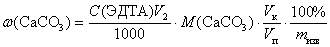 .
.
Подставляя числовые значения, получаем
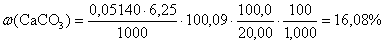
Объем стандартного раствора ЭДТА, затраченный на титрование Mg, найдем как V1–V2 = 19,25 – 6,25 = 13,00 мл, тогда
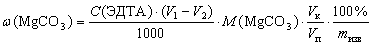 ,
,
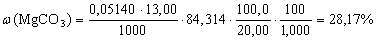 .
.
Пример 2.
На титрование 20,00 мл раствора Hg(NO3)2 после добавления избытка Na2MgY (комплексоната магния) и протекания реакции замещения
MgY2- + Hg2+ → HgY2- + Mg2+
затрачено 19,85 мл 0,05 М ЭДТА (K=1,055). Вычислить концентрацию (г/л) раствора Hg(NO3)2.
Решение.
При титровании по методу замещения
n(Hg2+) = n(Mg2+) = n(ЭДТА).
Выразим количество вещества ЭДТА (моль) с учетом условия задачи
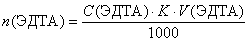
Тогда массу определяемого вещества можно представить формулой
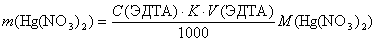
Концентрацию исходного раствора Hg(NO3)2 можно выразить в виде
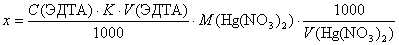
После подстановки числовых значений получаем:
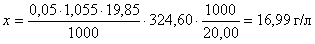
1. На титрование 40мл воды при определении общей жесткости потребовалось 5,10мл 0,015М раствора трилона Б. Вычислить общую жесткость воды.
2. Рассчитать концентрацию магния в воде (в ммоль/л) если при титровании 200мл воды ЭДТА при рН = 9,7 с хромогеном черным Т до синей окраски израсходовано 25мл 0,015М раствора.
3. Сколько граммов меди обнаружено в растворе, если на титрование этого раствора уходит 15 мл 0,03М раствора ЭДТА в присутствии индикатора мурексида?
4. Навеску MgCl2 , равную 0,3г, растворили в мерной колбе вместимостью 250мл. На титрование 25мл полученного раствора израсходовали 10,5мл 0,025М раствора ЭДТА. Рассчитать массовую долю MgCl2 в исследуемом образце.
5. На титрование 15,0мл минеральной воды израсходовано 2,8мл 0,05М раствора ЭДТА. Рассчитать общую жесткость воды.
