Реакции нуклеофильного замещения
За счет электрофильного центра в молекулах карбоновых кислот протекают реакции нуклеофильного замещения. Замещение, а не присоединение с разрывом π-связи характерно потому, что при этом не нарушается p,π-сопряженная система.
Рассмотрим механизм реакции SN в общем виде:
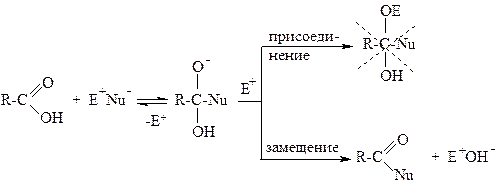 |
Новая связь C-Nu образуется за счет пары электронов нуклеофила. π-Связь C=O разрывается гетеролитически, пара электронов уходит к кислороду, на нем возникает отрицательный заряд. На следующей стадии реакции электрофил E+ может присоединиться к O-, но при этом сопряженная система нарушится. Этот путь реакции для карбоновых кислот не характерен. Электрофил E+ может также отщепить группу HO-, при этом вновь образуется p,π-сопряженная система. Поэтому данный путь реакции (замещение) и характерен для карбоновых кислот.
По механизму нуклеофильного замещения протекает, например, реакция образования сложных эфиров (реакция этерификации).
В этой реакции участвуют карбоновая кислота и спирт в присутствии концентрированной серной кислоты. Например:
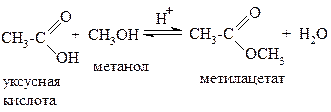 |
Серная кислота необходима как водоотнимающее средство и как катализатор.
Рассмотрим механизм реакции этерификации:
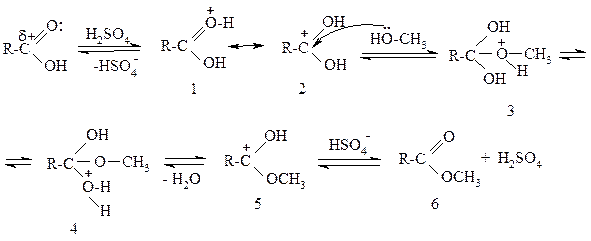 |
Молекула спирта – это слабый нуклеофил. Поэтому для успешного протекания реакции необходимо активизировать электрофильный центр в молекуле карбоновой кислоты. С этой целью и применяют серную кислоту как катализатор. Реакция начинается по основному центру карбоновой кислоты, к которому присоединяется протон водорода. Протонированная карбоновая кислота может существовать в виде двух резонансных структур (1 и 2). В катионе (2) на электрофильном центре существует полный положительный заряд, а не частичный, как в исходной молекуле карбоновой кислоты, т.е. электрофильный центр активизировался. Далее он атакуется нуклеофильным реагентом – молекулой спирта. Новая связь C-O образуется за счёт неподеленной электронной пары кислорода, поэтому на нем появляется положительный заряд (3). Кислород отщепляет протон водорода, чтобы компенсировать положительный заряд, а протон присоединяется к неподеленной электронной паре другого атома кислорода. Он также получает положительный заряд (4). Далее происходит отщепление молекулы воды и образование катиона (5), для стабилизации которого необходимо отщепление протона водорода (под действием гидросульфат-аниона, оставшегося в реакционной среде). Образуется молекула сложного эфира (6) и серная кислота – катализатор реакции.
Сложные эфиры являются функциональными производными карбоновых кислот, т.е. производными, полученными путем замещения гидроксила в карбоксильной (функциональной) группе на нуклеофил.
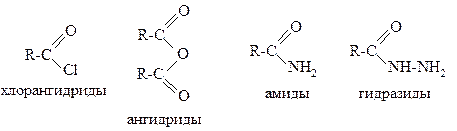 Другими функциональными производными карбоновых кислот являются:
Другими функциональными производными карбоновых кислот являются:
Все эти производные могут быть получены из карбоновых кислот.
Так, хлорангидриды кислот получают при взаимодействии карбоновых кислот с тионилхлоридом (SOCl2) или хлоридом фосфора (PCl5), например:
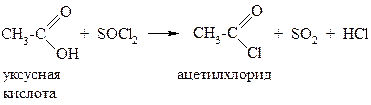 | |||
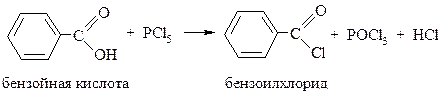 |
Ангидриды образуются при нагревании карбоновых кислот с водоотнимающими средствами, например с P2O5:
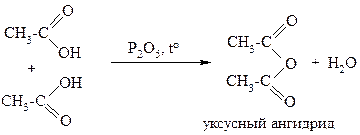 |
Амиды могут быть получены при взаимодействии карбоновых кислот с аммиаком с последующим термическим разложением образующихся аммониевых солей:
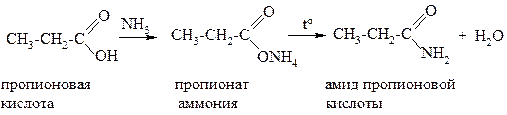 |
Функциональные производные карбоновых кислот можно также получить одни из других (менее активные из более активных).
Сравним активность функциональных производных карбоновых кислот в реакциях нуклеофильного замещения. Для этого необходимо сравнить величины частичных положительных зарядов на электрофильном центре, т.е. рассмотреть влияние заместителей на δ+.
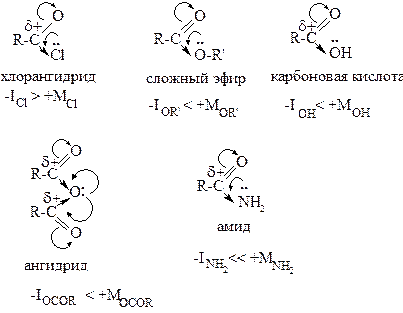
Атом хлора в хлорангидриде оказывает электроноакцепторное действие, т.е увеличивает величину δ+ на электрофильном центре (активность также увеличивается). Гидроксильная группа в молекуле кислоты и алкокси-группа (OR’) в сложном эфире оказывают примерно одинаковое электронодонорное действие, понижая величину частичного положительного заряда на электрофильном центре, значит, в сравнении с хлорангидридом активность также будет снижаться. Заместитель в молекуле ангидрида кислоты также является электронодонорным, но его влияние распределяется пополам между двумя электрофильными центрами. Величина δ+ уменьшается, но не так сильно, как в случае карбоновой кислоты или сложного эфира. И, наконец, в молекуле амида кислоты электронодонорное действие NH2-группы проявляется наиболее сильно, и активность амидов в реакциях нуклеофильного замещения самая низкая.
Таким образом, ряд убывания активности функциональных производных карбоновых кислот в реакциях нуклеофильного замещения следующий:
хлорангидрид > ангидрид > сложный эфир ≈ карбоновая кислота > амид.
Сравнивая активность функциональных производных карбоновых кислот с позиций «уходящей группы» (см. стр. 50), можно сделать тот же вывод (ведь чем лучше «уходящая группа», тем успешнее протекает реакция).

Исходя из этого, из хлорангидридов кислот можно получить все остальные функциональные производные, из ангидридов кислот – сложные эфиры, карбоновые кислоты и амиды.
Рассмотрим реакции хлорангидридов кислот:
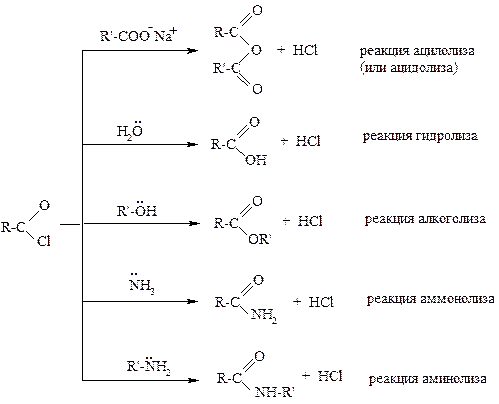 |
Все эти реакции протекают по механизму нуклеофильного замещения, нуклеофилами являются, соответственно, карбоксилат-анион, вода, спирт, аммиак и амин. Реакции протекают активно, не требуют нагревания.
По отношению к хлорангидриду кислоты эти реакции называют гидролиз, аминолиз и т.д. («лизис» – расщепление). С другой стороны, по отношению к спирту, амину и т.д. – это реакции ацилирования (введение в молекулу остатка карбоновой кислоты – ацила). Поэтому ряд убывания активности функциональных производных карбоновых кислот в реакциях нуклеофильного замещения можно также назвать рядом убывания ацилирующей способности.
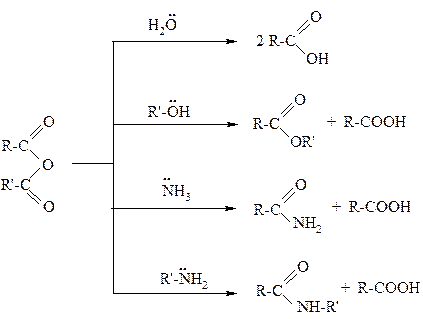 Из ангидридов карбоновых кислот можно получить все другие функциональные производные, кроме хлорангидридов:
Из ангидридов карбоновых кислот можно получить все другие функциональные производные, кроме хлорангидридов:
Реакции протекают менее активно, чем с хлорангидридами кислот.
В биохимических процессах важную роль играют смешанные ангидриды карбоновых кислот и фосфорной кислоты – ацилфосфаты.
С их помощью в организме осуществляется перенос ацильных групп к гидроксильным, тиольным и аминогруппам различных соединений:
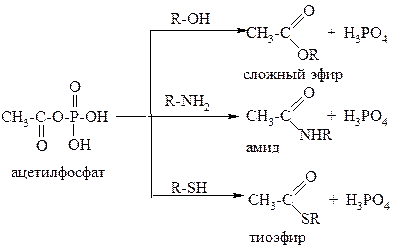
Сложные эфиры вступают в реакции гидролиза и образования амидов.
Гидролиз сложных эфиров проводят в кислой или щелочной среде. Кислотный гидролиз является обратимым процессом:
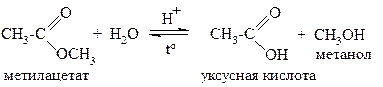 |
Щелочной гидролиз сложных эфиров необратим, т.к. в результате реакции образуются соли карбоновых кислот, для которых реакции SN не характерны:
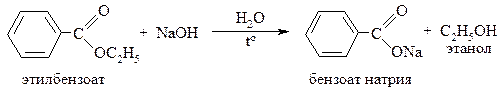 |
Реакции гидролиза сложных эфиров протекают не столь активно, как гидролиз ангидридов или галогенангидридов кислот.
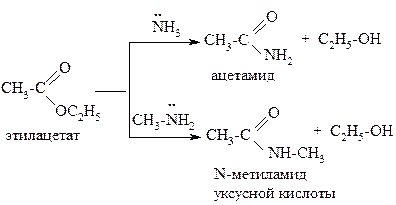 Сложные эфиры вступают также в реакции нуклеофильного замещения с аммиаком и аминами с образованием соответствующих амидов:
Сложные эфиры вступают также в реакции нуклеофильного замещения с аммиаком и аминами с образованием соответствующих амидов:
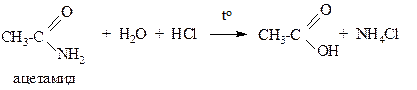 Амиды карбоновых кислот являются наименее активными функциональными производными. Они подвергаются гидролизу, но только в достаточно жестких условиях (кипячение с водными растворами кислот или щелочей в течение длительного времени).
Амиды карбоновых кислот являются наименее активными функциональными производными. Они подвергаются гидролизу, но только в достаточно жестких условиях (кипячение с водными растворами кислот или щелочей в течение длительного времени).
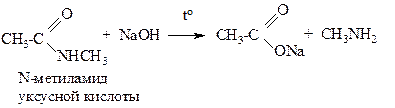 |
За счёт p,π-сопряжения основные свойства амидов понижены в сравнении с аминами. Амиды кислот образуют соли с сильными минеральными кислотами. Предполагают, что при этом амид образует соль за счёт оксониевого основного центра:
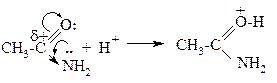 |
Амиды могут реагировать также с сильными основаниями, например, амидом натрия, проявляя кислотные свойства:
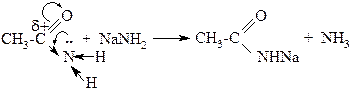 |
