Способы титрования в объемном анализе
Прямое титрование. Титрант (рабочий раствор) добавляют в небольшом количестве из бюретки к анализируемому раствору до состояния эквивалентности. Определяют объем титранта по бюретке, результат записывают в журнал. Расчет концентрации производят исходя из закона эквивалентов.
Пример: определить эквивалентную концентрацию и титр раствора соляной кислоты, если на титрование 2 мл соляной кислоты пошло 3 мл 0,0205 моль/л раствора NaOH.
Решение: реакция, заложенная в определении:
HCl + NaOH=NaCl + H2O
По закону эквивалентов Cн(HCl) ∙V(HCl) = Cн(NaOH)∙ V(NaOH)

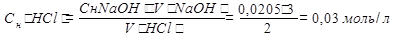
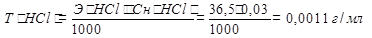
Обратное титрование. Метод заключается в последовательном использовании двух титрантов.
Первый из них добавляется к определяемому раствору точно отмеренным объемом и в избытке. При этом титрант вступает в реакцию с определяемым веществом, а избыток его (первого рабочего раствора) оттитровывают вторым титрантом до момента эквивалентности.
Пример: определить количество в (г) хлорида натрия в растворе, если к его раствору добавили в избытке 10 мл 0,1н раствора AgNO3 , избыток нитрата серебра оттитровали в присутствии индикатора железоаммиачных квасцов и на титрование пошло 4 мл 0,1н раствора роданида калия.
Решение: Реакции, заложенные в определении:
NaCl + AgNO3 = AgCl + NaNO3
AgNO3 (изб.) + KNCS = KNO3 + AgNCS↓
По второй реакции определяют избыток раствора нитрата серебра:
Cн(AgNO3)∙ ∙V(AgNO3) = Cн(KNCS)∙∙ V(KNCS)

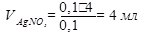
Объем нитрата серебра, затраченный на реакцию с хлоридом натрия, определяют следующим образом:
V (AgNO3)общ. ─ V (AgNO3)изб. =10 − 4 =6 (мл)
Количество грамм хлорида натрия определяют по закону эквивалентов:
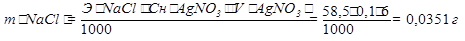
Косвенное титрование или титрование по замещению.
В этом случае, как и в прямом титровании, используется один титрант, но титруют им не анализируемое вещество, а продукт реакции, образующийся при взаимодействии определяемого вещества со вспомогательным компонентом.
Пример: определить количество активного хлора в белильной извести, навеска которой -равна 0,402 г, если на образовавшийся иод израсходовано 10 мл 0,02н раствора тиосульфата натрия (индикатор – крахмал).
Решение: Реакции, заложенные в определении:
CaOCl2 + 2HCl =CaCl2 + Cl2 + H2O
Cl2 + 2KJ = 2KCl + J2
J2 + 2Na2S2O3 = 2NaJ + Na2S4O6
Количество хлора, характеризующее активность хлорной извести, косвенно вступает в реакцию с тиосульфатом натрия:
Э(Cl2) − Э(Na2S2O3)
m(Cl2) ─ (T V) Na2S2O3
Отсюда:
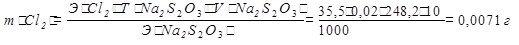
Навеска хлорной извести была 0,402 г, активного хлора в ней 0,0071 г, что в % составляет 0,0071∙100/0,402 = 17,1%
Ответ: активный хлор в хлорной извести составил 17,1%, что по ГОСТу указывает: данная хлорка может быть использована для дезинфекции.
