Электролиты в роли структурообразователя
При промывке скважины в соленосных горных породах глинистыми и полимерными растворами происходит их нейтрализация и интенсивная коагуляция поэтому ведутся поиски по замене этих растворов растворами, устойчивыми к солевой агрессии. К таким растворам можно отнести растворы с конденсированной твердой фазой. Конденсированная твердая фаза должна быть:
- гидрофильной, обладать активными функциональными группами: – ОН-; – СО3-; 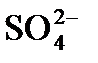 ; SiO2-;
; SiO2-;
- агрегативно- и седиментационно устойчивой.
Для получения конденсированной твердой фазы используют легкорастворимые в воде соли, вступающие друг с другом или с водой в реакцию с получением нерастворимых или малорастворимых (но с гидрофильной поверхностью) соединений.
Так, в результате взаимодействия ионов магния растворенного в воде бишофита с гидроксильной группой ОН- каустической соды образуются кристаллогидраты гидроксида магния с гидрофильной поверхностью:
MgCl2+NaOH=Mg(OH)2+Na++Cl-
Благодаря наличию полярных групп -ОН вокруг микрокриcталлов Mg(OH)2 в воде образуются гидратные слои, значительной толщины, в результате чего раствор в спокойном состоянии превращается в гидрогель. Поэтому буровые растворы с конденсированной твердой фазой, содержащей гидроксильную группу, получили название гидрогелей (в данном случае гидрогель магния).
С целью получения твердой фазы с большой удельной поверхностью и большей агрегативной и седиментационной устойчивостью рост частиц твердой фазы ограничивают введением в раствор полимеров (чаще всего КМЦ). Адсорбируясь на микрокристаллах Mg(OH)2, КМЦ не только ограничивает рост кристалла, но и активирует поверхность твердой фазы.
Подобные гидрогели могут образовывать гидроксиды трех и четырехвалентных элементов: Al(OH)3; Si(ОН)4 и т.д. В отличие от двухвалентных металлов, которые образуют гидроксиды только в щелочной среде трех- и четырехвалентные элементы образуют гидроксиды в нейтральной и даже в кислой среде. Так, например, гидроксид алюминия появляется уже при рН=5. При действии на кислые растворы солей алюминия щелочью из раствора выпадает студенистый осадок гидрогеля алюминия.
Кремниевые кислоты Н2О·SiO2, Si(OH)4, в растворе также образуют гидрогели.
Предотвращая сращивание микрокристаллов с помощью полимеров, получают стойкие структурированные растворы.
Наряду с гидрогелями широкое распространение получают солегели промывочные жидкости твердой фазой, образованной из двух взаимодействующих в растворе солей:
 Na2CO3+CaCl2=CaCO3+2Na++2Cl-
Na2CO3+CaCl2=CaCO3+2Na++2Cl-
 Na2SiO3+CaCl2=CaSiO3+2Na++2Cl- и т.д.
Na2SiO3+CaCl2=CaSiO3+2Na++2Cl- и т.д.
и гидрогели,образованные из двух солей и воды:
Al(SO4)3+3CaCl2+3H2O=3CaSO4+2Al(OH)3+3H++3Cl-
Полученные таким образом соли также имеют гидрофильные функциональные группы и способны образовывать гели, поэтому их называют солегелями и гидросолегелями.
С целью ограничения роста кристаллов и гидрофилизации твердой фазы так же, как и при получении гидрогелей, в раствор добавляют полимеры: КМЦ, гипан, крахмал. Тип солегелей определяется по наименованию аниона и катиона конденсированной соли (сульфатно-кальциевый солегель, силикатно-кальциевый солегель, алюмо-силикатный солегель) или по названию соли (например, гипсовый солегель).
Гидрогели и солегели при бурении соленосных отложений для максимально возможного снижения растворяющей способности промывочной жидкости насыщают солями одновалентных или двухвалентных металлов в зависимости от требуемой соли. В табл.4.2 приводится состав некоторых гидро- и солегелей, применяемых для бурения соленосных отложений.
К недостаткам гидрогелей и солегелей следует отнести высокую материалоемкость дефицитных материалов, что значительно повышает себестоимость промывочных жидкостей.
Таблица 4.2
