Контрольные тестовые задания
Тест № 1
1. Количество теплоты (кДж), поглощаемое при разложении 0,5 моль оксида углерода (IV) по уравнению реакции
СО2 (г) = С (т) + О2 (г) – 393,4 кДж,
равно …
1) 98,35 2) 196,7 3) 786,8 4) 8,96
2. Энтропия увеличивается в процессе …
1) замерзания воды 2) растворения соли в воде
3) 3Н2 (г) + N2 (г) = 2NН3 (г) 4) 2СО (г) + О2 (г) = 2СО2 (г)
3. Необходимым условием возможности осуществления химической реакции является …
1) увеличение энтальпии
2) увеличение энтропии
3) уменьшение энергии Гиббса
4) увеличение изобарно-изотермического потенциала
Тест № 2
1. Теплосодержание системы, в которой протекает экзотермическая реакция, в начальном состоянии …
1) больше, чем в конечном
2) меньше, чем в конечном
3) одинаково с конечным
2. Энтропия увеличивается в процессе …
1) Н2 (г) + Сl2 (г) = 2НСl (г)
2) превращения пара в жидкость
3) С (графит) + СО2 (г) = 2СО (г)
4) кристаллизации жидкости
3. Реакция 3С2Н2 (г) = С6Н6 (ж) ; ΔН < 0 возможна при …
1) высоких температурах
2) низких температурах
3) любой температуре
Тест № 3
1. Количество теплоты (кДж), выделяющееся при окислении 0,2 моль оксида мышьяка (III) по уравнению реакции
Аs2О3 (к) + О2 (г) = Аs2О5 (к) + 270,8 кДж, равно …
1) 135,4 2) 27,08 3) 54,16 4) 108,32
2. Энтропия увеличивается в процессе …
1) I2 (к) = I2 (г) 2) SО3 (г) + Н2О (ж) = Н2SО4 (ж)
3) Н2О (г) = Н2О (к) 4) N2 (г) + О2 (г) = 2NО (г)
3. При стандартных условиях термодинамически более устойчиво соединение…
1) Н2О (ΔG0298 = -229 кДж/моль)
2) Н2S (ΔG0298 = -34 кДж/моль)
3) Н2Sе (ΔG0298 = + 16 кДж/моль)
4) Н2Те (ΔG0298 = + 138 кДж/моль)
Тест № 4
1. Для экзотермической реакции энтальпия в начальном состоянии…
1) больше, чем в конечном
2) меньше, чем в конечном
3) такая же, как в в конечном
2. Последовательное увеличение энтропии происходит в ряду превращений…
1) Н2О (г) → Н2О (ж) → Н2О (т)
2) СО2 (г) → СО2 (т) → СО2 (г)
3) I2 (т) → I2 (ж) → I2 (г)
4) О2 (г) → О2 (ж) → О2 (г)
3. Из водородных соединений элементов VIА подгруппы
Н2О (г) Н2S (г) Н2Sе (г) Н2Те (г)
ΔG0298 (кДж/моль): -229 -34 + 71 + 138
непосредственно из простых веществ можно получить …
1) Н2Sе и Н2S 2) Н2О и Н2S
3) Н2Те и Н2S 4) Н2Sе и Н2О
Тест № 5
1. Для эндотермической реакции энтальпия в начальном состоянии …
1) больше, чем в конечном
2) такая же, как конечном
3) меньше, чем в конечном
2. Энтропия увеличивается в реакции …
1) Н2 (г) + Вr2 (г) = 2НВr (г) 2) Н2 (г) + Вr2 (ж) = 2НВr (г)
3) Н2 (г) + S (ромб.) = Н2S (г) 4) СО (г) + Н2 (г) = С (т) + Н2О (г)
3. Из галогеноводородов
НF (г) НСl (г) НВr (г) НI (г)
ΔG0298 (кДж/моль): -270 -95 -51 +1,8
непосредственно из простых веществ можно получить …
1) НСl и НI 2) НI и НВr
3) НF и НI 4) НСl и НВr
Тест № 6
1. Количество теплоты (кДж), выделяющееся при образовании 1 моль оксида мышьяка (V) по уравнению реакции
3Аs2О3 (к) + 2О3 (г) = 3Аs2О5 (к) + 1096,3 кДж,
равно …
1) 3288,9 2) 328,89 3) 548,15 4) 365,43
2. Энтропия идеально построенного кристалла при Т → 0 К стремится к …
1) – ∞ 2) 0 3) + ∞ 4) – 273
3. Реакция N2 (г) + 2О2 (г) = 2NО2 (г) ; ΔН > 0 термодинамически …
1) возможна при низких температурах
2) возможна при любых температурах
3) возможна при высоких температурах
4) не возможна
Тест № 7
1. Количество теплоты (кДж), выделяющееся при образовании 3 моль меди по уравнению реакции
2Сu2О (к) + Сu2S (к) = 6Сu (к) + SО2 (г) + 115,5 кДж, равно …
1) 57,75 2) 346,5 3) 11,55 4) 19,25
2. Энтропия увеличивается в случае фазового превращения …
1) Нg (ж) → Нg (г) 2) Вr2 (г) → Вr2 (ж)
3) I2 (ж) → I2 (к) 4) S (г) → S (ромб.)
3. При стандартных условиях термодинамически возможным является получение из простых веществ соединений набора …
1) Сl2О (г) (ΔG0298 = 93,4 кДж/моль)
СuО (к) (ΔG0298 = – 127,2 кДж/моль)
2) СаСl2 (к) (ΔG0298 = – 750,2 кДж/моль)
НСl (г) (ΔG0298 = – 95,3 кДж/моль)
3) С2Н4 (г) (ΔG0298 = 68,1 кДж/моль)
С2Н6 (г) (ΔG0298 = – 32,9 кДж/моль)
4) NО (г) (ΔG0298 = 86,7 кДж/моль)
NН3 (г) (ΔG0298 = 16,6 кДж/моль)
Тест № 8
1. Экзотермическая реакция выражается термохимическим уравнением …
1) А + В = С ; ΔН > 0
2) А + В + Q = С
3) А + В = С ; ΔН < 0
4) А + В = С – Q
2. Энтропия увеличивается в процессе …
1) 3О (г) = О3 (г) 2) 2НI (г) = I2 (г) + Н2 (г)
3) 1,5О2 (г) = О3 (г) 4) СаСО3 (к) = СаО (к) + СО2 (г)
3. Температура (К), при которой равновероятны оба направления реакции 2SО2 (г) + О2 (г) 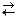 2SО3 (г) ; ΔН0 = -158 кДж, ΔS0 = - 0,189 кДж/К, равна …
2SО3 (г) ; ΔН0 = -158 кДж, ΔS0 = - 0,189 кДж/К, равна …
1) 836 2) 3416 3) 401 4) 2120
Тест № 9
1. Экзотермическая реакция выражается термохимическим уравнением …
1) А + В = С + Q 2) А + В + Q = С
3) А + В = С – Q 4) А + В = С ; ΔН > 0
2. Энтропия системы практически не изменяется в процессе …
1) I2 (г) + Н2 (г) = 2НI (г) 2) Н2 (г) + О2 (г) = Н2О2 (ж)
3) Сl2 (г) = 2Сl (г) 4) КСlО3 (г) = 2КСl (г) + 3О2 (г)
3. Температура (К), при которой равновероятны оба направления реакции N2 (г) + 3Н2 (г) 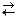 2NН3 (г) ; ΔН0 = -92,38 кДж, ΔS0 = –0,198 кДж/К, равна …
2NН3 (г) ; ΔН0 = -92,38 кДж, ΔS0 = –0,198 кДж/К, равна …
1) 92,182 2) 466,6 3) 2,1·10–3 4) 18,3
Тест № 10
1. Эндотермическая реакция выражается термохимическим уравнением …
1) А + В = С ; ΔS > 0 2) А + В = С ; ΔS < 0
3) А + В = С ; ΔН > 0 4) А + В = С ; ΔН < 0
2. Энтропия увеличивается в реакции …
1) СаО (к) + СО2 (г) = СаСО3 (к) 2) Аl2О3 (к) + 3SО3 (г) = Аl2(SО4)3 (к)
3) Н2 (г) + Вr2 (ж) = 2НВr (г) 4) С2Н4 (г) + Н2 (г) = С2Н6 (г)
3. Необходимым условием возможности осуществления химического процесса является …
1) увеличение энергии Гиббса в ходе реакции
2) увеличение энтальпии и уменьшение энтропии в ходе реакции
3) уменьшение энтропии в ходе реакции
4) уменьшение изобарно-изотермического потенциала
Тест № 11
1. При стандартных условиях теплота образования равна 0 для …
1) СаСО3 (к) 2) SО2 (г) 3) N2 (г) 4) СаО (т)
2. Для реакций:
NН3 (г) + НСl (г) = NН4Сl (к)
СН4 (ж) + 4Сl2 (г) = ССl4 (ж) + 4НСl (г)
энтропия соответственно …
1) практически не изменяется, увеличивается
2) уменьшается, практически не изменяется
3) практически не изменяется, уменьшается
4) увеличивается, уменьшается
3. Реакция N2 (г) + 2О2 (г) = 2NО2 (г) – Q …
1) невозможна ни при каких температурах
2) возможна при любых температурах
3) возможна при низких температурах
4) возможна при высоких температурах
Тест № 12
1. Для реакции 2Н2О2 = 2Н2О + О2 тепловой эффект рассчитывают по уравнению …
1) ΔН = 2ΔН0298, Н2О + ΔН0298, О2 – 2ΔН0298, Н2О2
2) ΔН = 2ΔН0298, Н2О + ΔН0298, О2 + 2ΔН0298, Н2О2
3) ΔН = ΔН0298, Н2О2 – 2ΔН0298, Н2О – ΔН0298, О2
4) ΔН = ΔН0298, Н2О + ΔН0298, О2 – ΔН0298, Н2О2
2. Энтропия уменьшается для реакции …
1) 3Fе (т) + 4Н2О (г) = Fе3О4 (т) + 4Н2 (г)
2) 2КСlО3 (т) = 2КСl (т) + 3О2 (г)
3) ВаО (т) + СО2 (г) = ВаСО3 (т)
4) АgNО3 (т) = Аg (т) + 1/2О2 (г) + NО2 (г)
3. Реакция возможна при любых температурах, если …
1) ΔН < 0, ΔS < 0 2) ΔН > 0, ΔS < 0
3) ΔН < 0, ΔS > 0 4) ΔН > 0, ΔS > 0
Тест № 13
1. Количество теплоты (кДж), необходимое для разложения 6 моль оксида серы (VI) по уравнению реакции
2SО3 (г) = 2SО2 (г) + О2 (г) ; ΔН = 197 кДж,
равно …
1) 32,8 2) 591 3) 65,7 4) 1182
2. В реакциях:
2Мg(NО3)2 (т) = 2МgО (т) + 4NО2 (г) + О2 (г)
РСl5 (г) = РСl3 (г) + Сl2 (г)
соответственно энтропия …
1) уменьшается, увеличивается
2) увеличивается, увеличивается
3) увеличивается, уменьшается
4) уменьшается, уменьшается
3. Реакция возможна, если при её протекании энергия Гиббса …
1) увеличивается
2) уменьшается
3) не изменяется
СПИСОК ЛИТЕРАТУРЫ
1. Ахметов Н. С. Общая и неорганическая химия. – 4-е изд. – М.: Высшая школа, 2002. – 743 с.
2. Глинка Н. Л. Общая химия / Под ред. А.И. Ермакова. – 30-е изд. – М.: Интеграл-пресс, 2002. – 727 с.
3. Глинка Н. Л. Задачи и упражнения по общей химии / Под ред. В. А. Рабиновича и Х. М. Рубиной. – 30-е изд. – М.: Интеграл-пресс, 2003. – 240 с.
4. Зайцев О. С. Задачи, упражнения и вопросы по химии. – М.: Химия, 1996. – 430 с.
5. Карапетьянц М. Х., Дракин С. И. Общая и неорганическая химия. – 3-е изд. – М.: Химия, 2000. – 592 с.
6. Коржуков Н. Г. Общая и неорганическая химия / Под ред. В. И. Деляна. – М.: МИСиС, 2004. – 512 с.
7. Слесарёв В.И. Химия. Основы химии живого. – С-Пб.: Химиздат, 2001. – 784 с.
ПРИЛОЖЕНИЕ
СТАНДАРТНЫЕ ЭНТАЛЬПИИ ОБРАЗОВАНИЯ 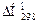 , ЭНТРОПИИ
, ЭНТРОПИИ 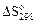 И ЭНЕРГИИ ГИББСА ОБРАЗОВАНИЯ
И ЭНЕРГИИ ГИББСА ОБРАЗОВАНИЯ 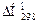
НЕКОТОРЫХ ВЕЩЕСТВ ПРИ 298 К (25 оС)
| Вещество | 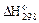 , кДж / моль , кДж / моль | 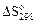 , Дж / (моль∙К) , Дж / (моль∙К) | 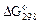 , кДж / моль , кДж / моль |
| Al2O3 (к) | –1676,0 | 50,9 | –1582,0 |
| С (графит) | 5,7 | ||
| ССl4 (ж) | –135,4 | 214,4 | –64,6 |
| СН4 (г) | –74,9 | 186,2 | –50,8 |
| С2Н2 (г) | 226,8 | 200,8 | 209,2 |
| С2Н4 (г) | 52,3 | 219,4 | 68,1 |
| С2Н6 (г) | –89,7 | 229,5 | –32,9 |
| С6Н6 (ж) | 82,9 | 269,2 | 129,7 |
| С2Н5ОН (ж) | –277,6 | 160,7 | –174,8 |
| С2Н12О6 (глюкоза) | –1273,0 | – | –919,5 |
| СО (г) | –110,5 | 197,5 | –137,1 |
| СО2 (г) | –393,5 | 213,7 | –394,4 |
| СаСО3 (к) | –1207,0 | 88,7 | –1127,7 |
| СаF2 (к) | –1214,6 | 68,9 | –1161,9 |
| Са3N2 (к) | –431,8 | 105,0 | –368,6 |
| Са(ОН)2 (к) | –986,6 | 76,1 | –896,8 |
| Cl2 (г) | 222,9 | ||
| Cl2О (г) | 76,6 | 266,2 | 122,3 |
| ClО2 (г) | 105,0 | 257,0 | 122,3 |
| Cl2О7 (ж) | 251,0 | – | – |
| Cr2О3 (к) | –1440,6 | 81,2 | –1050,0 |
| CuO (к) | –162,0 | 42,6 | –129,9 |
| FeO (к) | –264,8 | 60,8 | –244,3 |
| Fe2O3 (к) | –822,2 | 87,4 | –740,3 |
| Fe3O4 (к) | –1117,1 | 146,2 | –1014,2 |
| Н2 (г) | 130,5 | ||
| НBr (г) | –36,3 | 198,6 | –53,3 |
| НСN (г) | 135,0 | 113,1 | 125,5 |
| НСl (г) | –92,3 | 186,8 | –95,2 |
| НF (г) | –270,7 | 178,7 | –272,8 |
| НI (г) | 26,6 | 206,5 | 1,8 |
| НN3 (ж) | 294,0 | 328,0 | 238,8 |
| Н2О (г) | –241,8 | 188,7 | –228,6 |
| Н2О (ж) | –285,8 | 70,1 | –237,3 |
| Н2S (г) | –21,0 | 205,7 | –33,8 |
| КСl (к) | –435,9 | 82,6 | –408,0 |
Продолжение таблицы
| Вещество | 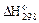 , кДж / моль , кДж / моль | 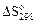 , Дж / (моль∙К) , Дж / (моль∙К) | 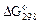 , кДж / моль , кДж / моль |
| КСlО3 (к) | –391,2 | 143,0 | –289,9 |
| MgCl2 (к) | –641,1 | 89,9 | –591,6 |
| Mg3N2 (к) | –461,1 | 87,9 | –400,9 |
| MgO (к) | –601,8 | 26,9 | –569,6 |
| N2 (г) | 191,5 | ||
| NН3 (г) | –46,2 | 192,6 | –16,7 |
| NН4NO2 (к) | –256,0 | – | – |
| NН4NO3 (к) | –365,4 | 151,0 | –183,8 |
| N2О (г) | 82,0 | 219,9 | 104,1 |
| NO (г) | 90,3 | 210,6 | 86,6 |
| N2О3 (г) | 83,3 | 307,0 | 140,5 |
| NО2 (г) | 33,5 | 240,2 | 51,5 |
| N2О4 (г) | 9,6 | 303,8 | 98,4 |
| N2О5 (к) | –42,7 | 178,0 | 114,1 |
| NiO (к) | –239,7 | 38,0 | –211,6 |
| О2 (г) | 205,0 | ||
| ОF2 (г) | 25,1 | 247,0 | 42,5 |
| Р2О3 (к) | –820,0 | 173,5 | – |
| Р2О5 (к) | –1492,0 | 114,5 | –1348,8 |
| PbO (к) | –219,3 | 66,1 | –189,1 |
| PbO2 (к) | –216,3 | 74,9 | –218,3 |
| SO2 (г) | –296,9 | 248,1 | –300,1 |
| SO3 (г) | –395,8 | 256,7 | –371,2 |
| SiСl4 (ж) | –687,8 | 239,7 | – |
| SiН4 (г) | 34,7 | 204,6 | 57,2 |
| SiO2 (кварц) | –910,9 | 41,8 | –856,7 |
| SnO (к) | –286,0 | 56,5 | –256,9 |
| SnO2 (к) | –580,8 | 52,3 | –519,3 |
| Ti (к) | 30,6 | ||
| ТiСl4 (ж) | –804,2 | 252,4 | –737,4 |
| ТiО2 (к) | –943,9 | 50,3 | –888,6 |
| WO3 (к) | –842,7 | 75,9 | –763,9 |
| ZnO (к) | –350,6 | 43,6 | –320,7 |
СОДЕРЖАНИЕ
1. Основные термины
2. Первый закон термодинамики
3. Понятие о самопроизвольных процессах. Энтропия
4. Второй закон термодинамики. Энергия Гиббса
5. Принцип энергетического сопряжения биохимических реакций
6. Особенности термодинамики в биохимических процессах в
равновесных и стационарных состояниях. Понятие о гомеостазе
Заключение
Контрольные задания
Типовые тестовые задания
Список литературы
Приложение
АГТУ. Заказ № . Тираж 50 экз. 2016 г.
[*] Система, от греч. Sistema– буквально, целое, составленное из частей
* Термин «теплосодержание», сохранивший исторически (под влиянием некогда господствовавшей в физике теории теплорода), может создать впечатление, что он характеризует просто «количество теплоты в теле» (в то время как в действительности теплосодержание – это мера энергии, накапливаемой веществом при его образовании). Поэтому в химической литературе вместо термина «теплосодержание» пользуются термином «энтальпия» (от греч. enthalpo – нагреваю).
* In vitro – вне организма, буквально в стекле.
* Конечным продуктом азотистого обмена в организме в действительности является не свободный азот, а такие продукты неполного сгорания, как мочевая кислота, мочевина, аммонийные соли, однако на практике принято вести расчёты, предполагая образование молекулярного азота.
* Пригожин Илья Романович – лауреат Нобелевской премии, бельгийский физик и физикохимик, один из создателей неравновесной термодинамики. Родился в Москве, вместе с родителями эмигрировал из России в 1920 г.
* Остеобласти (от греч. ostéon – кость и blastós – росток, зародыш) – клетки, синтезирующие материал волокон и основного вещества костной ткани и регулирующие поток ионов Са2+ в очагах костеобразования.
** Остеокласты (от osteo – кость и греч. kláo – ломаю, разбиваю) – костедробители, обычно многоядерные крупные клетки, разрушающие костную ткань.
* Эмбриогенез (от греч. émbrion – зародыш животных и человека и génesis – происхождение) – зародышевое развитие.
** Регенерация (от позднелат. regeneratio – возрождение, возобновление) – восстановление организмом утраченных или повреждённых органов и тканей. Термин предложен в 1712 г. французским естествоиспытателем Р. Реомюром.
