Природа и свойства электронных спектров
МИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательное
учреждение высшего профессионального образования
«Юго-Западный государственный университет»
(ЮЗГУ)
Кафедра органической и аналитической химии
УТВЕРЖДАЮ
Проректор по учебной работе
___________О. Г. Локтионова «_____» ____________2013 г.
СКАНИРОВАНИЕ И ОБРАБОТКА ЭЛЕКТРОННЫХ СПЕКТРОВ НА МНОГОЦЕЛЕВОМ СПЕКТРОФОТОМЕТРЕ «SHIMADZU» МОДЕЛИ «UV-1800» С РУЧНЫМ И ВНЕШНИМ УПРАВЛЕНИЕМ ОТ ЭВМ
Методические указания по выполнению лабораторной работы по дисциплине «Аналитической химия» для студентов 3 курса по направлению 020101.62 «Химия», 020201.65 «Фундаментальная и прикладная химия»; по дисциплине «Аналитическая химия и ФХМА» для студентов 2 курса по направлению 222900.62 «Нанотехнологии и микросистемная техника» и 240100.62 «Химическая технология» (профиль «Технология и переработка полимеров»)
Курск 2013
УДК 543.42
Составители: Н. А. Борщ, Л. А. Горбачева
Рецензент
Кандидат химических наук, доцент кафедры
«Физическая химия и химическая технология»
С. Д. Пожидаева
Сканирование и обработка электронных спектров на многоцелевом спектрофотометре «Shimadzu» модели «UV-1800» с ручным и внешним управлением от ЭВМ: методические указания по выполнению лабораторной работы по дисциплине «Аналитическая химия», «Аналитическая химия и ФХМА» / Юго-Зап. гос. ун-т; сост.: Н. А. Борщ, Л. А. Горбачева. Курск, 2013. 22 с.
Описана методика сканирования и обработки электронных спектров на многоцелевом спектрофотометре «Shimadzu» модели «UV-1800» с ручным и внешним управлением от ЭВМ. Приведены подробное описание эксперимента для подготовки образцов и рекомендации для интерпретации электронных спектров.
Предназначены для студентов, обучающихся по направлению 020101.62 «Химия»; 020201.65 «Фундаментальная и прикладная химия»; 222900.62 «Нанотехнологии и микросистемная техника»; 240100.62 «Химическая технология» (профиль «Технология и переработка полимеров»).
Текст печатается в авторской редакции
Подписано в печать Формат 60х84 1/16
Усл. печ. л. 1.28 Уч.-изд. л. 1.16 Тираж 30 экз. Заказ . Бесплатно.
Юго-Западный государственный университет.
305040, г. Курск, ул. 50 лет Октября, 94
ЦЕЛЬ РАБОТЫ:
1 Изучить принцип действия спектрофотометра «UV-1800» фирмы «Shimadzu» с ручным и внешним управлением от ЭВМ.
2 Ознакомиться с прикладной программойсканирования и обработки электронных спектров «UVProbe».
3 Приобрести навыки сканирования электронных спектров веществ.
4 Освоить методику определения параметров электронных спектров и отнесения полос поглощения по типу электронного перехода.
Оборудование: многоцелевой спектрофотометр «UV-1800», оснащенный интерфейсом для связи с ЭВМ, прикладная программа «UVProbe», принтер для печати отчета.
Условия проведения анализа: работа проводится в специализированной лаборатории спектроскопических методов анализа при наличии допуска к самостоятельной работе и спецодежды (белого халата) под наблюдением опытного лаборанта.
В аналитической химии наибольшее распространение получили спектрофотометрические методы анализа, основанные на поглощении в видимой области спектра (400-800 нм). Однако в последние годы спектрофотометрический метод химического анализа успешно развивается и для ультрафиолетовой области спектра. Количество методик, специально разработанных к условиям ультрафиолетовой области спектра, настолько возросло, так что в последнее время их объединили в отдельную группу методов – ультрафиолетовую спектрофотометрию. Появление этой группы методов обусловлено наличием у многих соединений наиболее сильных полос поглощения в УФ области спектра при строгой индивидуальности электронных спектров поглощения.
Природа и свойства электронных спектров
Электронным спектром вещества, поглощающего электромагнитные колебания в области 190-1100 нм, называют более или менее сплошную кривую зависимости оптической плотности D или молярного коэффициента поглощения e от длины волны l (или частоты u). Таким образом, спектр поглощения есть кривая вида D = f (l) с указанием толщины поглощающего слоя и концентрации истинной или формальной. Если состав и состояние равновесия вещества известны, тогда спектр поглощения выражают как функцию e = f (l). Большое значение имеет ширина полосы поглощения: чем шире полоса, тем труднее анализировать смесь нескольких соединений. Для количественной оценки используют понятие полуширины полосы поглощения α:
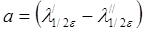 , которая для большинства молекул составляет 80-100 нм (рис. 1). Чем эта величина меньше, тем лучше.
, которая для большинства молекул составляет 80-100 нм (рис. 1). Чем эта величина меньше, тем лучше.
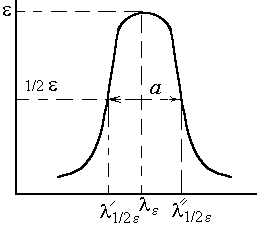 |
Рисунок 1 - Определение полуширины полосы поглощения в электронном спектре.
Возникновение электронных спектров, прежде всего, связано с перестройкой (возбуждением) электронной оболочки вещества, а не с движением ядер, как при возникновении колебательных спектров. Однако, особенности спектра, в частности форму контура полос, можно понять только с учетом движения и электронов, и ядер.
Формально природу электронных спектров можно охарактеризовать переходами вещества в различные энергетические состояния при поглощении кванта излучения с длиной волны l. Так как каждое вещество характеризуется своей системой энергетических уровней, то и спектры веществ располагаются как по числу полос, так и по их положению в шкале длин волн.
Другим важным свойством является интенсивность поглощения, что обусловлено характером перестройки электронной оболочки вещества. Чем больше изменяется дипольный момент вещества при возбуждении, тем интенсивнее полоса в спектре.
Электронные спектры можно классифицировать по типу энергетических уровней, между которыми происходит переход. Типы уровней, в свою очередь, определяются составом и строением вещества:
1. d-d*-, f-f*-спектры. Переходами между d- или f-орбиталями обусловлена окраска соединений переходных металлов. Эти переходы являются запрещенными по правилам отбора (маловероятны), поэтому соответствующие полосы в спектрах малоинтенсивные:e находится в пределах 10 – 103.
2. p-p*-спектры возникают в молекулах с сопряженными двойными связями. Интенсивность полос может достигать значений e = 105. Окраска большинства красителей обусловлена такими переходами.
3. n-p*-переходы возникают в молекулах с сопряженными связями, которые совершают гетероатомы с не поделенными парами электронов (n-электроны). Природу этих спектров характеризует возбуждение электронов не поделенной пары на вакантный p*-уровень. Такие переходы запрещены, поэтому соответствующие полосы в спектрах малоинтенсивны.
4. Полосы переноса заряда. Систему уровней молекулярных комплексов, например, йода с бензолом, можно считать лишь слегка возмущенным взаимодействием. В этом случае окраска обусловлена переносом электронов с верхнего занятого уровня молекулы донора (бензола) на свободный анти связывающий уровень молекулы акцептора –йода. Можно рассматривать такой переход как перенос заряда. Полосы переноса заряда, как правило, достаточно интенсивны: e = 103-104.
