Кинетика химической реакций. Химическое равновесие. Катализ.
Химический эквивалент.
1. Эквивалент оксида натрия Na2O равен:
1. 1 моль
2. 2 моль
3. 1/2 моль
4. 1/3 моль
5. 1/4 моль
2. Молярная масса эквивалента оксида серы (VI) SO3 равна:
1. 26,67 г/моль
2. 80 г/моль
3. 5,33 г/моль
4. 13,33 г/моль
5. 16 г/моль
3. Эквивалент оксида азота (V) N2O5 равен:
1. 1/2 моль
2. 1/5 моль
3. 1/7 моль
4. 1/10 моль
5. 2 моль
4. Эквивалент оксида свинца (IV) PbO2 равен
1. 1 моль
2. 1/2 моль
3. 2 моль
4. 1/3 моль
5. 1/4 моль
5. По формуле f = 1/(nּB), где n - число атомов металла; В – валентность металла, определяют эквивалент
1. кислоты
2. основания
3. окислителя
4. восстановителя
5. соли
6. Молярная масса эквивалента серной кислоты Н2SO4 равна
1. 98 г/моль
2. 30 г/моль
3. 49 г/моль
4. 16 г/моль
5. нет правильного ответа
7. Эквивалент кислоты вычисляют по формуле fэ = 1/n, где символ «n» обозначает
1. число атомов элемента-кислотообразователя
2. основность кислоты
3. валентность кислотного остатка,
4. число принятых или отданных электронов
5. число атомов кислорода в молекуле кислоты
8. По формуле: fэ = 1/n, где n - основность кислоты, определяют эквивалент:
1. кислоты
2. соли
3. основания
4. окислителя
5. восстановителя
9. Эквивалент элемента азот в соединении NH3 равен:
1. 1 моль
2. 3 моль
3. 1/3 моль
4. 17 моль
5. 14/3 моль
10. Химический эквивалент вещества имеет размерность
1. моль/л
2. моль
3. г/моль
4. г/мл
5. моль/кг
11. В уравнении реакции Са(ОН)2 + НСl = Са(ОН)Сl + Н2О эквивалент гидроксида кальция равен:
1. 1/2 моль
2. 1 моль
3. 37 г/моль
4. 74 г/моль
5. 2 моль
12. В уравнении реакции H3PO4 + 2KOH = K2HPO4 + 2H2O эквивалент фосфорной кислоты равен:
1. 1/3 моль/л
2. 1/2 моль/л
3. 1 моль
4. 33 г/моль
5. 49 г/моль
13. В уравнении Н3РО4 + КОН = КН2РО4 + Н2О эквивалент фосфорной кислоты равен
1. 1/ 3 моль
2. 1/ 2 моль
3. 1 моль
4. 98 г/моль
5. 32,6 г/моль
14. В уравнении Н3РО4 + КОН = КН2РО4 + Н2О эквивалент гидроксида калия равен
1.1/ 3 моль
2.1/ 2 моль
3. 1 моль
4. 98 г/моль
5. 32,6 г/моль
15. По уравнению реакции Н2СО3 + КОН = КНСО3 + Н2О эквивалент угольной кислоты составляет:
1. 62 г/моль
2. 31 г/моль
3. 1 моль
4. 1/2 моль
5. 2 моль
16. Количество вещества, которое в химических реакциях соединяется с 1 моль атомов водорода или замещает 1 моль атомов (ионов) водорода в соединениях, называется
1. молекулой вещества
2. массой вещества
3. химическим элементом
4. химическим эквивалентом вещества
5. титром раствора
4.
17. Укажите, от какого фактора зависит эквивалент химического элемента
1. от температуры
2. от атмосферного давления
3. от осмотического давления
4. от валентности элемента в соединении
5. от присутствия катализатора
4.
18. По формуле fэ = 1/(nּВ) , где n – кислотность основания, определяет эквивалент:
1. кислоты
2. основания
3. окислителя
4. восстановителя
5. соли
Концентрация растворов
1. Моляльная концентрация - это отношение количества вещества (моль)
1. к массе растворителя, кг
2. к количеству раствора, моль
3. к количеству растворителя, моль
4. к объему раствора, л
5. к объему растворителя, мл
2. Единица измерения молярной концентрации эквивалента вещества:
1. моль
2. г/моль
3. моль/л
4. г/мл
5. моль/кг
3. Концентрация показывающая, сколько граммов растворенного вещества содержится в 1 мл раствора, называется:
1. массовой долей растворенного вещества в растворе
2. титром
3. процентной концентрацией
4. молярной концентрацией
5. молярной концентрацией эквивалента
4. Молярная концентрация - это отношение количества вещества (моль)
1. к массе раствора, кг
2. к массе растворителя, кг
3. к количеству растворителя, моль
4. к объему раствора, л
5. к объему растворителя, мл
5. Смешали 5 г соли и 45 г воды. Массовая доля соли в полученном растворе составляет:
1. 5%
2. 10%
3. 45%
4. 9%
5. 11,1%
6. Смешали 10 г сахара и 40 г воды. Массовая доля сахара в полученном растворе составляет:
1. 10%.
2. 40%.
3. 2,5%.
4. 4%.
5. 20%.
7. В 250 мл раствора содержится 5 г хлороводорода НCl. Титр этого раствора равен
1. 0,02 г/мл
2. 5 г/мл
3. 7,3 г/мл
4. 0,028 г/мл
5. 0,365 г/мл
8. Количество вещества (моль) в 1 кг растворителя показывает:
1. молярная концентрация
2. молярная концентрация эквивалента
3. процентная концентрация
4. моляльная концентрация
5. массовая доля вещества
9. Раствор, который находится в динамическом равновесии с избытком растворенного вещества, называется
1. буферным
2. изотоническим
3. пересыщенным
4. ненасыщенным
5. насыщенным
10. В 50 мл раствора содержится 0,5 г азотной кислоты. Титр этого раствора равен
1. 0,01 г/мл
2. 2,00 г/мл
3. 0,63 г/мл
4. 1,26 г/мл
5. 0,0001 г/мл
11. Величина, равная отношению массы растворенного вещества к общей массе раствора - это
1. массовая доля растворенного вещества
2. молярная концентрация вещества
3. моляльная концентрация эквивалента
4. титр раствора
5. молярная доля растворенного вещества
12. Раствор, который содержит очень малое количество растворенного вещества по сравнению с количеством растворителя, называется
1. концентрированным
2. насыщенным
3. буферным
4. изотоническим
5. разбавленным
13. Единица измерения молярной концентрации вещества:
1. г/моль
2. моль
3. г/мл
4. моль/л
5. моль/кг
14. Число эквивалентов растворенного вещества, содержащееся в 1 литре раствора, называется:
1. титром раствора
2. процентной концентрацией
3. молярной концентрацией
4. молярной концентрацией эквивалента
5. эквивалентом вещества
15. Эквивалентная концентрация – это отношение количества моль эквивалента растворенного вещества к
1. Массе раствора, кг
2. Объёму раствора, л
3. Количеству растворителя, моль
4. Массе растворителя, кг
5. Объему растворителя, мл.
16. Титр раствора определяется как:
1. отношение массы растворенного вещества к массе раствора
2. количество растворенного вещества в 1 литре раствора
3. количество эквивалентов растворенного вещества в 1 литре раствора
4. количество граммов растворенного вещества в 1 мл раствора
5. количество вещества в 1 кг растворителя
17. Раствор серной кислоты, в 200 мл которого содержится 4,90 г вещества Н2SO4, имеет молярную концентрацию эквивалента равную:
1. 0,50 моль/л
2. 0,25 моль/л
3. 0,20 моль/л
4. 0,0005 моль/л
5. 0,00025 моль/л
18. Смешали 30г. Сахара и 180г. Воды. Массовая доля сахара в полученном растворе составляет:
1.14%
2.20%
3.90%
4.9%
5.11.1%
19. Масса 0,2 эквивалента гидроксида натрия составляет:
1.40 г.
2.8.0 г.
3.2.3 г.
4.1.7 г.
5.нет правильного ответа
20. Масса 0,01 эквивалента азотной кислоты составляет:
1.63 г.
2.0.63 г.
3.1,4 г.
4.21 г.
5. нет правильного ответа
21. В 100 мл раствора содержится 4г. Хлорида натрия. Титр этого раствора равен:
1.0,04 г/мл
2.0,002 г/мл
3.50 г/мл
4. 0,585 г/мл
5. нет правильного ответа
22. В 500мл раствора содержится 20г. гидроксида натрия. Титр этого раствора равен:
1.0,04 г/мл
2.2,50 г/мл
3.1 г/мл
4.0,8 г/мл
5. нет правильного ответа.
23. В 8 0 мл раствора 0.8 г. азотной кислоты. Титр этого раствора равен:
1.0,01 г/мл
2.1 г/мл
3.0,63 г/м
4.1,26 г/мл
5. нет правильного ответа.
24. В 250 мл раствора содержится 15г хлороводорода НCl . Титр этого раствора равен:
1.5 г/мл
2.0,06г/мл
3.7,3 г/мл
4.0,028 г/мл
5. нет правильного ответа.
25. Масса вещества, необходимая для приготовления раствора заданной молярной концентрации, рассчитывается по формуле:
1. m = CּMּV
2. m = m(раствора)ּ100%
3. m = 1000ּT
4. 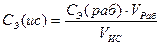
5. 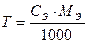
Химическая термодинамика
1. Термодинамический параметр энтропия измеряется в единицах:
1. Дж
2. кДж
3. кДж/моль
4. Дж/(моль·К)
5. моль/(л·сек)
2. Система, в которой отдельные части отделены друг от друга видимой поверхностью раздела и отличаются по свойствам, называется:
1. изолированной
2. открытой
3. закрытой
4. гомогенной
5. гетерогенной
3. Однородная часть системы с одинаковыми химическими и термодинамическими свойствами, отделенная от других частей поверхностью раздела, при переходе через которую физические и химические свойства резко меняются, называется:
1. параметром
2. энтропией
3. энтальпией
4. компонентом
5. фазой
4. Тепловой эффект реакции зависит только от природы и состояния исходных веществ и конечных продуктов, но не зависит от пути, по которому реакция протекает, - это
1. закон действующих масс
2. второе начало термодинамики
3. закон Гесса
4. закон Лавуазье-Лапласа
5. третье начало термодинамики
5. Химические уравнения, в которых указано агрегатное состояние веществ и тепловой эффект реакции, называются:
1. изохорными
2. изобарными
3. изотермическими
4. термохимическими
5. изобарно-изотермическими
6. Изменение любого из термодинамических параметров, описывающих состояние термодинамической системы, называется:
1. внутренней энергией
2. термодинамическим процессом
3. термодинамикой
4. термодинамической системой
5. открытой термодинамической системой
7. Наибольшее значение энтропия вещества имеет в агрегатном состоянии:
1. жидком
2. газообразном (парообразном)
3. твердом
4. в правильном кристалле при температуре абсолютного нуля
5. энтропия вещества постоянна, не зависит от агрегатного состояния
8. Фазовый переход вещества из жидкого состояния в пар называется:
1. плавлением
2. кристаллизацией
3. конденсацией
4. парообразованием
5. сжижением
9. Самопроизвольно могут протекать химические процессы, при которых изменение энергии Гиббса (дельта G):
1. имеет положительное значение
2. имеет отрицательное значение
3. равно нулю, дельта G = 0.
4. дельта G = 0 и энтропия уменьшается
5. дельта G > 0 и энтропия уменьшается
10. Единица измерения стандартных параметров «энтальпия» и «энергия» Гиббса в системе СИ (при стандартных условиях):
1. кДж, Дж, ккал, кал
2. кДж/моль
3. ккал/моль, кал/моль
4. моль/л/сек
5. моль/л
11. Химическая реакция, при которой энтальпия системы повышается, называется:
1. экзотермической
2. эндотермической
3. каталитической
4. реакцией обмена
5. окислительно-восстановительной
12. Тепловую энергию полностью в работу превратить нельзя, часть теплоты обязательно расходуется на нагревание окружающей среды. Это одна из формулировок:
1. периодического закона Д.И. Менделеева
2. первого начала термодинамики
3. 2-го начала термодинамики
4. закона действующих масс
5. закона постоянства состава вещества
13. Возможность протекания эндотермических реакций с повышением температуры
1. уменьшается
2. не изменяется
3. увеличивается
4. становится равной нулю
5. зависит от рН среды
14. кДж/(моль.град) - это единица измерения термодинамического параметра
1. внутренняя энергия
2. энтальпия
3. энтропия
4. энергия Гиббса
5. нет правильного ответа
15. Термодинамическая система, которая не обменивается с окружающей средой ни веществом, ни энергией, называется
1. открытой
2. живым организмом
3. закрытой
4. изолированной
5. гомогенной
16. Химическая реакция, при которой энтальпия и внутренняя энергия системы уменьшаются, называется:
1. экзотермической
2. каталитической
3. ферментативной
4. эндотермической
5. реакцией гидролиза
17. При стандартных условиях реакция: I2 + H2 = 2HI, для которой дельта G = +37 кДж:
1. находится в состоянии термодинамического равновесия
2. находится в стационарном состоянии
3. может протекать самопроизвольно в прямом направлении
4. не может протекать самопроизвольно
5. нет правильного ответа
18. Не проводя расчета, определите, как изменяется энтропия в химической реакции: N2O4(г) = 2NO2(г)
1. увеличивается
2. уменьшается
3. не изменяется
4. сначала уменьшается, затем увеличивается
5. становится равной нулю
19. Не производя расчеты, определите, как изменяется энтропия в химической реакции: CaO(т) + CO2 (Г) = CaCO3 (т)
1. увеличивается
2. уменьшается
3. не изменяется
4. сначала увеличивается, затем уменьшается
5. энтропия любой т/д системы всегда равна 0.
20. Математическая запись дельта НХ.Р. = S дельта Нобр.(продуктов) - S дельта Нобр.(исходн.) соответствует
1. Первому закону Рауля
2. Второму закону Рауля
3. Третьему закону Рауля
4. Первому следствию из закона Гесса
5. Правилу Вант-Гоффа
21. Наука, которая устанавливает связь между различными видами энергии, изучает возможность, направленность и пределы самопроизвольно текущих процессов, называется:
1. термодинамикой
2. кинетикой
3. аналитической химией
4. физической химией
5. физиологической химией
22. Химическая реакция, при которой внутренняя энергия системы повышается, а теплота поглощается, называется:
1. экзотермической
2. эндотермической
3. окислительно-восстановительной
4. каталитической
5. ферментативной
23. Термодинамическая система, которая обменивается с окружающей средой и веществом, и энергией, называется:
1. изолированной
2. закрытой
3. гетерогенной
4. открытой
5. гомогенной
24. Теплота, которая поглощается или выделяется при образовании 1 моль химического соединения из простых веществ при стандартных условиях называется теплотой:
1. разложения
2. сгорания
3. растворения
4. образования
5. сублимации
25. Теплота, которая поглощается или выделяется при разложении 1 моль химического соединения на простые вещества при стандартных условиях, называется теплотой:
1. образования
2. растворения
3. кристаллизации
4. разложения
5. плавления
26. Теплота, которая выделяется при сгорании 1 моль вещества при стандартных условиях, называется теплотой:
1. образования
2. разложения
3. растворения
4. сгорания
5. плавления
27. В изолированной системе все самопроизвольные процессы протекают в сторону:
1. уменьшения беспорядка в системе
2. уменьшения энтропии
3. увеличения рН раствора
4. уменьшения рН раствора
5. увеличения энтропии
28. Одновременное влияние энтальпийного и энтропийного факторов на термодинамический процесс выражается изменением:
1. давления
2. объёма
3. температуры
4. энергии Гиббса
5. внутренней энергии
29. Возможность протекания эндотермических реакций с понижением температуры:
1. уменьшается
2. не изменяется
3. увеличивается
4. становится равной нулю
5. зависит от рН
30. Не производя расчета, определите, как изменится энтропия системы при растворении кристаллов KNO3 в воде? KNO3 (т) ↔ K+(р-р) + NO-3 (р-р)
1. увеличивается
2. уменьшается
3. не изменяется
4. сначала уменьшается, затем увеличивается
5. энтропия любой термодинамической системы всегда равна 0.
Кинетика химической реакций. Химическое равновесие. Катализ.
1. Если на систему, находящуюся в равновесии оказать внешнее воздействие - изменить температуру Т, концентрацию С, давление Р, то равновесие сместится в сторону ослабления оказанного воздействия. Это:
1. закон сохранения массы веществ
2. закон действующих масс
3. закон сохранения энергии
4. закон Гесса
5. принцип Ле Шателье
2. Вещества, небольшие количества которых сильно замедляют скорость химической реакции, называются:
1. ингибиторами
2. индикаторами
3. ферментами
4. промоторами
5. каталитическими ядами
3. По своей природе ферменты (энзимы) - это:
1. только углеводы простые и сложные
2. только сложные неорганические соединения
3. простые и сложные неорганические соединения
4. специфические простые и сложные белки
5. только простые белки
4. При химическом равновесии длительно остаются постоянными в системе:
1. давление
2. температура
3. концентрация исходных веществ
4. концентрация продуктов
5. температура, давление и концентрация всех веществ
5. На скорость реакции, протекающей в жидкой фазе, не влияет
1. концентрация реагирующих веществ
2. температура
3. природа реагирующих веществ
4. присутствие катализатора
5. давление
6. Если катализатор и реагирующие вещества находятся в разных фазах, то катализ называется
1. независимым
2. гетерогенным
3. автокатализом (ускоряются по мере накопление продуктов, является kat)
4. гомогенным
5. коллоидным
7.Снижение скорости ферментативной реакции при достижении определенной температуры объясняется
1. высокой каталитической активностью фермента
2. высокой селективностью фермента
3. тепловой денатурацией ферментов, т.е. их инактивацией
4. амфотерными свойствами белка
5. зависимостью скорости реакции от концентрации субстрата
8. Число молекул, участвующих в простой реакции или элементарном акте, характеризует
1. константу скорости реакции
2. число стадий реакции
3. порядок реакции
4. вид реакции
5. молекулярность реакции
9. Изменение молярной концентрации реагирующих веществ или продуктов реакции в единицу времени называется
1. точка конца титрования
2. эквивалентной точкой
3. фазовым равновесием
4. скоростью химической реакции
5. обратимой реакцией
10. Температурный коэффициент для биохимических процессов имеет значение
1. от 2 до 4.
2. равен 273.
3. от 10 в степени (-9) м до 10 в степени (-7) м
4. от 7 до 9.
5. равен 22,4.
11. Неустойчивое состояние реагирующих веществ, когда старые связи еще полностью не разрушены, а новые связи еще не образовались, называется
1. активированным комплексом (переходным состоянием)
2. комплексным соединением
3. комплексоном III
4. энергией активации
5. химическим равновесием
12. Величина, показывающая какая часть взятых веществ вступает в реакцию в единицу времени – это:
1. эбуллиоскопическая константа
2. криоскопическая константа
3. константа равновесия
4. константа скорости
5. универсальная газовая постоянная
13. Реакции, протекающие в несколько стадий- это реакции
1. простой
2. сложной
3. гомогенной
4. гетерогенной
5. медленной
14. До конца, до полного израсходования реагирующих веществ, не идут реакции
1. простые
2. сложные
3. необратимые
4. каталитические
5. обратимые
15. Реакции, которые протекают в одну стадию - это реакции:
1. простые
2. сложные
3. необратимые
4. обратимые
5. каталитические
16. При повышении температуры на каждые 10 градусов скорость химической реакции увеличивается в 2-4 раза, это -
1. Закон Гесса
2. Принцип Ле Шателье
3. Правилофаз Гиббса
4. Правило Вант-Гоффа
5. Закон действующих масс
17 В уравнении Аррениуса К = Ае-Еа/RT , величина А - стерический или пространственный фактор, который характеризует
1. долю активных соударений
2. температуру системы
3. энергию активации
4. геометрическую конфигурацию реагирующих молекул
5. внутреннюю энергию системы
18. Для реакции СаO(к) + СО2(г) « СаСО3(к) выражение константы равновесия соответствует записи
1. 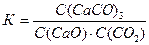
2. 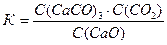
3. 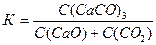
4. 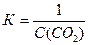
5. К = С(СО2)
19. Реакции второго порядка соответствует кинетическое уравнение
1.v=kС
2. v=к
3. v=kР
4. v= kСА.СВ
5. v=kC3
20. Математическое выражение закона действующих масс для реакции протекающих по уравнению: mA+nB=C
1. 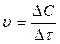
2. 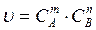
3. 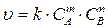
4. 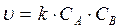
5. 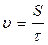
5. Коллигативные свойства растворов
1. Односторонняя диффузия растворителя через полупроницаемую мембрану из раствора с меньшей концентрацией в раствор с большей концентрацией - это:
1. коагуляция
2. желатинирование
3. буферное действие
4. буферная емкость
5. осмос
2. На сколько градусов понизится температура замерзания раствора, если в 1 кг растворителя растворить 1 моль вещества, показывает
1. криометрическая константа
2. эбулиометрическая константа
3. изотонический коэффициент
4. газовая постоянная
5. степень диссоциации
3. Длительное время изолированные органы организма и отдельные клетки могут сохраняться:
1. в гипертоническом растворе
2. в гипотоническом растворе
3. в физиологическом растворе
4. в любом буферном растворе
5. в растворе любого сильного электролита
4. При одинаковой моляльной концентрации самую высокую температуру кипения имеет раствор
1. анилина
2. глюкозы
3. хлорида кальция
4. сахарозы
5. все растворы имеют одинаковую температуру кипения
5. Для очищения раны от гноя, микроорганизмов и продуктов распада, в хирургии применяются
1. гипотонические растворы
2. изотонические растворы
3. физиологический раствор
4. гипертонические растворы
5. нет правильного ответа
6. При помещении клетки крови (эритроцита) в гипертонический раствор наблюдается явление сморщивания клетки, которое называется
1. гемолизом
2. плазмолизом
3. желатинированием
4. катализом
5. коагуляцией
7. Используемые в качестве слабительного средства соли MgSO4 и Na2SO4 применяются в виде:
1. гипотонических растворов
2. гипертонических растворов
3. изотонических растворов
4. физиологических растворов
5. гипотонических и физиологических растворов
8. При одинаковой температуре будут замерзать водные растворы с одинаковой молярной концентрацией вещества:
1. глицерин и сульфат натрия
2. сульфат натрия и глюкоза
3. глицерин и глюкоза
4. глюкоза и гидроксид калия
5. глюкоза и сульфат калия
9. Растворимость газов в растворах электролитов всегда меньше, чем в чистом растворителе. Это закон:
1. Генри
2. Сеченова
3. Вант-Гоффа
4. Рауля
5. Менделеева
10. Два раствора, имеющие одинаковые концентрации и одинаковое осмотическое давление, называются
1. буферными
2. гипотоническими
3. гипертоническими
4. изотоническими
5. физиологическими
11. Метод исследования, основанный на измерении понижения температуры замерзания растворов, называется:
1. осмометрия
2. криометрия
3. эмбулиометрия
4. изоосмия
5. рН-метрия
12. При помещении клетки крови (эритроцита) в гипотонический раствор наблюдается разрыв оболочки клетки и образование раствора «лаковой» крови - это явление называется
1. гемолизом
2. плазмолизом
3. желатинированием
4. катализом
5. коагуляцией
13. В организм человека можно вводить в больших количествах:
1. только гипотонические растворы
2. только гипертонические растворы
3. только изотонические растворы
4. гипотонические, гипертонические и изотонические растворы
5. гипотонические и гипертонические
14. Экзосмос эритроцита приводит к явлению, которое называется:
1. гемолизом
2. плазмолизом
3. тургором
4. желатинированием
5. коагуляцией
15. При одинаковой молярной концентрации и одинаковой температуре изотоническими будут водные растворы:
1. поваренной соли, сахара
2. глюкозы, азотной кислоты
3. гидроксида калия, уксусной кислоты
4. хлорида калия, глицерина
5. глюкозы, сахара, глицерина
16. Метод исследования, основанный на измерении осмотического давления растворов, называется
1. криометрия
2. эбулиометрия
3. изоосмия
4. осмометрия
5. кислотно-основное титрование
17. Раствор изотонический плазме крови называется
1. гипертоническим
2. гипотоническим
3. буферным
4. физиологическим
5. каталитическим
18. Криометрическая константа растворителя зависит от:
1.природы растворенного вещества
2.природы растворителя
3.от концентрации растворенного вещества
4.температуры раствора
5.природы и концентрации растворенного вещества
19. Отношение повышения температуры кипения раствора электролита к повышению температуры кипения раствора не электролита такой же концентрации называется
1. константой диссоциации
2. электродным потенциалом
3. водородным показателем
4. изотоническим коэффициентом
5. электропроводностью раствора
20. Самопроизвольный процесс выравнивания концентрации вещества в растворе за счет теплового движения молекул - это:
1. коагуляция
2. осмос
3. диффузия
4. желатинирование
5. концентрация
21. Растворы различных не электролитов с одинаковой молярной концентрацией имеют:
1. одинаковую молярную массу веществ
2. одинаковое осмотическое давление
3. одинаковую скорость диффузии молекул
4. различное осмотическое давление
5. одинаковую изоэлектрическую точку
22. Стандартный раствор глюкозы имеет концентрацию 0,02 моль/л. По отношению к этому раствору изотоническим будет раствор с концентрацией глюкозы
1. 0,04 моль/л
2. 0,05 моль/л
3. 0,10 моль/л
4. 0,02 моль/л
5. 0,01 моль/л
23. Если степень диссоциации электролита равна 1 и изотонический коэффициент равен 2. то электролит диссоциирует
1. на 3 иона
2. на 2 иона
3. на 4 иона
4. на 5 ионов
5. не диссоциирует
24. Если степень диссоциации электролита равна 0,9, то изотонический коэффициент раствора соли NaNO3 равен:
1. 1,0.
2. 2,0.
3. 2,1.
4. 1,8.
5. 1,9.
25.Осмотическая концентрация веществ в крови лягушки составляет 0,22 моль/л. Если R = 0,082 (л.атм)/(град.моль), то при 7 градусах С осмотическое давление крови лягушки равно
1. 5,05 атм.
2. 2,85 атм.
3. 0,13 атм.
4. 7,77 атм.
5. нет правильного ответа
22. Неустойчивое состояние реагирующих веществ, когда старые связи еще
полностью не разрушены, а новые связи еще не образовались, называется
1. активированным комплексом (переходным состоянием)
2. комплексным соединением
3. комплексоном III
4. энергией активации
5. химическим равновесием
23. Раздел химии, изучающий законы и механизм протекания химических
реакций, влияние внешних условий на них, называется:
1. аналитической химией
2. химическим эквивалентом
3. химической термодинамикой
4. химической кинетикой
5. физической химией
24. Скорость реакции от концентрации реагирующих веществ находится
1. в прямо пропорциональной зависимости
2. в обратно пропорциональной зависимости
3. не зависит
4. находится в зависимости от суммы концентраций
5. находится в зависимости от разности концентраций
25. Вещества, небольшие количества которых сильно замедляют скорость
химической реакции, называются:
1. ингибиторами
2. индикаторами
3. ферментами
4. промоторами
5. каталитическими ядами
26. Энергия, необходимая для перевода 1 моль неактивных молекул в активное
состояние, называется:
1. внутренней энергией
2. свободной энергией
3. энергией Гиббса
4. энергией активации
5. нет правильного ответа
Буферные растворы
1. Карбонатный буфер состоит из смеси:
1. угольной кислоты и гидрокарбоната натрия
2. угольной кислоты и карбоната натрия
3. угольной и уксусной кислоты
4. гидрокарбоната и карбоната натрия
5. гидрофосфата и дигидрофосфата калия
2. Числом моль-эквивалентов сильной кислоты или щелочи, которое надо добавить к 1 л буферного раствора, чтобы изменить его рН на единицу, определяется:
1. рН буферной системы
2. буферная емкость раствора
3. механизмы буферного действия раствора
4. резервная щелочность крови
5. изоэлектрическое состояние белка
3. Буферным раствором, состоящим из слабого основания и его соли от сильной кислоты, является:
1. ацетатный буфер
2. гемоглобиновый буфер
3. аммонийный буфер
4. оксигемоглобиновый буфер
5. карбонатный буфер
4. При добавлении к буферному раствору небольшого количества сильной кислоты его рН
1. не изменяется
2. уменьшается
3. увеличивается
4. сначала увеличивается, затем становится равным 7.
5. нет правильного ответа
5. При добавлении к белковому буферу дистиллированной воды его рН:
1. увеличивается
2. уменьшается
3. не изменяется
4. становится равным нулю
5. всегда становится равным 7.
6. В норме рН крови имеет значение от 7,36 до 7,40. При ацидозе рН крови:
1. смещается в кислую сторону (рН < 7,36).
2. смещается в щелочную сторону (рН > 7,40).
3. находится в пределах от 7,36 до 7,40.
4. смещается в щелочную сторону до рН = 9.
5. нет правильного ответа
7. рК угольной кислоты равен 6,35. При смешивании равных объемов компонентов рН гидрокарбонатного буфера равен 6,35, если концентрация соли
1. больше концентрации кислоты
2. в 10 раз больше концентрации кислоты
3. меньше концентрации кислоты
4. равна концентрации кислоты
5. в 10 раз меньше концентрации кислоты
8. При добавлении к ацетатному буферу дистиллированной воды его буферная емкость:
1. уменьшается
2. не изменяется
3. увеличивается
4. становится равной нулю
5. соответствует рН = 7.
9. При алкалозе резервная щелочность крови
1. не изменяется
2. увеличивается
3. уменьшается
4. сначала уменьшается до рН = 7, затем увеличивается
5. соответствует рН = 1.
10. Укажите ряд, в котором перечислены только белковые буферные системы
1. аммонийный, гемоглобиновый буфер
2. аминокислотный и ацетатный буфер
3. аммонийный, ацетатный и фосфатный буферы
4. гемоглобиновый, оксигемоглобиновый и белковый буферы
5. белковый, фосфатный, ацетатный буферы
11. При добавлении к буферному раствору небольшого количества щелочи его рН
1. уменьшается
2. не изменяется
3. увеличивается
4. становится равным нулю
5. становится равным 7.
12. При ацидозе щелочной резерв крови по сравнению с нормой
1. увеличен
2. уменьшен
3. находится в норме
4. соответствует рН = 10.
5. сначала увеличивается до рН = 10, затем уменьшается
13. Бикарбонатная буферная система состоит из смеси
1. угольной кислоты и гидрокарбоната натрия
2. угольной кислоты и карбоната натрия
3. гидрокарбоната и карбоната натрия
4. гидрокарбоната и гидрофосфата натрия или калия
5. карбоната и фосфата натрия или калия
14. Резервная щелочность крови у человека в норме составляет
1.10-15 объемных % СО2.
2. 90-100 объемных % СО2.
3. 20-35 объемных % СО2.
4. 0,90% хлорида натрия
5. 50-65 объемных % СО2.
15. рН буферного раствора зависит:
1. от температуры, природы компонентов буферного раствора и соотношения концентрации компонентов
2. только от концентрации компонентов буферного раствора
3. от концентрации кислоты
4. от концентрации соли
5. от концентрации основания
16. 75% буферной емкости крови составляет:
1. ацетатный буфер
2. ацетатный и аммонийный буфер
3. аммонийный буфер
4. гемоглобиновый и оксигемоглобиновый буферы
5. гемоглобиновый и ацетатный буферы
17. Если в растворе С(Н+) < C(ОН-), то реакция среды этого раствора
1. буферная
2. кислая
3. щелочная
4. нейтральная
5. положительная
18. Свойство растворов сохранять постоянство концентрации ионов водорода (рН) при добавлении небольших количеств кислоты или щелочи, а также при разбавлении, называется:
1. буферной емкостью
2. буферным действием или буферностью
3. каталитическим действием или катализом
4. плазмолизом
5. гемолизом
19. При добавлении к аммонийному буферу соляной кислоты образуется эквивалентное количество:
1. сильной кислоты
2. слабой кислоты
3. слабого основания и воды
4. хлорида аммония и воды
5. слабого основания
20. Фосфатная буферная система состоит из смеси:
1. фосфорной кислоты и гидрофосфата калия
2. фосфорной кислоты и дигидрофосфата калия
3. дигидрофосфата и гидрофосфата калия
4. фосфорной и угольной кислоты
5. фосфорной кислоты и ортофосфата калия
21. К буферным системам крови не относится:
1. фосфатный буфер
2. гидрокарбонатный буфер
3. ацетатный буфер
4. гемоглобиновый буфер
5.оксигемоглобиновый буфер
22. Аммонийная буферная система состоит из смеси:
1. гидроксида аммония и ацетата натрия
2. гидроксида и хлорида аммония
3. гидроксида аммония и уксусной кислоты
4. хлорида аммония и уксусной кислоты
5. ацетата и хлорида аммония
23. При добавлении к буферному раствору дистиллированной воды его буферная емкость:
1.уменьшается
2.не изменяется
3.увеличивается
4. становится равной нулю
5.соответствует рН=7.
24. Смешали по 5 мл слабой кислоты и ее калиевой соли одинаковой концентрации, рК кислоты равен 4,80. рН полученного буферного раствора равен:
1. 6,80.
2. 0,70.
3. 9,20.
4. 5,80.
5. 4,80.
25. По формуле рН = рК + lg 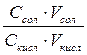 рассчитывают:
рассчитывают:
1. рН любого раствора
2. рН буферного раствора
3. рН растворов высокомолекулярных веществ (ВМВ)
4. рН воды
5. рН изоэлектрического состояния
8. Электродные потенциалы. Окислительно–восстановительные процессы. Потенциометрия в медицинской практике.
1. Нормальный (стандартный) потенциал любого электрода равен Э.Д.С. элемента составленного из данного электрода, в растворе которого активность ионов металла равна 1 моль/л и
1. насыщенного каломельного электрода
2. нормального водородного электрода, в растворе которого а(Н+) =1.
3. насыщенного хлорсеребряного электрода
4. любого металлического электрода, в растворе которого а(Меn+) =1.
5. хингидронного электрода
2. Укажите, какой заряд может быть на металлической пластине, погруженной в раствор своей соли
1. только отрицательный
2. только положительный
3. только равным нулю
4. положительным, отрицательным и равным нулю
5. заряд на пластине при погружении её в раствор соли не возникает
3. От концентрации водородных ионов в растворе не зависит потенциал
1. хингидронного электрода
2. водородного электрода
3. стеклянного электрода
4. каломельного электрода
5. правильного ответа нет
4. Укажите электрод, потенциал которого зависит от рН среды электрода
1. каломельного
2. цинкового
3. хлорсеребряного
4. медного
5. стеклянного
5. В методе потенциометрического титрования для определения концентрации кислот и щелочей производят измерение
1. электропроводности раствора
2. сопротивления раствора
3. эквивалентной электропроводности раствора
4. электродвижущей силы гальванического элемента, состоящего из электрода сравнения и электрода определения
5. удельной электропроводности раствора
6. При погружении металла в чистую воду, на металле возникает заряд
1. отрицательный
2. положительный
3. равный нулю
4. в зависимости от активности металла: положительный, отрицательный или равный нулю
5. заряд на металле, погруженном в воду не возникает
7. Скачок потенциала на границе между различными по составу или по концентрации растворами называется
1. стандартным потенциалом
2. водородным электродом
3. диффузным потенциалом
4. мембранным потенциалом
5. электродвижущей силой гальванического элемента
8. Методы потенциометрического титрования по реакциям нейтрализации, осаждения, окисления-восстановления и комплексообразования основаны
1. на плавном изменении потенциала вблизи эквивалентной точки
2. на резком изменении потенциала вблизи эквивалентной точки
3. на прямой зависимости потенциала от активности потенциалобразующего иона
4. на полной независимости потенциала от активности потенциалобразующего иона.
5. на изменении окраски титранта вблизи эквивалентной точки
9.Укажите, как изменяется потенциал металлического электрода, погруженного в раствор своей соли, если концентрацию соли увеличить
1. не изменяется
2. уменьшается
3. увеличивается
4. сначала уменьшается, а затем увеличивается
5. принимает значение равное нулю и далее не изменяется
10. Металл, погруженный в раствор электролита, например, в раствор своей соли, представляет собой токопроводящую систему, которую в электрохимии называют
1. индикатором
2. электродом
3. электролитической ячейкой
4. адсорбентом
5. катарометром
11. При погружении в раствор своей соли отдавать катионы в раствор и заряжаться отрицательно способны
1. все металлы независимо от их активности
2. только металлы, стоящие в ряду напряжений после водорода
3. только химически активные металлы
4. водород и пассивные металлы
5. металлы способны заряжаться только положительно
12. Реакции, в результате которых изменяется степень окисления одного или нескольких элементов, называют
1. реакциями нейтрализации
2. реакциями гидролиза
3. реакциями обмена
4. окислительно-восстановительными реакциями
5. реакциями соединения
4.
13.Укажите, в каких случаях в уравнениях для расчета величины электродного потенциала можно вместо активности использовать величину концентрации
1. в любом случае
2. в сильно концентрированных растворах
3. в разбавленных растворах
4. нельзя никогда пользоваться концентрацией вместо активности
5. при стандартных условиях
14. Способность вещества проводить электрический ток называется:
1. электродным потенциалом
2. поляризацией электродов
3. диффузным потенциалом
4. сопротивлением
5. электропроводностью
15. Вещество-окислитель и соответствующее вещество-восстановитель называют
1. сопряженной окислительно-восстановительной парой
2. сопряженными кислотой и основанием
3. водородным и гидроксильным показателями
4. мономером и полимером
5. гемолизом и плазмолизом
1.
16. Морфологической и химической неоднородностью внутреннего содержания клеток обусловлен:
1. мембранный и межфазовый потенциалы
2. потенциал хингидронного электрода
3. потенциал каломельного электрода
4. потенциал водородного электрода
5. стандартный потенциал водородного электрода
17. Диффузный потенциал возникает
1. на границе металл-раствор
2. на границе двух металлов
3. между двумя растворами, отделенными друг от друга полупроницаемой мембраной
4. на границе двух газов
5. при контакте двух жидкостей одной природы, но разных концентраций
18 Мембранный потенциал возникает
1. на границе металл-раствор
2. на границе двух металлов
3. между двумя растворами, отделенными друг от друга полупроницаемой мембраной
4. при контакте двух жидкостей одной природы, но разных концентраций
5. на границе газ - жидкость
19. Электродные потенциалы железа и меди соответственно равны -0,44 В и +0,34 В. Электродвижущая сила гальванического элемента из этих электродов равна:
1. -0,78 B
2. +0,10 В
3. +0,78 В
4. -0,10 В
5. +1,29 В
20. Условный заряд, который приписывается атому в молекуле химического соединения, исходя из предположения, что молекула в целом нейтральна и состоит только из ионов, называют
1. степенью электролитической диссоциации
2. степенью гидролиза
3. степенью окисления атома
4. степенью дисперсности
5. насыщаемостью ковалентной связи
21. Реакции, в результате которых изменяется степень окисления одного или нескольких элементов, называют
1. реакциями нейтрализации
2. реакциями гидролиза
3. реакциями обмена
4. окислительно-восстановительными реакциями
5. реакциями соединения
22. В окислительно-восстановительных реакциях изменение степени окисления элементов и их ионов связано
1. с переходом электронов от одних атомов или ионов к другим.
2. с применением катализаторов.
3. с применением ферментов.
4. с понижением температуры процесса до абсолютного нуля.
5. с переходом системы из твердого состояния (кристалл) в жидкое (раствор).
23. Уравнение 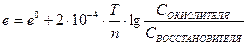 это
это
1. уравнение для определения электродвижущей силы гальванического элемента
2. математическая запись правила Вант-Гоффа
3. уравнение Нернста для определения потенциала окислительно-восстановительного электрода
4. формула для расчета массы эквивалента окислителя и восстановителя
5. формула для расчета степени окисления элементов в уравнениях окислительно-восстановительных реакций
