Необратимыми называют реакции, которые протекают только в одном направлении.
4.
Обратимыми называют реакции, которые одновременно протекают в двух противоположных направлениях.
H2 + I2 ⇄ 2HI
2NO + O2 ⇄ 2NO2
Необратимыми называют реакции, которые протекают только в одном направлении.
BaCl2 + K2SO4 BaSO4¯ + 2KCl
Na2CO3 + 2HCl 2NaCl + CO2 + H2O
Многие процессы протекают без подвода энергии от внешнего источника. Такие процессы называют самопроизвольными.( падение камня с высоты, переход теплоты от более нагретого тела к менее нагретому.
5.Закон Гесса формулируется так:
Изменение энтальпии реакции образования заданных продуктов из данных реагентов не зависит от числа и вида реакций, в результате которых образуются эти продукты.
I следствие:
Энтальпия реакции равна сумме стандартных энтальпий образования продуктов реакции за вычетом суммы стандартных энтальпий образования исходных веществ с учетом стехиометрических коэффициентов.
Для реакции:
aA + bB = cC + dD
математическое выражение I следствия из закона Гесса в общем виде выглядит следующим образом:
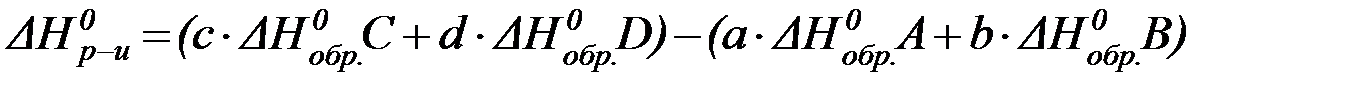 |
II следствие:
Энтальпия реакции равна сумме стандартных энтальпий сгорания исходных веществ за вычетом суммы стандартных энтальпий сгорания продуктов реакции с учетом стехиометрических коэффициентов.
В данном случае математическое выражение запишется так:
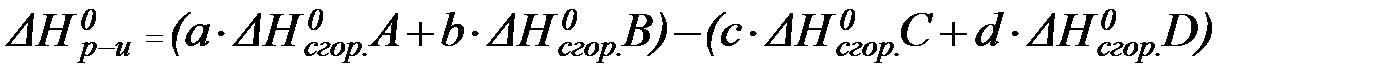 6. Энтропия (S) - термодинамическая функция состояния системы, которая отражает вероятность реализации того или иного состояния системы в процессе теплообмена. В обратимом процессе, протекающем в изотермических условиях, изменение энтропии можно рассчитать по формуле: 6. Энтропия (S) - термодинамическая функция состояния системы, которая отражает вероятность реализации того или иного состояния системы в процессе теплообмена. В обратимом процессе, протекающем в изотермических условиях, изменение энтропии можно рассчитать по формуле:
из которой видно, что размерность энтропии Дж/К или Дж/(моль×К). В необратимых процессах выполняется неравенство:
|
7.
Энтальпия (H) - термодинамическая функция состояния системы, применяемая для изобарных процессов, учитывающая внутреннюю энергию и энергию, затрачиваемую на преодоление внешнего давления. Иными словами, энтальпия характеризует теплосодержание системы.
Стандартной энтальпией образования вещества
( 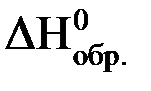 ) называют изменение энтальпии реакции образования 1 моль данного вещества из соответствующих простых веществ, взятых в стандартном состоянии при стандартных условиях. Например:
) называют изменение энтальпии реакции образования 1 моль данного вещества из соответствующих простых веществ, взятых в стандартном состоянии при стандартных условиях. Например:
C(тв.) + О2(газ) = СО2(газ); 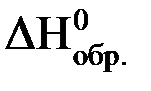 CO2 = -393,5 кДж/моль.
CO2 = -393,5 кДж/моль.
Стандартной энтальпией сгораниявещества( 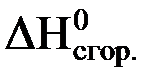 ) называется стандартная энтальпия реакции окисления 1 моль данного вещества до конечных продуктов окисления при стандартных условиях. Например:
) называется стандартная энтальпия реакции окисления 1 моль данного вещества до конечных продуктов окисления при стандартных условиях. Например:
С6H12O6(тв.) + 6O2(газ) = 6CO2(газ) + 6H2O(жидк.);
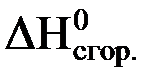 С6H12O6 = -2810 кДж/моль.
С6H12O6 = -2810 кДж/моль.
II следствие: закона Гесса
Энтальпия реакции равна сумме стандартных энтальпий сгорания исходных веществ за вычетом суммы стандартных энтальпий сгорания продуктов реакции с учетом стехиометрических коэффициентов.
В данном случае математическое выражение запишется так:
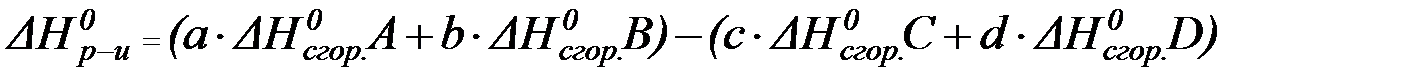
8.Скорость химической реакциидля гомогенной реакции:
Для гомогенной (однородной) системы скорость химической реакции измеряется количеством веществ, вступивших в реакцию или образующихся в результате реакции за единицу времени в единице объема системы.
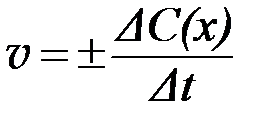 |
aA + bB ⇄ cC + dD,
скорость прямой реакции: 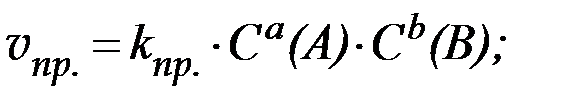
скорость обратной реакции: 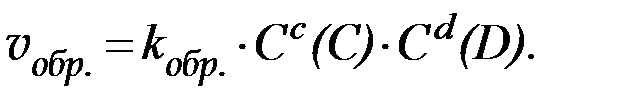
[моль∙л-1∙с-1].
9.Скорость химической реакции для гетерогенной реакции:
Для гетерогенной (неоднородной) системы скорость химической реакции измеряется количеством веществ, вступивших в реакцию или образующихся в результате реакции за единицу времени на единице поверхности раздела фаз:
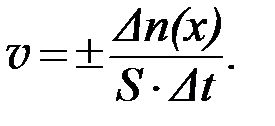
: [моль∙м–2∙с–1].
10. правило Вант-Гоффа:
При повышении температуры на каждые 100 скорость химической реакции возрастает в 2-4 раза. Для ферментативных процессов, протекающих в биосистемах, Yбольше 4( обычно около 7).
11.Закон действующих масс открыли в 1864 году норвежские ученые К.Гульдберг и П.Вааге.
Скорость химической реакции, протекающей при постоянной температуре в гомогенной среде, пропорциональна произведению концентраций реагирующих веществ в степенях, равных коэффициентам, стоящим перед формулами этих веществ в уравнении реакции.
aA + bB = cC + dD,
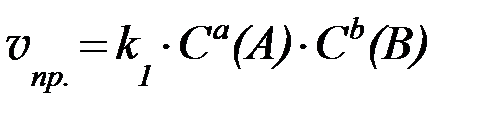
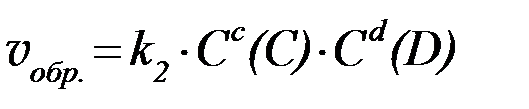
12.Катализ – это изменение скорости химической реакции в присутсвии веществ, которые после завершения реакции в неизменном виде и количестве.
Увелечение скорости реакции называют положительным катализом
Уменьшение скорости реакции называют положительным катализом
Ингибитор – вещества вызывающие отрицательный катализ
Гомогенный катализ – если реагенты и катализаторы находятся в одном агрегатном состоянии.
Гетерогенный катализ – если реагенты и катализаторы находятся в разных агрегатных состояних.
Биокатализаторы- ферме́нты или энзи́мы — обычно белковые молекулы или молекулы РНК или их комплексы, ускоряющие химические реакции в живых системах.
Необратимыми называют реакции, которые протекают только в одном направлении.
В частности, к необратимым реакциям относятся те, которые сопровождаются образованием осадка, газа или малодиссоциирующего вещества (например, Н2О).
Примеры:
BaCl2 + K2SO4 BaSO4¯ + 2KCl

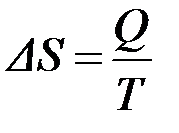 ,
, 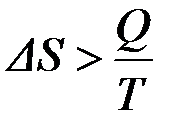 . Физический смысл энтропии установила статистическая термодинамика. Согласно уравнению Больцмана:
. Физический смысл энтропии установила статистическая термодинамика. Согласно уравнению Больцмана: 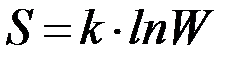 ,
,