При постоянных давлении и температуре самопроизвольно протекают только такие химические реакции, которые сопровождаются уменьшением энергии Гиббса.
Анализ уравнения позволяет установить, какой из факторов, составляющих энергию Гиббса, ответственен за направление протекания химической реакции, энтальпийный (ΔH) или энтропийный (ΔS · T).
· Если ΔH < 0 и ΔS > 0, то всегда ΔG < 0 и реакция возможна при любой температуре.
· Если ΔH > 0 и ΔS < 0, то всегда ΔG > 0, и реакция с поглощением теплоты и уменьшением энтропии невозможна ни при каких условиях.
· В остальных случаях (ΔH < 0, ΔS < 0 и ΔH > 0, ΔS > 0) знак ΔG зависит от соотношения ΔH и TΔS. Реакция возможна, если она сопровождается уменьшением изобарного потенциала; при комнатной температуре, когда значение T невелико, значение TΔS также невелико, и обычно изменение энтальпии больше TΔS. Поэтому большинство реакций, протекающих при комнатной температуре, экзотермичны. Чем выше температура, тем больше TΔS, и даже эндотермические реакции становятся осуществляемыми.
2.Постулаты Бора. Принцип Гейзенберга.
Исходя из своих постулатов Бор создал теорию простейшего водородоподобного атома и объяснил линейчатый спектр атома водорода.
датский физик Нильс Бор разработал теорию строения атома водорода, используя модель Резерфорда и квантовый постулат Планка.
1. постулат Существуют только некоторые стационарные состояния атома, находясь в которых он не излучает энергию. Этим стационарным состояниям соответствуют вполне определенные (стационарные) орбиты, по которым движется электроны. При движении по стационарным орбитам электроны, несмотря на наличие у них ускорения, не излучают электромагнитных волн.
Второй постулат устанавливает :
При переходе атома (электрона) из одного стационарного состояния в другое испускается или поглощается один фотон с энергией
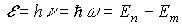 , (7)
, (7)
где Еn, Еm - энергии атома (электрона) в стационарных состояниях n и m, которые определяются согласно (6
Теория Бора позволила объяснить механизм образования оптического спектра.
Принцип неопределённости Гейзенбе́рга (или Га́йзенберга) в квантовой механике — фундаментальное соображение (соотношение неопределённостей), устанавливающее предел точности одновременного определения пары характеризующих систему квантовых наблюдаемых, описываемых некоммутирующими операторами (например, координаты и импульса, тока и напряжения, электрического и магнитного поля).
Соотношение неопределённостей[* 1] задаёт нижний предел для произведения среднеквадратичных отклонений пары квантовых наблюдаемых. Принцип неопределённости, открытый Вернером Гейзенбергом в 1927 г., является одним из краеугольных камней физической квантовой механики.
3. NH4CI+K2CO3+H2O=>... ( Гидролиз )
2NH4Cl+K2CO3+H2O=2NH4OH+2KCl+CO2.
--------------------------------------------------------------------------------------------------------------------------
Дисперсные системы
Диспе́рсная систе́ма — это образования из двух или большего числа фаз (тел), которые практически не смешиваются и не реагируют друг с другом химически. Первое из веществ (дисперсная фаза) мелко распределено во втором (дисперсионная среда). Если фаз несколько, их можно отделить друг от друга физическим способом (центрифугировать, сепарировать и т. д.).
Обычно дисперсные системы — это коллоидные растворы, золи. К дисперсным системам относят также случай твёрдой дисперсной среды, в которой находится дисперсная фаза.
Наиболее общая классификация дисперсных систем основана на различии в агрегатном состоянии дисперсионной среды и дисперсной фазы. Сочетания трех видов агрегатного состояния позволяют выделить девять видов дисперсных систем. Для краткости записи их принято обозначать дробью, числитель которой указывает на дисперсную фазу, а знаменатель на дисперсионную среду, например для системы «газ в жидкости» принято обозначение Г/Ж.
Примером сложной дисперсной системы может служить молоко, основными составными частями которого (не считая воды) являются жир, казеин и молочный сахар. Жир находится в виде эмульсии и при стоянии молока постепенно поднимается кверху (сливки). Казеин содержится в виде коллоидного раствора и самопроизвольно не выделяется, но легко может быть осаждён (в виде творога) при подкислении молока, наприм., уксусом. В естественных условиях выделение казеина происходит при скисании молока. Наконец, молочный сахар находится в виде молекулярного раствора и выделяется лишь при испарении воды.
2.ионное произведение воды, ph
3.гидролиз какой-то
--------------------------------------------------------------------------------------------------------------------------
Билет 4
1) Потенциал ионизации, радиус атома, сродство к электрону.
Ионизация – это удаление электрона из свободного атома или молекулы в газе. (Только неупругие столкновения приводят к ионизации). Энергия, которая должна быть сообщена электрону для его ионизации, называют потенциалом ионизации.
Потенциал ионизации. – это энергия, затраченная в вакууме на удаление электрона из атома на бесконечно большое расстояние. Ме = Меn+ + е + I . (+) соответствует затрате энергии извне – система энергию получает.
Измеряется в электрон-вольтах или кДж. 1 эВ = 1.6 10-19Дж.
Например: IСа= 6,11 эВ. Чем меньше потенциал ионизации, тем легче электрон оторвать от атома. Легче всего удалить первый электрон, затем второй и т.д., поэтому I1 < I2 < I3. Фактически, П.И. – это мера степени металлических свойств элемента. Чем меньше П.И., тем сильнее выражены металлические свойства атома.
В группе придвижении сверху вниз (с увеличением порядкового номера) наблюдается уменьшение П.И., что связано с увеличением атомных радиусов, большим расстоянием до ядра и. соответственно, меньшим притяжением к ядру. В периоде с увеличением порядкового номера – в основном, постепенное увеличение П.И., связанное с ростом заряда ядра и, соответственно с большим притяжением электронов к ядру. Однако есть исключения, связанные с особенностями электронной структуры атомов.
Радиусом атома- называется расстояние между атомным ядром и самой дальней из стабильных орбит электронов в электронной оболочке этого атома.
Значения атомных радиусов элементов находятся в периодической зависимости от атомного номера элемента. В периоде при движении слева направо наблюдается уменьшение атомных радиусов, т.к. увеличивается притяжение электронов к ядру, несмотря на силы отталкивания между электронами, количество которых увеличивается. При движении в группах сверху вниз имеет место увеличение атомных радиусов из-за увеличения числа электронных слоев атома. Радиусы катионов меньше, а радиусы анионов больше, чем радиусы атомов.
СРОДСТВО к ЭЛЕКТРОНУ (Е).
Сродство к электрону – энергия, которая выделяется в результате присоединения электрона к атому: Э + е = Эn+ -
Наибольшим сродством к электрону обладают р-элементы VII группы, т.к. они приобретают конфигурацию s2р6 – инертных газов.
Наименьшим и даже отрицательным – атомы с конфигурацией s2р6 (инертные газы), т.е. они фактически отталкивают электрон от атома. Водород может не только терять электрон, но и приобретать. Но сродства к электрону водорода в 20 раз меньше, чем потенциал ионизации. Поэтому, в основном атом водорода образует положительно заряженные ионы Н+, а не Н-.
2) Растворы. Законы Рауля.
Раствор — гомогенная физико–химическая система переменного состава, состоящая из двух или более компонентов и продуктов их взаимодействия.
По агрегатному состоянию растворы разделяют на жидкие, твердые и газообразные (рис.1). Наиболее значительную роль в химии и особенно в биохимии играют жидкие растворы.
Компонентами раствора являются растворитель (среда) и растворенное вещество, равномерно распределенное в растворителе в виде молекул или ионов. Под растворителем обычно понимают то вещество, которое находится в таком же агрегатном состоянии, как и раствор в целом. Если вещества, составляющие раствор, имеют одинаковое агрегатное состояние (например, спирт и вода), то растворителем называют то из веществ, которое имеется в большем количестве.
Первый закон Рауля
Над каждой жидкостью (растворителем или раствором) устанавливается определенное давление пара, насыщающего пространство. Это давление характеризует состояние равновесия между жидкой фазой и находящимися над нею молекулами растворителя.
Согласно Первому закону Рауля относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества:
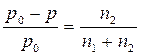 или
или 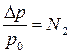 ,
,
где n2– количество растворенного вещества
n1- количество вещества растворителя.
p0-давление пара растворителя , p -давление пара раствора
Второй закон Рауля
Наряду с понижением давления пара изменяются также температуры кипения и замерзания указанных растворов. Растворы кипят при более высокой температуре, а замерзают – при более низкой, по сравнению с соответствующими температурами для чистого растворителя.
Повышение температуры кипения одномоляльного раствора называется эбулиоскопической постоянной растворителя Екип, а понижение температуры замерзания – криоскопической постоянной растворителя Езам. Таким образом, в соответствии со вторым законом Рауля повышение температуры кипения или понижение температуры замерзания разбавленных растворов неэлектролитов пропорциональны числу частиц растворенного вещества и не зависят от его природы:
Dtкип = Екип · m,
Dtзам = Езам · m;
где Екип и Езам – коэффициенты пропорциональности, соответственно - эбулиоскопическая и криоскопическая константы, зависящие только от природы растворителя. Для воды Езам = 1,86; Екип = 0,516; m – моляльность раствора.
3) CI2+I2+H20 = (ОВР)
5Cl2 + I2 + 6H2O = 10HCl + 2HIO3
Cl2(0) +2e- --> 2Cl(-1) 5 процесс восстановления, Cl окисл-ль
I2(0) -10e- ----> 2I(+5) 1 процесс окисления, I восстановитель
--------------------------------------------------------------------------------------------------------------------------
1) Понятие валентности и естественное окисление элемента. Основные классификации неорганических соединений.
2) Произведение растворимости.
3)Написать продукты реакции: Na2S+ZnSO4=(эта реакция обмена)
ZnSO4 + Na2S=Na2SO4+ZnS
Zn^(2+) + SO4^(2-) + 2Na^(+) + S^(2-) = 2Na^(+) + SO4^(2-) + ZnS
Zn^(2+) + S^(2-) = ZnS
--------------------------------------------------------------------------------------------------------------------------
Билет 12:
1) ОВР: ZN+H2SO4(конц.)
3Zn+4H2SO4(конц)=3ZnSO4+S+4H2O
Zn(0)-2e=Zn(+2)|3 окисление
S(+6)+6e=S(0) |1 восстановление
