Вопрос № 3 Стехиометрические законы химии (30 мин.)
Стехиометрия – раздел химии, в котором рассматриваются массовые и объемные отношения между реагирующими веществами.
1. Закон сохранения массы вещества
(М.В. Ломоносов, 1748 г.; А.Лавуазье, 1789 г.)
Масса веществ, вступающих в реакцию, равна массе веществ, образующихся в результате реакции.
С точки зрения атомно-молекулярного учения этот закон объясняется следующим образом: в результате химической реакции атомы не исчезают и не возникают, а происходит их перегруппировка. Так как число атомов до реакции и после нее остается неизменным, то их общая масса также не изменяется.
Ломоносов связал закон сохранения массы вещества с законом сохранения энергии и рассматривал их в единстве как всеобщий закон природы. Современная наука подтвердила выводы Ломоносова. Взаимосвязь массы и энергии выражается уравнением Эйнштейна: Е = mc2.
2. Закон постоянства состава
(Ж. Пруст, 1801 г.)
Всякое чистое вещество, независимо от способа его получения, всегда имеет постоянный качественный и количественный состав.
Например, оксид углерода (IV) – углекислый газ – можно получить различными способами:
С + О2 ® СО2
С3Н8 + 5О2 ® 3СО2 + 4Н2О
СаСО3 ® СО2 + СаО
Na2CO3 + 2HCl ® СО2 + 2NaCl + H2O
И во всех случаях углекислый газ будет иметь один и тот же состав:
27,29 % С и 72,71 % Н.
Данный закон справедлив для соединений с молекулярной структурой (такие соединения называются дальтониды). Соединения с немолекулярной структурой – бертоллиды – с атомной, ионной и металлической решеткой имеют переменный состав, который зависит от способа получения. Например, в зависимости от давления и температуры оксиды урана могут иметь различный состав: UO3 – от UO2,5 до UO3; UO – от UO0,9 до UO1,3.
3. Закон кратных отношений
(Д. Дальтон, 1803 г.)
Если два элемента образуют друг с другом несколько химических соединений, то количества одного элемента, соединяющееся с одним и тем же количеством другого, относятся друг к другу как небольшие целые числа.
Этот закон справедлив только для соединений молекулярного состава. Хорошей иллюстрацией его являются оксиды азота.
| Оксид | Состав оксида, % | Части О на 1 часть N | Относитель-ное содержание О | |
| азот | кислород | |||
| Оксид азота (I) N2O | 63,7 | 36,3 | 0,57 | |
| Оксид азота (II) NO | 46,7 | 53,3 | 1,14 | |
| Оксид азота (III) N2O3 | 36,8 | 63,2 | 1,71 | |
| Оксид азота (IV) NO2 | 30,4 | 69,6 | 2,28 | |
| Оксид азота (V) N2O5 | 25,9 | 74,1 | 2,85 |
Закон кратных отношений не соблюдается для соединений переменного состава, а также для соединений, которые состоят из большого числа атомов. Например, в углеводородах С18Н38 и С20Н42 массы углерода и водорода соотносятся как целые числа, но их нельзя назвать небольшими числами.
4. Закон объемных отношений
(Гей-Люссак, 1808 г.)
Объемы вступающих в реакцию газов относятся друг к другу и к объемам образующихся газообразных продуктов как небольшие целые числа.
Например, в реакции получения аммиака
N2 + 3H2 D 2NH3
объемы азота, водорода и аммиака относятся как 1 : 3 : 2.
Закон этот справедлив в том случае, если все измерения объемов газов проведены при одинаковых температуре и давлении.
5. Закон эквивалентов
( И. Рихтер, 1793 г.)
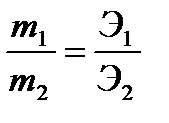 | Массы реагирующих друг с другом веществ пропорциональны их эквивалентам. |
Из закона постоянства состава следует, что элементы взаимодействуют между собой в строго определенных количественных соотношениях.
Химическим эквивалентом элемента или соединения называется такое его количество (в молях), которое взаимодействует с 1 моль атомов водорода или замещает это же количество атомов водорода в химических соединениях.
Единица химического эквивалента – моль.
Например, в соединениях
| HBr | Эквивалент Br = 1 моль |
| H2O | Эквивалент О = 1/2 моль |
| PH3 | Эквивалент Р = 1/3 моль |
| SiH4 | Эквивалент Si = 1/4 моль |
Эквивалентная масса - масса 1 эквивалента, выраженная в г/моль или кг/кмоль.
При решении задач удобнее пользоваться другой формулировкой закона эквивалентов:
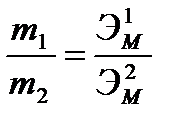 | Массы реагирующих друг с другом веществ пропорциональны их эквивалентным массам (объемам). |
Вычисление эквивалентных масс
1. Эквивалентная масса элемента
ЭМ (элемента) = 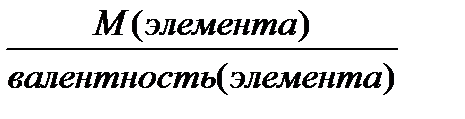 , г/моль (кг/кмоль)
, г/моль (кг/кмоль)
| HBr | ЭМ (Br) = 80/1 = 80 г/моль |
| H2O | ЭМ (O) = 16/2 = 8 г/моль |
| PH3 | ЭМ (P) = 31/3=10,3 г/моль |
| CO2 | ЭМ (C) = 12/4 = 3 г/моль |
| CO | ЭМ (C) = 12/2 = 6 г/моль |
2. Эквивалентная масса кислоты
ЭМ (кислоты) = 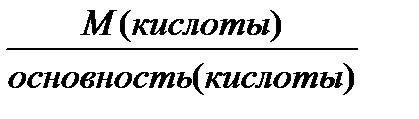 , г/моль (кг/кмоль)
, г/моль (кг/кмоль)
Основность кислоты равна числу атомов водорода в ней.
| HNO3 | ЭМ (HNO3) = 63/1 = 63 г/моль |
| H2SO4 | ЭМ (H2SO4) = 98/2 = 49 г/моль |
| H3PO4 | ЭМ (H3PO4) = 98/3 = 32,7 г/моль |
3. Эквивалентная масса гидроксида (основания)
ЭМ (гидроксида) = 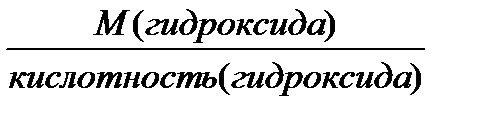 , г/моль (кг/кмоль)
, г/моль (кг/кмоль)
Кислотность гидроксида равна числу ОН-групп в нем.
| KOH | ЭМ (KOH) = 56/1 = 56 г/моль |
| Ba(OH)2 | ЭМ (Ba(OH)2) = 171/2 = 85,5 г/моль |
| Fe(OH)3 | ЭМ (Fe(OH)3) = 107/3 = 35,7 г/моль |
4. Эквивалентная масса оксида
N(O) – число атомов кислорода в оксиде.
ЭМ (оксида) = 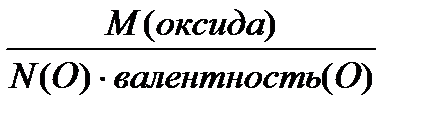 , г/моль (кг/кмоль)
, г/моль (кг/кмоль)
| NO | ЭМ (NO) = 30/(1×2) = 15 г/моль |
| NO2 | ЭМ (NO2) = 46/(2×2) = 11,5 г/моль |
5. Эквивалентная масса соли
N(металла) – число атомов металла в соли.
ЭМ (соли) = 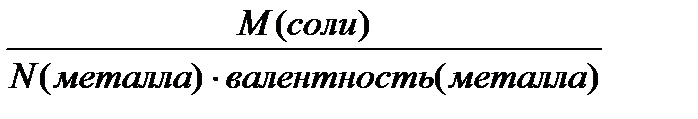 , г/моль (кг/кмоль)
, г/моль (кг/кмоль)
| СаСО3 | ЭМ (СаСО3) = 100/(1×2) = 50 г/моль |
| Al2(SO4)3 | ЭМ (Al2(SO4)3) = 342/(2×3) = 57 г/моль |
6. Закон Авогадро (1811 г.)
В равных объемах различных газов при одинаковых условиях содержится одинаковое число молекул.
Из закона Авогадро вытекают два очень важных следствия.
1 следствие
Один моль любого газа при одинаковых условиях занимает один и тот же объем (молярный объем газа).
Один моль любого газа при нормальных условиях занимает объем
V0 = 22,4 л/моль (м3/кмоль). Точное значение 22,41383 ± 0,0070 л/моль.
| Нормальные условия t0 = 00C; T0 = 273 K; p0 = 1 ат = 760 мм рт.ст. = 101,3 кПа = 105 Па = 0,1 МПа |
В условиях, отличных от нормальных (Т, р), молярный объем газа или пара можно рассчитать по формуле объединенного газового закона:
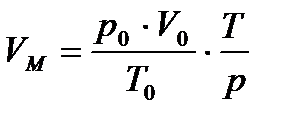 , л/моль (м3/кмоль)
, л/моль (м3/кмоль)
2 следствие
Отношение массы определенного объема одного газа к массе такого же объема другого газа (при одинаковых условиях Т, р) называется плотностью первого газа по второму.
D2 = 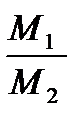
D2 – плотность первого газа по второму.
| Расчет плотности газа или пара по | |||
| водороду | кислороду | азоту | воздуху |
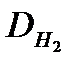 = = 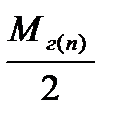 | 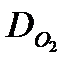 = = 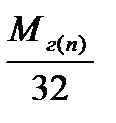 | 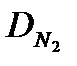 = = 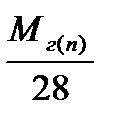 | 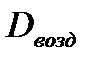 = = 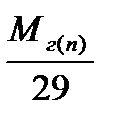 |
Закон Авогадро как и другие газовые законы строго выполняется лишь для идеального газа, в котором молекулы не имеют объема и сталкиваются между собой только упруго. Так как в природе идеального газа нет, то газовые законы имеют приближенный характер.
(Все определения, формулы, графики и уравнения реакций даются под запись.)
