Параметры химической связи двухатомных молекул
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
НИЖЕГОРОДСКИЙ ГОСУДАРСТВЕННЫЙ
ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ им. Р.Е.АЛЕКСЕЕВА
Кафедра «Общая и неорганическая химия»
СПРАВОЧНЫЕ МАТЕРИАЛЫ
ПО КУРСУ ОБЩЕЙ И НЕОРГАНИЧЕСКОЙ ХИМИИ
Для студентов всех специальностей дневной и вечерней форм обучения
(Выпуск 3)
Нижний Новгород 2010
Составители: Л.Н.Четырбок, А.Д.Самсонова, В.И. Наумов, Г.Н.Борисова, А.В.Борисов
УДК 54 (07)
Справочные материалы по курсу общей химии для студентов всех
специальностей дневной и вечерней форм обучения/НГТУ; Сост.: Л.Н.Четырбок, А.Д.Самсонова и др. . Н.Новгород, 2009.- 36с.
Приведены справочные материалы для практических и лабораторных
занятий по курсу общей и неорганической химии.
Научный редактор Г.Н. Паниичева
Редактор Э..Б.Абросимова
Подп. к печ. Формат 60×841/16. Бумага газетная. Печать офсетная. Печ.л. . Уч.-изд.л. . Тираж 2000 экз. Заказ .
-----------------------------------------------------
Нижегородский государственный технический университет.
Типография НГТУ. 603600, Н.Новгород, ул. Минина, 24.
© Нижегородский государственный
технический университет, 2010
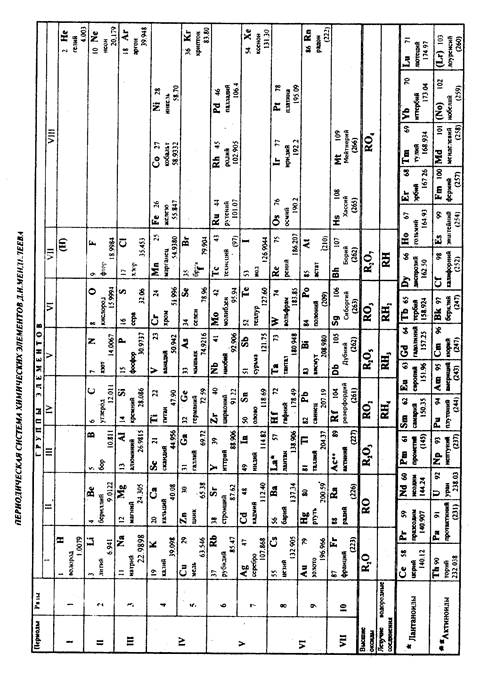
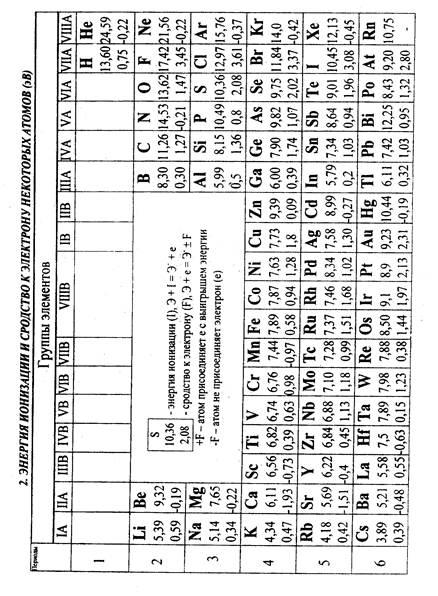
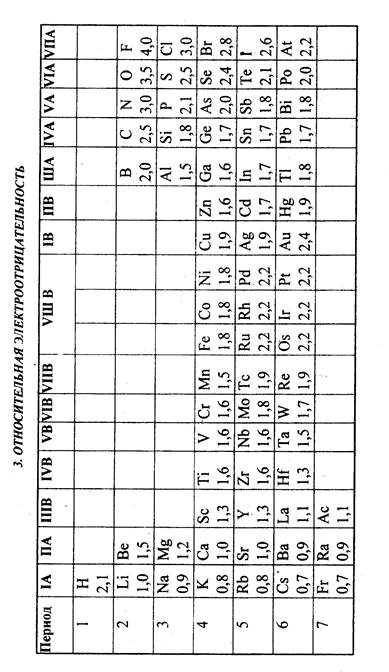
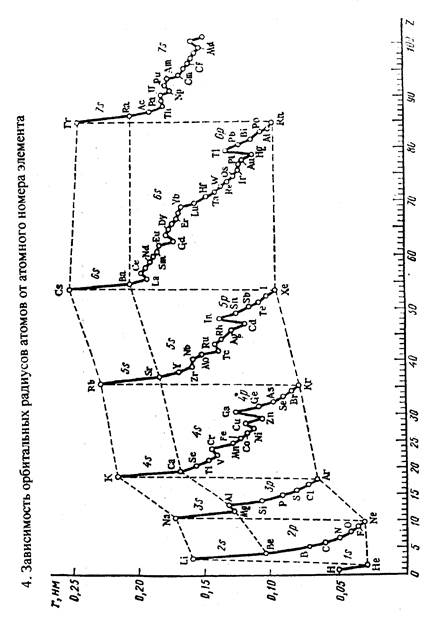
ПЕРИОДИЧЕСКАЯ ЗАВИСИМОСТЬ СРОДСТВА К ЭЛЕКТРОНУ (F1) И ПЕРВОЙ ЭНЕРГИИ ИОНИЗАЦИИ(I1 ) АТОМОВ ОТ АТОМНОГО НОМЕРА ЭЛЕМЕНТА
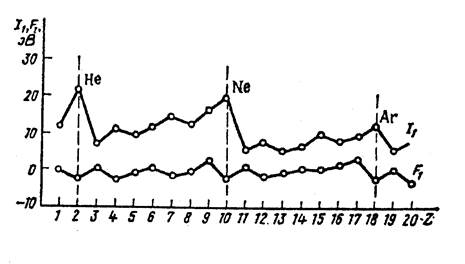 Сродство к электрону взято с обратным знаком, т.е. приведены первые энергии ионизации отрицательно заряженных ионов Э-
Сродство к электрону взято с обратным знаком, т.е. приведены первые энергии ионизации отрицательно заряженных ионов Э-
СВЕДЕНИЯ О НЕКОТОРЫХ ЭЛЕМЕНТАРНЫХ ЧАСТИЦАХ
| Частица | Символ | Масса покоя | Заряд, Кл | Заряд | |
| Кг | относительная масса | ||||
| Протон Нейтрон Электрон | Р n e | 1,673 10-27 1,675 10-27 9,109 10-31 | 1,007276 1,008665 0,000549 | 1,602 10-19 0 1,602 10-19 | +1 -1 |
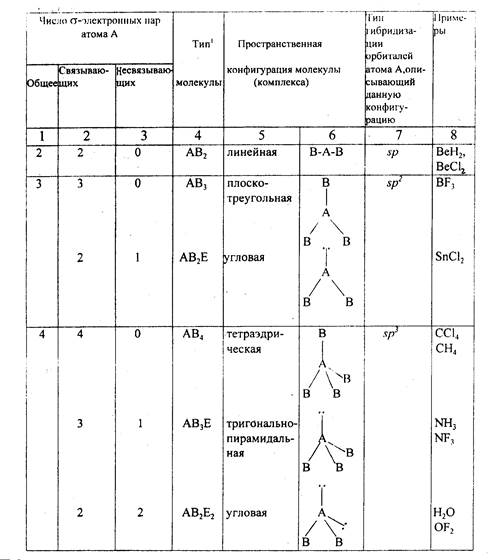
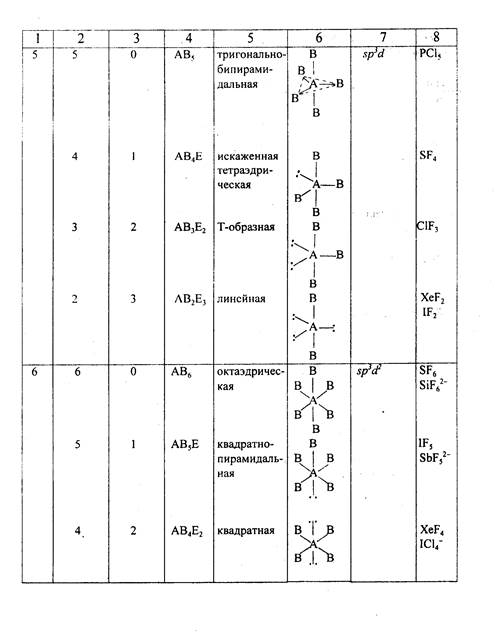
РАСПОЛОЖЕНИЕ ВАЛЕНТНЫХ σ-ЭЛЕКТРОННЫХ ПАР
ЦЕНТРАЛЬНОГО АТОМА "А" И ПРОСТРАНСТВЕНННАЯ
КОНФИГУРАЦИЯ МОЛЕКУЛ (КОМПЛЕКСОВ) АВn
СТРОЕНИЕ И ЭЛЕКТРИЧЕСКИЕ МОМЕНТЫ ДИПОЛЕЙ (μ) НЕКОТОРЫХ МОЛЕКУЛ
| Тип | Пространственная конфигурация | Молекула | μ∙1029, Кл×м | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
ДЛИНА (d) И ЭНЕРГИИ (Е) ХИМИЧЕСКОЙ СВЯЗИ
| Связь | d, нм | Е, кДж/моль | Связь | d, нм | Е, кДж/моль | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
| |
|
|
|
ПАРАМЕТРЫ ХИМИЧЕСКОЙ СВЯЗИ ДВУХАТОМНЫХ МОЛЕКУЛ
| Молекула | Энергия связи, кДж/моль | Длина связи, нм | Энергия иони-зации, эВ | Сродство к электрону, эВ | ||||||||||||||||||||||||||||||||||||
| I |
|
|
|
| | |||||||||||||||||||||||||||||||||||
| II |
|
|
|
|
| |||||||||||||||||||||||||||||||||||
| III |
|
|
|
| |
Молекулы группы I при ионизации теряют связывающие электроны, мо-лекулы группы II – теряют разрыхляющие электроны, а молекулы группы III теряют не связывающие электроны
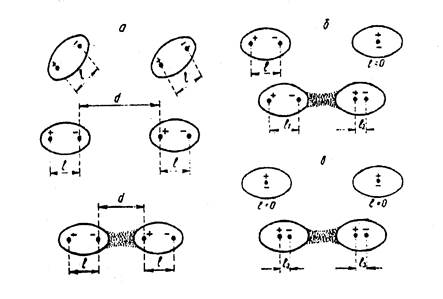 11. ТИПЫ МЕЖМОЛЕКУЛЯРНЫХ ВЗАИМОДЕЙСТВИЙ
11. ТИПЫ МЕЖМОЛЕКУЛЯРНЫХ ВЗАИМОДЕЙСТВИЙ
а-ориентационное; б – индукционное; в – дисперсионное; l – длина диполя; d – межмолекулярное расстояние
