Комплексные соединения. Основные положения координационной теории.
Комплексные соединения - химические соединения, представляющие собой сложные ионы или молекулы, способные существовать как в кристаллическом, так и в растворённом состоянии. Основоположник химии комплексных соединений Альфред Вернер.Основные положения координационной теории:
1.Комплексные соединения состоят из внутренней и внешней сферы.
2.Во внутреннюю сферу входит центральный ион-комплексообразователь, окруженный лигандами. Внутреннюю сферу обозначают квадратными скобками.
(* Ионами-комплексообразователями чаще всего являются ионы металлов преимущественно d – элементов)
3. Вокруг центрального иона-комплексообразователя находятся противоположно заряженные ионы или нейтральные молекулы- лиганды.
Важнейшие лиганды:
анионы нейтральные мол-ы
I- - иодо NH30 – аммин
Cl- - хлоро H2O0 – аква
Br- - бромо СО0 – карбонил
CN- - циано NO0 - нитрозил
OH- - гидроксо
 NO2- – нитро
NO2- – нитро
SO4 –сульфато
4.Число лигандов, которые координируются вокруг центрального иона-комплексообразователя, называется координационным числом.
* Координационное число зависит от заряда центрального иона, и, как правило, в 2 раза больше него.
5. Заряд внутренней сферы (комплексного иона) равен алгебраической сумме зарядов иона-комплексообразователя и лигандов.
6. Ионы, не вошедшие во внутреннюю сферу, образуют внешнюю сферу. Заряд внешней сферы численно равен заряду внутренней сферы, но противоположен по знаку.
Пример:
18.Комплексные соединения: строение, класиффикация, номенклатура.
Строение: ( на примере тетрагидроксоалюмината натрия) 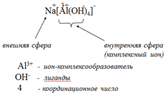
 Классификация:
Классификация:
Номенклатура:
Соль содержит комплексный катион[ Kat ]+An-
Называют:
1. анион соли (сульфат, фосфат, хлорид и т.д.)
2.входящие во внутреннюю сферу лиганды:
● сначала анионы с окончанием на «о» ,
● затем лиганды, представляющие собой нейтральные молекулы.
* Если одинаковых лигандов во внутренней сфере больше одного, то их количество указывают греческими числительными (2 - ди, 3 – три, 4 – тетра, 5 - пента, 6 - гекса и т. д.)
3. центральный ион – комплексообразователь в русской транскрипции в
родительном падеже.
* Если центральный атом имеет переменную валентность, её указывают римской цифрой в скобках после названия комплексообразователя.
Пример:
Соль содержит комплексный анион Kat +[An]-
Называют
1.входящие во внутреннюю сферу
● сначала анионы с окончанием на «о» ,
● затем лиганды, представляющие собой нейтральные молекулы
* Если одинаковых лигандов во внутренней сфере больше одного, то их количество
указывают греческими числительными (2 - ди, 3 – три, 4 – тетра, 5- пента, 6- гекса и т. д.)
2. центральный ион – комплексообразователь в латинской транскрипции с прибавлением суффикса – «ат»
Fe –феррат, Cu – купрат, Ag – аргентат,Zn – цинкат, Hg – меркурат, Co – кобальтат, Cr – хромат и т.д.
* Если центральный атом имеет переменную валентность, её указывают римской цифрой в скобках после названия комплексообразователя.
пример:

19. Комплексные соединения: Получение. Химические свойства, Применение комплексных соединений.
Получение:
Для их протекания необходимо наличие в растворе соединения,
содержащего атом-комплексообразователь, и ионов или молекул,
которые могут выступать в качестве лигандов.
Al(OH)3 + NaOH = Na[Al(OН)4]
СuSO4 + 4NН3 = [Сu(NНЗ)4]SO4
FeSО4 +6KCN = K4[Fe(CN)6] + K2SО4
Химические свойства: 

Применение комплексных соединений:
1.Комплексные соединения имеют важное значение для живых организмов, так гемоглобин крови образует комплекс с кислородом для доставки его к клеткам, хлорофилл находящийся в растениях является комплексом.
2. В аналитической химии в качестве индикаторов.
3. извлечение металлов из руд.
