Тема 7 . Элементы качественного анализа
В качественном анализе неорганических веществ преимущественно исследуют растворы электролитов (солей, кислот и оснований), которые в водных растворах находятся в диссоциированном состоянии:
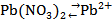 + 2
+ 2 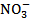 ;
; 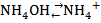 +
+ 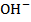 ;
; 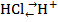 +
+ 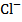
Целью качественного анализа является установление состава вещества, или обнаружение того или иного иона (катиона или аниона).
Качественный анализ выполняется путем проведения аналитической реакции на данный ион с использованием определенного реактива или реагента. Аналитические реакции заканчиваются определенным визуальным эффектом: выпадением осадка, изменением окраски раствора, выделением газа. В качестве аналитических реакций используют реакции:
а)осаждения: 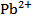 + 2
+ 2 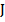 =
= 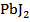 ;
;
б) комплексообразовния: 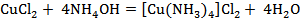 ;
;
в) окислительно-восстановительные: 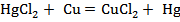 .
.
При проведении качественного анализа особое значение имеют чувствительность реакций и их специфичность.
Чувствительность реакции определяется наименьшим количеством вещества, которое может быть обнаружено данным реактивом в капле раствора (0,01 – 0,03 мл). Чувствительность реакции выражают взаимно связанными величинами: открываемым минимумом и минимальным разбавлением.
Открываемым минимумом называют наименьшее количество вещества ( в мкг), которое можно открыть данной реакцией. Например, открываемый минимум для иона меди 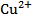 с аммиаком составляет 1:250 000 мл, что указывает на возможность этой реакции открыть ион меди при его содержвании 1 г 250 000 мл раствора.
с аммиаком составляет 1:250 000 мл, что указывает на возможность этой реакции открыть ион меди при его содержвании 1 г 250 000 мл раствора.
Открываемый минимум (m) и минимальная концентрация © связаны между собой соотношением:
m = C∙V∙ 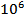 ; C=
; C= 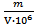
где C – минимальная концентрация, моль/л;
m – открываемый минимум, мкг;
V – объем раствора, мл.
Специфические реакции (частные) позволяют обнаружить какой-либо один ион в смеси с другими ионами. Например, специфической или частной реакцией на ион Fe(II) является гексацианоферрат(III) калия 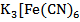 с образованием осадка турнбулевой сини:
с образованием осадка турнбулевой сини:
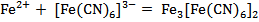
турнбулева синь
Специфической реакцией на ион Fe(III) является реакция с роданид-ионом с образованием кроваво-красного роданида железа (lll):
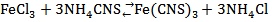
роданид железа(lll)
Никакой другой ион не дает такого эффекта с роданид-ионом.
Открытие иона специфической реакцией проводится в отдельной порции исследуемого раствора дробным анализом.
Когда невозможно обнаружить ионы в смеси дробным анализом, так как разные ионы одинаково реагируют на один и тот же реактив используется другой вид химического анализа – систематический.
В ходе систематического анализа необходимо отделять последовательно один ион от другого. Для этого производят осаждение группы ионов групповым осадителем, а затем применяют комплекс операций (растворяют легкорастворимые соединения, фильтруют, проверяют осаждение какого-либо иона на полноту осаждения и т.п.), в результате которых отделяют один ион от другого. После этого проводят специфические реакции на каждый ион.
Для удобства обнаружения ионы делят на группы. В настоящее время общепринятой является классификация катионов на пять аналитических групп (см.табл. 7.1), основанная на применении следующих групповых реактивов: соляной кислоты НСl, серной кислоты 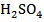 , раствора щелочи NaOH и гидроксида аммония
, раствора щелочи NaOH и гидроксида аммония 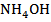 .
.
Кислотно-основная классификация катионов
Таблица 7.1
| Группа | Катионы | Групповой реагент |
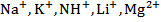 | Нет | |
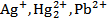 | Растворы HCl | |
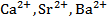 | Растворы 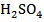 | |
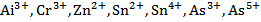 | Растворы NaOH (осадки растворимы в избытке NaOH) | |
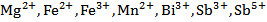 | Раствор NaOH или водный аммиак (осадки не растворимы в избытке NaOH) | |
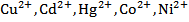 | Водный аммиак (осадки растворимы в избытке 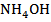 ) ) |
Строгой классификации анионов по аналитическим группам из-за отсутствия групповых реактивов нет.
Лабораторная работа № 10.
