Коллигативные свойства растворов неэлектролитов
Коллигативные свойства растворов электролитов.
Раствор электролита состоит из растворителя и растворенного вещества (электролита), которое частично или полностью диссоциирует на ионы. В растворе число частиц в результате диссоциации увеличивается. Коллигативные свойства растворов электролитов описываются уравнениями с поправочным множителем – изотоническим коэффициентом ( i), учитывающим процесс диссоциации:
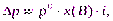 (12)
(12)
×i(13)
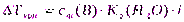 (14)
(14)
pосм= С×R×T×i, (15)
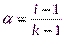 (16)
(16)
α – степень диссоциации электролита;
k– число частиц, образующихся при диссоциации 1молекулы электролита.
Пример 8. Определите температуру кипения раствораAgNO3, еслиω(AgNO3)= 2%,α(AgNO3) = 90%,ρ(р-ра) = 1 г/мл.
Решение.1. Определим сm(AgNO3):
Примем m(р-ра)= 100г, тогдаm(AgNO3)=ω(AgNO3)=2г;
m(H2O)= 100- 2= 98г;
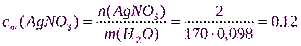 моль/кг;
моль/кг;
M(AgNO3)=170 г/моль;
2.Определим iпо формуле (16):AgNO3=Ag++NO3–;k=2;
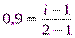 ; i=1,9
; i=1,9
3. Определим DТкиппо формуле (10):
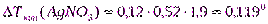
4. Ткип(AgNO3)= 373 + 0,119 = 373,1190
Пример 8а.Определите осмотическое давление раствораAgNO3, при 200С, еслиω(AgNO3)= 2%,α(AgNO3) = 90%,ρ(р-ра) = 1 г/мл.
Решение.1. Определим с(AgNO3) по формуле (4):
Из примера 8 m(р-ра)= 100г,m(AgNO3) =2г
V(р-ра)= 100/ 1= 100 мл = 0,1 л;
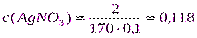 моль/л
моль/л
2. Определим pосм(AgNO3) по формуле (15):
Из примера (8) i=1,9; Т=293К
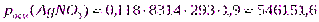 Па
Па
Пример 8б.Определите давление насыщенного пара над растворомAgNO3при 200С, если р0(Н2О)=2337,8 Па,ω(AgNO3)= 2%,α(AgNO3) = 90%,ρ(р-ра) = 1 г/мл.
Решение.Из примера 8m(AgNO3)=2г;m(H2O)= 98г;
1. Определим x(В)
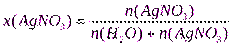 ;
;
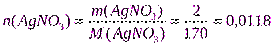 моль
моль
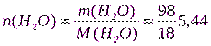 моль;
моль; 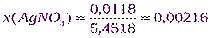
2. Определим Dpпо формуле (12):
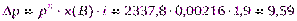 Па
Па
3. Определим pпо формуле (8а):
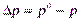 ;
; 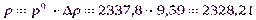 Па
Па
Пример 9.При 00С осмотическое давление 0,1н раствора К2СО3равно 272 кПа. Определите степень диссоциации карбоната калия в этом растворе.
Решение.1.Рассчитаемc(B) по формуле (4):
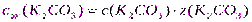 ;
; 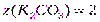
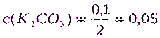 моль/л
моль/л
2. Рассчитаем iпо формуле (15):
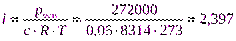
3.Рассчитаем aпо формуле (16):
K2CO3= 2K++CO32-;k = 3;
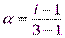 ;α= 0,699.
;α= 0,699.
Пример 10.Определите моляльую концентрацию раствораKCl, если его водный раствор замерзает при -0,320C, аα(KCl)=66,5%.
Решение.
1. По формуле (9а) ΔТзам=0,320
2. Рассчитаем iпо формуле (16):
KCl = K+ + Cl–; k =2 ; 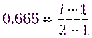 ; i = 1,665;
; i = 1,665;
3. Рассчитаем моляльную концентрацию по формуле (13):
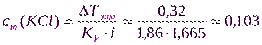 моль/кг;
моль/кг;
Коллигативные свойства растворов неэлектролитов
Раствор неэлектролита состоит из растворителя и растворенного вещества в виде недиссоциированных молекул. Коллигативными свойствами раствора неэлектролита являются свойства, которые зависят от концентрации и практически не зависят от природы неэлектролита. К таким свойствам относятся:
Относительное понижение давления насыщенного пара растворителя над раствором (Iзакон Рауля)
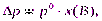 (8)
(8)
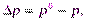 (8а)
(8а)
р0- давление насыщенного пара над чистым растворителем, Па;
р – давление насыщенного пара над раствором неэлектролита, Па;
х(В) – молярная доля неэлектролита в растворе;
Понижение температуры замерзания (IIзакон Рауля)
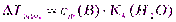 (9)
(9)
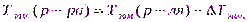 (9а)
(9а)
Кк– криоскопическая константа,Kk(H2O)=1,86 К×кг/моль
сm(B) – моляльная концентрация неэлектролита, моль/кг;
Повышение температуры кипения (IIзакон Рауля)
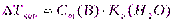 (10)
(10)
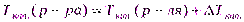 (10а)
(10а)
Кэ–эбуллиоскопическая постоянная, Кэ(Н2О)=0,52 К×кг/моль
Осмотическое давление раствора (закон Вант-Гоффа)
pосм= с(В)×R×T, Па (11)
R= 8,314 л×Па/моль×К, Т – температура, К
с(В) – молярная концентрация неэлектролита, моль/л
Пример 5.Давление насыщенного пара воды при 500С равно 12334 Па. Вычислите давление насыщенного пара воды над раствором, содержащим 50г этиленгликоляC2H4(OH)2в 900г воды. Определите температуру замерзания этого раствора.
Решение.1.Рассчитаем молярную долю вещества в растворе по формуле (3):
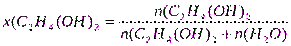
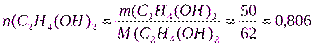 моль;
моль;
M(C2H4(OH)2= 62 г/моль;
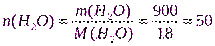 моль, М(Н2О)= 18 г/моль;
моль, М(Н2О)= 18 г/моль;
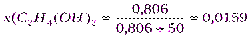 ;
;
2.Рассчитаем понижение давления насыщенного пара:
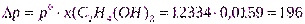 Па;
Па;
3.Рассчитаем давление насыщенного пара над раствором:
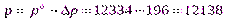 Па;
Па;
4.Определим DТзампо формуле (9):
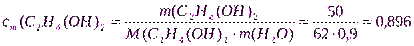
моль/кг; 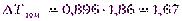 0
0
5.Определи Тзамраствора:
Тзам.(р-ра)= 0 – 1,67 = - 1,670
Пример 6.Сколько граммов глицерина С3Н8О3надо растворить в 2 л воды, чтобы получить раствор, закипающий при 100,60С?
Решение.
1. Определим DТкиппо формуле (10а):
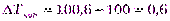 0
0
2. Определим сm(В):
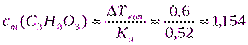 моль/кг
моль/кг
3. Определим n(В) по формуле (6):
n(C3H8O3) = 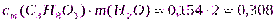 моль;m(H2O)=V∙ρ=2000∙1=2000г=2кг;
моль;m(H2O)=V∙ρ=2000∙1=2000г=2кг;
4.Определим массу глицерина:
m(C3H8O3) =nM(C3H8O3) =0,308×92= 28,336 г
M(C3H8O3) =92 г/моль
Пример 7.При 420С давление насыщенного пара воды равно 2,34 кПа. На сколько понизится давление насыщенного пара воды над раствором при указанной температуре, если в 540г воды растворить 36г глюкозы.
Решение.1. Определимx(В) по формуле (3):
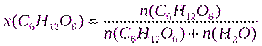 ;
;
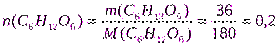 моль
моль
М(С6Н12О6)= 180г/моль;
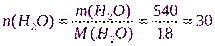 моль
моль
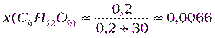
2. Рассчитаем Dpпо формуле (8а):
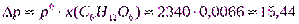 Па
Па
Первый закон Рауля
Пар, находящийся в равновесии с жидкостью, называют насыщенным. Давление такого пара над чистым растворителем (p0) называют давлением или упругостью насыщенного пара чистого растворителя.

Франсуа Мари Рауль
В 1886 (1887) году Ф. М. Рауль сформулировал закон:
Давление пара раствора, содержащего нелетучее растворенное вещество, прямо пропорционально мольной доле растворителя в данном растворе:
p = p0 · χр-ль, где
p — давление пара над раствором, Па;
p0 — давление пара над чистым растворителем;
χр-ль —— мольная доля растворителя.
