Методи кількісного визначення.
Державна фармакопея України, її структура. Параметри якості, які використовуються для стандартизації лікарських речовин (опис, розчинність, ідентифікація та інш.). Реакції ідентифікації на іони згідно ДФУ
| 1. Калію хлорид ідентифікують за іоном калію реакцією з: A *тартратною кислотою B цинкуранілацетатом C срібла нітратом; D натрію гідроксидом; E калію феріціанідом | До дають розчин винної кислоти, розчин натрію ацетату, 95% спирт і взбовтують; утворюється білий уристалічнийосад, розчинний у мінеральних кислотах і лугах: 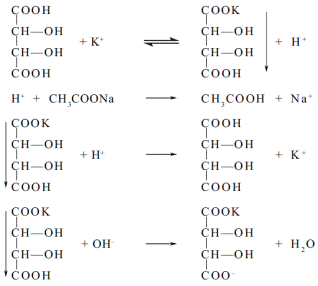 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.9 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.9 |
| 2. Солі калію внесені в безбарвне полум”я газового пальника забарвлюють його в колір A *фіолетовий B червоний C цеглястий D жовтий E зелений | Солі калію внесені в безбарвне полум”я газового пальника забарвлюють його в фіолетовий колір, при розгляданні через синє скло – у пурпурово червоний. «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.10 |
| 3. Яким реактивом можна ідентифікувати калій в Калію ацетаті? A *натрію гексанітрокобальтатом B амонію оксалатом C барію хлоридом D натрію гідроксидом; E магнію сульфатом | До розчину субстанції, попередньо прожареної для видалення солей амонію, додають розведену оцтову кислоту і натрію гексанітрокобальтат, утворюється жовтий осад: 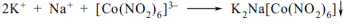 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.10 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.10 |
| 4. Хімік може підтвердити в препараті,що містить залізо (II), наявність останнього реакцією з: A* розчином калію ферроціанидом B розчином калію ціаніду C розчином калію хлориду D розчином калію тіоціанат E розчином калію броміду | До солі 2-х валентного феруму додають розведену хлороводневі кислоту і калію ферроціанід; утворюється синій осад, нерозчинний у мінеральних кислотах, але руйнується лугами з утворенням феруму (П) гідроксиду: 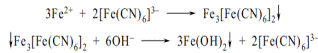 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.8 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.8 |
| 5. Наявність у складі лікарської форми катіона заліза (II) може бути підтверджено провізором-аналітиком аптеки за допомогою розчину: A* амонію сульфіду B натрію хлориду C магнію сульфату D калію броміду E натрію витрати | До солі 2-х валентного феруму додають розчин амонію сульфіду, утворюється чорний осад, розчиний у розведених у мінеральних кислотах: 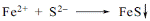 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.8 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.8 |
| 6. Наявність іонів бісмуту в дерматолі підтверджують реакцією в кислому середовищі з: A * натрію сульфідом B амонію оксалатом C барію хлоридом D аргентуму нітратом E калію нітратом | З натрію сульфідом в кислому середовищі іони вісмуту утворюють черно-коричневий осад, який розчиняється при додаванні рівного об’єму концентрованої нітратної кислоти:  «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.7-8 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.7-8 |
| 7. Провізор-аналітик аналізує ксероформ. Який з наведених реактивів він може використати для ідентифікації бісмуту у складі ксероформу? A *натрію сульфід B барію хлорид C амоніаку гідрооксид D калію натрію тартрат E міді сульфат | З натрію сульфідом в кислому середовищі іони вісмуту утворюють черно-коричневий осад, який розчиняється при додаванні рівного об’єму концентрованої нітратної кислоти:  «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.7-8 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.7-8 |
| 8. Провізор-аналітик при ідентифікації ксероформу провів реакцію з натрію сульфідом; при цьому утворився чорний осад. Вкажіть, який іон він виявив: A *Бісмуту B Плюмбуму C Цинку D Купруму E Аргентуму | З натрію сульфідом в кислому середовищі іони вісмуту утворюють черно-коричневий осад, який розчиняється при додаванні рівного об’єму концентрованої нітратної кислоти:  «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.7-8 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.7-8 |
| 9. Провізор–аналітик для ідентифікації цинку сульфату додав розчин натрію сульфіду. Що при цьому спостерігається? A *Випадіння білого осаду B Випадіння чорного осаду C Поява зеленої флюорисценції D Виділення бульбашок газу E Поява жовтого забарвлення | Це реакція на Zn2+. Утворюється білий осад, легко розчинний в розведеній хлористоводневій кислоті, нерозчинний в розведеній оцтовій кислоті: 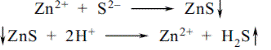 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.13 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.13 |
| 10. Для ідентифікації хлорид-йону в хлоридній кислоті АНД пропонує проводити реакцію з наступним реактивом A *діоксидом марганцю B хроматом калію C нітратом калію D сульфатом калію E молібдатом амонію | При нагріванні субстанції з мангану діоксином виділяється вільний хлор, який ідентифікують за запахом: 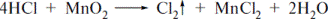 «Фармацевтична хімія»; під заг. ред.проф. Безуглого П.О. с.73 «Фармацевтична хімія»; під заг. ред.проф. Безуглого П.О. с.73 |
| 11. Хлорид-іони виявляють розчином аргентуму нітрату в кислому середовищі в присутності кислоти: A * нітратної B сульфатної C фосфатної D оцтової E сульфітної | Хлорид-іони виявляють з розчином аргентуму нітрату в в присутності розведеної нітратної кислоти; утворюється білий сирнистий осад, нерозчинний у нітратній кислоті і розчинний у розчині амоніаку: 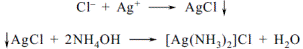 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.20 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.20 |
| 12. Провізор-аналітик підтверджує наявність хлорид-іона в молекулі клофеліну реакцією з нітратом срібла. Утворюється білий осад,який розчиняється в розчині: A* аміаку B кислоти азотної C натрію нітрату D формальдегіду E натрію гідроксиду | Хлорид-іони виявляють з розчином аргентуму нітрату в в присутності розведеної нітратної кислоти; утворюється білий сирнистий осад, нерозчинний у нітратній кислоті і розчинний у розчині амоніаку: 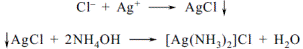 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.20 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.20 |
| 13. Для встановлення ідентифікації дифенгідраміну гідрохлориду використовують якісну реакцію на хлориди з: A *аргентуму нітратом B натрію сульфатом C калію карбонатом D калію перманганатом E натрію гідроксидом | Хлорид-іони виявляють з розчином аргентуму нітрату в в присутності розведеної нітратної кислоти; утворюється білий сирнистий осад, нерозчинний у нітратній кислоті і розчинний у розчині амоніаку: 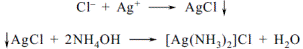 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.20 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.20 |
| 14. З метою ідентифікації сульфогрупи в молекулі сульфокамфорної кислоти її нагрівають з карбонатом і нітратом натрію. В результаті реакції утворюється сполука, яку провізору слід ідентифікувати з наступним реактивом: A *барію хлоридом B натрію сульфідом C амонію молібдатом D аргентуму нітратом E кобальту (ІІ) хлоридом | Утворюються сульфати SO42-, які реагують з барію хлоридом з утворенням біого осаду, нерозчинного у розведених мінеральних кислотах: 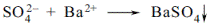 Реакція проводиться у солянокислому середовищі для розчинення осадів барію фосфатів і карбонатів, які на відміну від барію сульфату розчинні у соляній кислоті. «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.18 Реакція проводиться у солянокислому середовищі для розчинення осадів барію фосфатів і карбонатів, які на відміну від барію сульфату розчинні у соляній кислоті. «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.18 |
| 15. Наявність сульфат-іону в ЛЗ виявляють розчином барію хлориду в присутності: A * розведеної хлороводневої кислоти B льодяної оцтової кислоти C концентрованої нітратної кислоти D розведеної фосфатної кислоти E розведеної нітратної кислоти | Сульфати SO42-, які реагують з барію хлоридом з утворенням біого осаду, нерозчинного у розведених мінеральних кислотах: 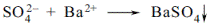 Реакція проводиться у солянокислому середовищі для розчинення осадів барію фосфатів і карбонатів, які на відміну від барію сульфату розчинні у соляній кислоті. «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.18 Реакція проводиться у солянокислому середовищі для розчинення осадів барію фосфатів і карбонатів, які на відміну від барію сульфату розчинні у соляній кислоті. «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.18 |
| 16. Для підтвердження наявності сульфат-іона в лікарському речовині "Магнію сульфат "провізор використовує наступні реактиви: A* розчин барію хлориду і кислоту хлористоводневу B розчин амонію хлориду і аміак C розчин срібла нітрату і кислоту азотну D розчин бензолсульфокислота E розчин діфеніламіна | Сульфати SO42-, які реагують з барію хлоридом з утворенням біого осаду, нерозчинного у розведених мінеральних кислотах: 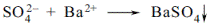 Реакція проводиться у солянокислому середовищі для розчинення осадів барію фосфатів і карбонатів, які на відміну від барію сульфату розчинні у соляній кислоті. «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.18 Реакція проводиться у солянокислому середовищі для розчинення осадів барію фосфатів і карбонатів, які на відміну від барію сульфату розчинні у соляній кислоті. «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.18 |
| 17. Фторафур використовується для лікування злоякісних пухлин шлунку та інших відділів шлунково-кишкового тракту. Фторид--іон можна визначить після попередньої мінералізації по утворенню осаду з: A *Кальцію хлоридом B Амонію гідроксидом C Калію нітратом D Натрію карбонатом E Калію хлоридом | Після мінералізації з сумішю для спікання залишок розчиняють і при рН = 4,0-5,0 додають розчин кальцію хлориду: 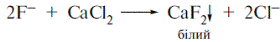 «Фармацевтична хімія»; під заг. ред.проф. Безуглого П.О. с.349 «Фармацевтична хімія»; під заг. ред.проф. Безуглого П.О. с.349 |
| 18. Атом фтору у фторурацилі відкривають після мінералізації за утворенням білого осаду з катіонами: A * Кальцію B Калію C Натрію D Літію E Амонію | Після мінералізації з сумішю для спікання залишок розчиняють і при рН = 4,0-5,0 додають розчин кальцію хлориду: 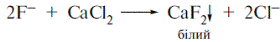 «Фармацевтична хімія»; під заг. ред.проф. Безуглого П.О. с.349 «Фармацевтична хімія»; під заг. ред.проф. Безуглого П.О. с.349 |
| 19. На аналіз надійшла субстанція магнію карбонату легкого. За допомогою якого реактиву можна підтвердити наявність в ньому катіона магнію? A * динатрію гідрофосфату B калію гідросульфату C калію гідрофталата D амонію тіоціанат E натрію тетрафенілбората | До розчину додають розчини амонію хлориду, амоніаку і динатрію гідро фосфату, утворюється білий кристалічний осад, розчиний у мінеральних та оцтовій кислотах: 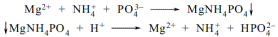 Амонію хлорид додається для запобігання утворення осаду магнію гідроксиду. Але й надлишку амонію хлориду слід уникати, так як можуть утворюватись розчинні комплекси [MgCl3]- і [MgCl4]2-. «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.10 Амонію хлорид додається для запобігання утворення осаду магнію гідроксиду. Але й надлишку амонію хлориду слід уникати, так як можуть утворюватись розчинні комплекси [MgCl3]- і [MgCl4]2-. «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.10 |
| 20. Оберіть назву реактиву, який використовується для проведення ідентифікації ацетат-іонів за вимогами ДФУ. A * Кислота щавлева B Кислота метоксифенілотцова C Кислота саліцилова D Кислота азотна E Кислота бензойна | Субстанцію нагрівають з рівною кількістю кислоти щавелевої. Утворюється оцтова кислота, яку визначають за запахом і кислою реакцією.  ДФУ-1, с.68 ДФУ-1, с.68 |
| 21.Оберіть назву реактиву, який використовується для ідентифікації сульфіт-іонів за вимогами ДФУ. A * Кислота хлористоводнева розведена B Кислота щавлева C Кислота борна D Кислота азотна розведена E Кислота сульфосаліцилова | До розчину, що містить SO32- розведену хлористоводневу кислоту і збовтують, поступово виділяється сірчистий газ з характерним різким запахом: 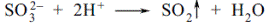 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с. 19 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с. 19 |
| 22. Для проведення ідентифікації лікарських засобів до складу яких входить сульфіт-іон провізор до розчину лікарської сполуки додає кислоту хлористоводневу і спостерігає: A виділення газу з різким запахом B виділення газу бурого кольору C появу жовтого забарвлення розчину D появу жовтого осаду E появу білого осаду | До розчину, що містить SO32- розведену хлористоводневу кислоту і збовтують, поступово виділяється сірчистий газ з характерним різким запахом: 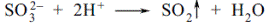 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с. 19 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с. 19 |
| 23. Провізор проводить ідентифікацію лікарської речовини за сульфіт-іонами згідно до вимог ДФУ. Який реактив знебарвлюється під час цього дослідження? A * Розчин йоду B Розчин заліза (III) хлоріду C Розчин аміаку D Розчин калію йодиду E Розчин калію нітрату | При додаванні до сульфіду 0,1 М розчину йоду відбувається його знебарвлення: 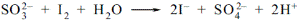 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с. 19 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с. 19 |
| 24. Для виявлення тіосульфат–іону, провізор додав надлишок реактиву, при цьому утворився білий осад, який повільно жовтів, бурів, чорнів. Який розчин додав провізор? A * аргентуму нітрату B барію хлориду C амонію оксалату D плюмбуму (ІІ) ацетату E дифеніламіну | При додаванні срібла нітрату : 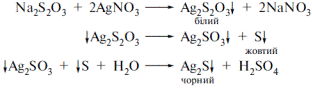 Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. с.89 Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. с.89 |
| 25. В ЛЗ катіон кальцію можна виявити з допомогою розчину A * амонію оксалату B аргентуму нітрату C калію перманганату D натрію нітриту E натрію хлориду | З розчином амонію оксалату солі кальцію утворюють білий осад, нерозчинний у розведеній оцтовій кислоті і розчині амоніаку, розчиний у розведених мінеральних кислотах: 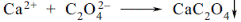 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с. 10 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с. 10 |
| 26. Однією з реакцій ідетинфікації ЛЗ, які вміщують катіон кальцію згідно вимог ДФУ є реакція з: AгліоксальгідроксіаніломB гідроксихіноліном C гідроксиламіном D алізаріном E кислотою сульфатною | До нейтрального розчину субстанції додають розчин гліоксальгідроксіанілу у сnирті, розчин натрію гідроксиду розведеного і розчин натрію карбонату. Суміш струшують з хлороформом і додають воду; хлороформний шар набуває червоного забарвлення 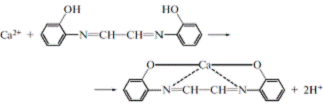 ДФУ-1, с.70 ДФУ-1, с.70 |
| 27. Для проведення ідентифікації ЛЗ до складу яких входить фосфат-іон, провізор використовує розчин: A аргентуму нітрату B амоніаку C ртуті нітрату D калію хлориду E натрію гідроксиду | Фосфат-іон з розчином арґентуму нітрату утворює жовтий осад, розчиний у розведеній нітратній кислоті і розчині амоніаку:  «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.19 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.19 |
| 28. Катіон натрію в натрію хлориді при внесенні в полум’я газового пальника забарвлює його в колір A *жовтий B цеглястий C фіолетовий D червоний E зелений | Катіон натрію в натрію хлориді при внесенні в полум’я газового пальника забарвлює його в жовтий колір «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.12 |
| 29. Катіон натрію в натрію цитраті ідентифікують за утворенням білого осадуз: A *калію піроантимонатом B барію хлоридом; C заліза [ІІІ] хлоридом; D аргентуму нітратом; E калію фероціанідом | Натрій з калію піроантимонатом (калію гексагідроксистибіату(V)) утворює білий осад: 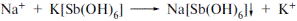 Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. с.45 Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. с.45 |
| 30. Для ідентифікації ЛЗ, що містить карбонат-іон, згідно з вимогами ДФУ, провізор повинен використовувати наступний реактив: A *кислоту оцтову розведену B реактив Несслера C розчин калію йодиду D розчин натрію гідроксиду E розчин натрію хлориду | В результаті реакції карбонат іону з розведеною оцтовою кислотою виділяється вуглекислий газ, який утворює білий осад при пропусканні крізь вапняну воду: 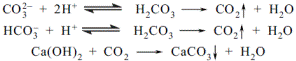 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.16 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.16 |
| 31. З допомогою якого реактиву можна розрізнити розчини карбонату і гідрокарбонату натрію? A *Магнію сульфат B Натрію сульфат C Натрію хлорид D Калію йодид E Калію хлорат | 1.Розчин карбонату з насиченим розчином магнію сульфату утворює білий осад, а розчин гідрокарбонату утворює з насиченим розчином магнію сульфату білий осад тільки при кипятінні: 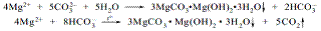 2. Розчин карбонату (1:10) забарвлюється у червоний колір при додаванні краплі розчину фенолфталеїну, а розчин гідрокарбонату – ні. «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.16 2. Розчин карбонату (1:10) забарвлюється у червоний колір при додаванні краплі розчину фенолфталеїну, а розчин гідрокарбонату – ні. «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001, с.16 |
| 32. Який реактив використовується під час проведення ідентифікації іонів арсену за вимогами ДФУ. A * Реактив гіпофосфіту B Розчин калію йодвісмутату C Розчин натрію гідроксиду D Реактив тіоацетаміду E Розчин альфа-нафтолу | 5 мл випробовуваного розчину нагрівають на водяній бані з рівним об'ємом реактиву гіпофосфіту,утворюється коричневий осад: 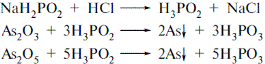 ДФУ-1, с.68 ДФУ-1, с.68 |
| 33. Згідно з вимогою ДФУ, реакцію ідентифікації йодид-іонів проводять в середовищі розведеної сульфатної кислоти в присутності хлороформу дією A *K2Cr2O7 B K2SO4 C NH4NO3 D Na2CO3 E NaSCN | Утворюється йод:  Який забарвлюєх хлороформний шар у фіолетовий або червоно-фіолетовий колір. Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. с.42 Який забарвлюєх хлороформний шар у фіолетовий або червоно-фіолетовий колір. Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. с.42 |
Методи кількісного визначення.
| 1. Виберіть лікарську речовину, яку можна визначити методом перманганатометрії A * Пероксид водню B Сульфат магнію C Нікотинова кислота D Парацетамол E Новокаїн | Пряма перманганатометрія без індикатору, Ѕ=2,5: 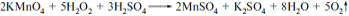 Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. |
| 2. Провізору перед прямим броматометричним визначенням миш'яковистого ангідриду, згідно вимогам АНД, до досліджуваного розчину необхідно додати: A* калію бромід B калію нітрат C натрію хлорид D натрію тіосульфат E натрію гідроксид | Пряма броматометрія з контрольним дослідом, індикатор- метиловий червоний, Ѕ=3/2. В точці еквівалентності індикатор знебарвлюється: 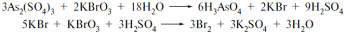 Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. |
| 3. Провізор-аналітик визначає кількісний вміст ЛЗ зворотним йодометричним методом. Який з перерахованих титрованих розчинів він повинен використовувати? A *натрію тіосульфат B срібла нітрат C натрію нітрит D натрію едетат E калію бромат | Методом зворотної йодометрій можна визначати сполуки, які повільно окислюються йодом (ізоніазид), утворюють з ним комплексні сполуки (кофеїн), дають реакцію ароматичого заміщення (антипірин), або потребують для стехіометричного необоротного окиснення лужного середовища (формальдегід, глюкоза, фурацилін). В останьому випадку окиснення йде за схемою: 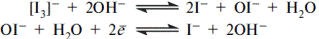 Після завершення реакції надлишок йоду відтитровують натрію тіосульфатом. Якщо окиснення йшло в лужному середовищі, до реакційної суміші спочатку додають надлишок кислоти, а потім йод, що виділився, відтитровують натрію тіосульфатом: Після завершення реакції надлишок йоду відтитровують натрію тіосульфатом. Якщо окиснення йшло в лужному середовищі, до реакційної суміші спочатку додають надлишок кислоти, а потім йод, що виділився, відтитровують натрію тіосульфатом: 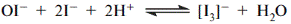 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001 «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001 |
| 4. Провізору-аналітику необхідно провести аналіз очних крапель, до складу яких входить калію йодид. Для його кількісного визначення використовується метод: A *аргентометріі B комплексонометрії C перманганатометрія D кислотно-основного титрування E нітрітометріі | Аргентометрія за методом Фаянса, індикатор – натрію еозинат, Ѕ=1: К 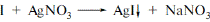 В точці еквівалентності осад стає рожевим внаслідок адсорбції на ньому індикатору. Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. В точці еквівалентності осад стає рожевим внаслідок адсорбції на ньому індикатору. Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. |
| 5. Провізор-аналітик проводить кількісне визначення субстанції срібла нітрату методом тіоціанатометріі. В якості індикатора в цьому випадку використовується: A *заліза (III) амонію сульфат B натрію еозінат C калію хромат D фенолфталеїн E розчин крохмалю | Пряма тіоціонатометрія, індикатор – залізоамонієвий галун (заліза (III) амонію сульфат); титрують в середовищі розведеної нітратної кислоти до жовто-червоного забарвлення, Ѕ=1: 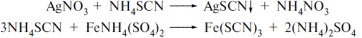 Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. |
| 6. При проведенні кількісного визначення калію хлориду аргентометричним методом (зворотне титрування) згідно ДФУ в якості індикатора використовується: A * заліза (III) амонію сульфат B діфенілкарбазон C калію хромат D фенолфталеїн E натрію еозінат | Звортня аргентометрія за Фольгардом в присутності дибутилфталату, , індикатор – залізоамонієвий галун (заліза (III) амонію сульфат); перерахунок ведуть на суху речовину, Ѕ=1: KCl +AgNO3→ AgCl↓ + KNO3  Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. |
| 7. Кількісний вміст натрію йодиду згідно ДФУ визначають методом: A * йодатометріі B аргентометріі C нітритометріі D перманганатометрія E броматометріі | Пряма йодатометрія. Титрують розчином калію йодиду в присутності хлористоводневої кислоти до переходу червоного забарвлення в жовте. Додають хлороформ і титрують до знебарвлення хлороформного шару. Перерахунок ведуть на суху речовину, S=2: 2NaI+KIO3+6HCl→3ICl+3NaCl+3H2O Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. |
| 8. Провізор-аналітик визначає кількісний вміст ЛЗ зворотним броматометричним методом. Який з перерахованих титрованих розчинів він повинен використати: A * Натрію тіосульфат B Калію бромат C Натрію едетат D Натрію нітрит E Аргентуму нітрат | Зворотнім броматометричним методом визначають речовини, які повільно реагують з бромом (феноли, ароматичні аміни). До розчину речовини додають розчин калію броміду, калію бромату, сульфатну або хлороводневі кислоту. Бром, що виділився, вступає в реакцію електрофільного заміщення. Надлишок брому визначають йодометрично – додають калію йодид, і йод, що виділився, відтитровують натрію тіосульфатом. «Фармацевтичний аналіз», під заг. ред. П.О. Безуглого, Харків, 2001 |
| 9. ЛП з групи алкалоїдів, кількісно визначають методом ацидиметрії у неводному середовищі. Титрантом виступає: A * Хлорна кислота B Натрію тіосульфат C Сірчана киислота D Диметилформамід E Азотно-кисле срібло | В якості титранту використовують хлорну кислоту - НСІО4 |
| 10. Загальним методом визначення кількісного вмісту препаратів з групи галогенідів лужних металів є: A *аргентометрія B перманганатометрія C комплексонометрія D алкаліметрія E нітритометрія | Аргентометрія базується на реакції утворення осадів хлорид-, бромід-, йодид-, тіоціонат-іонів з солями арґентуму. Визначення точки еквівалентності проводиться візуально за допомогою індикаторів або потенціометрично. Застосовуються індикатори, які утворюють забарвлені осади або комплекси або ж адсорбційні індикатори. |
| 11. Для кількісного визначення субстанції фторурацилу згідно ДФУ використовують метод неводного титрування. Який титрований розчин йому необхідно використати? A *Тетрабутиламонію гідроксиду B Натрію нітриту C Калію бромату D Амонію тіоціанату E Натрію едетату | Пряма алкаліметрія в неводному середовищі, індикатор тимоловий синій, Ѕ=1. Титрують розчином тетрабутиламонію гідроксиду [N(C4H9)4]OH в середовищі ДМФА, паралельно проводять контрольний дослід. ДФУ 1.0, с. 469 |
| 12. Кількісний вміст дифенгідраміну гідрохлориду у відповідності з вимогами ДФУ визначається методом алкаліметріі. В якості титранту використовується розчин: A * натрію гідроксиду B калію бромата C натрію тіосульфату D калію перманганату E кислоти хлористоводневої | 0.250 г субстанції розчиняють у 50 мл 95% спирту,додають 5.0 мл 0.01 M розчину кислоти хлористоводневої, титрують 0.1М розчином натрію гідроксиду потенціометрично. До розрахунку беруть об'єм титранту між двома стрибками потенціалів на кривій титрування. ДФУ 1.2, с. 430 |
| 13. При проведенні кількісного визначення кислоти аскорбінової йодометричним методом згідно ДФУ в якості індикатора використовується: A * крохмаль B діфенілкарбазон C бромфеноловий синій D фенолфталеїн E мурексиду | 0,150 г субстанції розчиняють у суміші 10 мл кислоти сірчаної розведеної і 80 мл води, вільної від вуглецю діоксиду. Додають 1 мл розчину крохмалю і титрують 0,05 М розчином йоду до одержання стійкого синьо-фіолетового забарвлення. 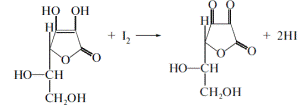 ДФУ 1.0, с. 388 ДФУ 1.0, с. 388 |
| 14. Індикатором при зворотному йодхлорметричному методі кількісного визначення етакридину лактату є: A *Крохмаль B Тропеолін 00 C Метиловий черв. D Бромтимоловий синій E Метиловий оранж. | Зворотня йодохлорметрія, індикатор – крохмаль, Ѕ=1/2: 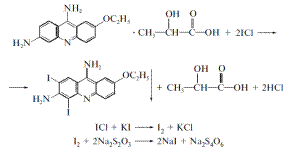 Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. Фармацевтична хімія; під заг. ред.проф. Безуглого П.О. |
