Скорость химической реакции. Классификация химических реакций.
Материалы к занятию №7
Классификация химических реакций.
Химическая кинетика. Учение о скорости химической реакции.
Химическое равновесие. Принцип Ле Шателье
Термохимия. Тепловой эффект химической реакции.
Домашнее задание:
1.Теория:
А.С.Егоров Химия. Репетитор, 2013:
§ 4,2(задания для самостоятельной работы №1-4),
§ 4,3 (задания для самостоятельной работы № 2-6),)
§ 4,4 (задания для самостоятельной работы № 3-5),)
§ 4,5 (задания для самостоятельной работы № 1-3),
2.Упражнения:
В.Н. Доронькин и др. Тренировочная тетрадь"Общая химия;" Ростов-на-Дону, Легион ,2013
1) раздел 8 с101-108 №№ 8.1-8.3,
2) раздел 9 с109-110 №№ 9.1-9.4
3) раздел 10 с111-112 №№ 10.1-10.4
1) раздел 11 с121-124 №№ 11.2.16 -11.2.28,
.
Тесты
1.В.Н. Доронькин и др. Химия Тематические тесты. Базовый и повышенный уровень,Ростов-на- Дону, Легион , 2014
Вопрос А19 ( типы реакций)
Вопрос А20 ( скорость химической реакции)
Вопрос А21 ( химическое равновесие)
Вопрос А28 ( расчеты теплового эффекта реакции)
2.ЕГЭ. Химия Типовые экзаменационные варианты, под редакцией А.А. Кавериной 2015,
Вопрос 18 ( типы реакций)
Вопрос 19 ( скорость химической реакции)
Вопрос 20 ( химическое равновесие)
Вопрос 25 ( расчеты теплового эффекта реакции)
(варианты с 1 по 30)
Электронные тесты
4.Любые другие тесты - рассматриваемые темы .
Тесты
Типы химических реакций
Тест 1
1. Взаимодействие водорода с хлором относится к реакциям
1) разложения, экзотермическим 2) обмена, эндотермическим
3) соединения, эндотермическим 4) соединения, экзотермическим
2. Какому типу реакции соответствует уравнение Zn + H2SO4 = ZnSO4 + H2
1) обмена 2) соединения 3) разложения 4) замещения
3.Укажите схемы реакций соединения:
1) Fe(ОН)3 →Fe2O3 +Н2О
2) AgNO3 → Ag + О2 + NO2
3) SO2 + О2→ SO3
4) NO2 +О2+Н2О→ НNO3
4. Какому типу реакции соответствует уравнение Zn(OH)2 + Н2SO4 = ZnSO4 + 2H2O
1) обмена 2) соединения 3) разложения 4) замещения
5. Какое из приведенных уравнений соответствует реакции нейтрализации
1) BaCO3 + 2HCl = BaCl2 + CO2 + H2O 2) Na2SO4 + Ba(OH)2 = BaSO4 + 2NaOH
3) CaCl2 + Na2CO3 = CaCO3 + 2NaCl 4) 3NaOH + H3PO4 = Na3PO4 + 3H2O
6. Горение аммиака 4NH3(г) + 3О2(г) =2N2(г)+ 6Н2О(ж) + Q является реакцией
1) соединения, каталитической, эндотермической
2) замещения, каталитической, экзотермической
3) ок-восст. некаталитической, экзотермической
4) обмена, некаталитической, эндотермической
7. Укажите схемы реакций, для проведения которых используется катализатор:
1) KOH +H2SО4→К2SО4 + Н2О
2) N2+Н2→NH3
3) NH3 + О2→ NO+Н2О
4)NH3 + О2 → N2 + Н2О
8. Какое из приведенных уравнений соответствует реакции нейтрализации
1) BaCO3 + 2HCl =BaCl2 + CO2 + H2O 2) Ba(OH)2 + H2SO4 = BaSO4 +2H2O
3) CaCl2 + Na2CO3 = CaCO3 + 2NaCl 4) 3NaOH + FeCl3 = Fe(OH)3 + 3NaCl
9. Взаимодействие метана с хлором является реакцией
1) соединения, экзотермической 2) замещения, эндотермической
3) соединения, эндотермической 4) замещения, экзотермической
10. К необратимым реакциям относится взаимодействие между
1) N2 и H2 2) SO2 и O2 3) C и О2 4) Н2 и S
Тест2
1. Выберите уравнения или схемы гетерогенных реакций:
1) CaCO3(т) →CaO(т) + CO2(г)
2) СН4(г) +О2(г) →СО2 (г) + Н2О(ж)
3) FeS2(т) + О2(г) → Fe2О3(т) + SO2(г)
4)KOH(р-р) + НNO3(р-р) →КNO3(р-р) +Н2О(ж)
2. Гомогенной экзотермической окислительно-восстановительной реакцией является:
1) нейтрализация водного раствора едкого натра соляной кислотой
2) взаимодействие оксида азота (IV) с водой в присутствии кислорода
3) синтез монооксида азота из азота и кислорода
4) образование серной кислоты из серного ангидрида и воды
3. Какой из следующих процессов не является окислительно-восстановительным?
1) фотосинтез 3) коррозия металла
2) горение природного газа 4) гашение извести
4. Укажите уравнения или схемы реакций разложения:
1) НNO3 → Н2О + NO2 + О2
2) Fe + Cu(NO3) 2 → Fe(NO3) 2 + Cu
3)NaOH + HCl → NaCl + Н2О
4) Н2О2 → Н2О + О2
5. Реакцией замещения является образование воды в результате:
1) горения водорода в кислороде
2) восстановления оксида меди (II) водородом
3) взаимодействия гидроксида калия с серной кислотой
4) термической дегидратации гидроксида цинка
6. Выберите уравнения или схемы гомогенных реакций:
1) K(т) +Н2О(ж) → KOH(р-р) +Н2(г)
2) N2(г) +Н2(г) → NH3(г)
3) ВаС12 (р-р) + H2SО4 (р-р) → BaSO4(т) + 2НС1 (р-р)
4) Са(ОН)2 (р-р) + НС1 (р-р) → Н2О(ж) + СаС12 (р-р)
7. Правильной характеристикой реакции нейтрализации сильной кислоты сильным основанием, протекающей в водном растворе, является:
1) практически необратимая, гомогенная, экзотермическая реакция обмена
2) обратимая, гомогенная, экзотермическая реакция обмена
3) практически необратимая, гомогенная, эндотермическая реакция обмена
4) практически необратимая, экзотермическая реакция замещения
8. Дана следующая цепь превращений:
Fe 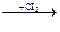 FeCl3
FeCl3 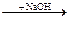 Fe(OH)3
Fe(OH)3 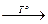 Fe2O3
Fe2O3 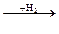 Fe
Fe
Реакции, с помощью которых осуществляются эти превращения, относятся соответственно к типам:
1) замещения, обмена, разложения, присоединения
2) присоединения, замещения, разложения, обмена
3) присоединения, обмена, разложения, замещения
4) присоединения, обмена, замещения, разложения
9. К какому из приведенных типов реакций можно отнести реакцию ионного обмена
1) разложения 2) замещения 3) нейтрализации 4) соединения
10. Взаимодействие кальция с соляной кислотой относится к реакциям
1) соединения, экзотермической
2) замещения, экзотермической
3) обмена, экзотермической
4) замещения, эндотермической
Тест 3
1. Укажите уравнения или схемы реакций замещения:
1) Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
2) Fe+H2SО4 → FeSО4 + Н2
3) CaCl2 + Na2CO3 → CaCO3 + 2NaCl
4) Al(NO3)3 → Al2O3 + NO2 + О2
2. Укажите уравнения или схемы экзотермических реакций:
1) N2+Н2→ NH3+Q
2) SO2 + О2 → SO3+Q
3) С + О2 → СО2 + 369 кДж
4) СаСО3 → СаО + СО2 - 157 кДж
3. Укажите уравнения или схемы реакций обмена:
1) NaOH + H2SО4→ Na2SО4 + Н2О
2) Ba(NO3)2 + K2SО4→ BaSО4 + KNO3
3) N2О5 + Н2О→ НNO3
4) CuO + 2НNO3 → Cu(NO3)2 + Н2О
4.Укажите уравнения или схемы окислительно-восстановительных реакций:
1) Al + Cl2 → AlCl3
2) BaCO3 → ВаO +СО2
3)Н2О2 → Н2О + О2
4) Cu + AgNO3→Cu(NO3)2 + Ag
5. Укажите уравнения или схемы необратимых реакций:
1) N2+3Н2→2NH3
2) Ba(OH)2 + H2SО4→ BaSО4 + Н2О
3) NaOH + HСl → NaCl + Н2О
4) SO2 + О2→ SO3
6.Реакция между карбонатом натрия и соляной кислотой является одновременно реакцией
1)замещения и необратимой
2)соединения и обратимой
3)обмена и необратимой
4) обмена и обратимой
7.Окислительно-восстановительной реакцией является разложение
1)гидрокарбоната кальция
2)хлорида аммония
3)перманганата калия
4)кремниевой кислоты
8.К реакциям замещения относится реакция взаимодействия брома с
1)водородом
2)магнием
3)этиленом
4) пропаном
9.К реакциям обмена относят
1)дегидрирование спиртов
2)галогенирование алканов
3)реакцию щелочных металлов с водой
4)реакцию нейтрализации
10.Взаимодействие оксида углерода (IV) c водой относится к реакциям
1)соединения, необратимым
2)обмена, необратимым
3)соединения, обратимым
4)обмена, обратимым
Скорость химической реакции
Тест 1
1. С наибольшей скоростью при обычных условиях протекает реакция
1) 2Ва + О2 = 2ВаО
 2) Ва2+ + СО32- = ВаС03
2) Ва2+ + СО32- = ВаС03
3) Ва + 2Н+ = Ва2+ + Н2
4) Ва + S = ВаS
2. Скорость химической реакции между медью и азотной кислотой зависит от
1) массы меди
2) объема кислоты
3) концентрации кислоты
4) увеличение давления
3. Для уменьшения скорости химической реакции необходимо
1) увеличить концентрацию реагирующих веществ
2) ввести в систему катализатор
3) повысить температуру
4) понизить температуру
4.Для увеличения скорости реакции 2СО + О2 = 2СО2 + Q необходимо
1) увеличить концентрацию СО
2) Уменьшить концентрацию O2
3) понизить давление
4) понизить температуру
5 .Для увеличения скорости химической реакции Mg(тв) + 2Н+→М g2+ + Н2(г) + 462 кДж .
необходимо
1) уменьшить концентрацию ионов водорода
2) увеличить концентрацию ионов водорода
3) понизить температуру
4) повысить давление
6. С наибольшей скоростью при комнатной температуре протекает реакция
1) углерода с кислородом
2) железа с раствором уксусной кислоты
3) железа с соляной кислотой
4) растворов гидроксида натрия и серной кислоты
7. На скорость химической реакции между раствором серной кислоты и железом не оказывает влияния
1) концентрация кислоты 2) измельчение железа
3) температура реакции 4) увеличение давления
8.Скорость гомогенной химической реакции пропорциональна изменению
1) концентрации вещества в единицу времени 2) количества вещества в единице объема
3) массы вещества в единице объема 4) объема вещества в ходе реакции
9. С большей скоростью идет реакция соляной кислоты с
1) медью 2) железом
3) магнием 4) цинком
10.Для увеличения скорости химической реакции Zn(тв) + 2Н+↔ Zn2+ + Н2(г)
необходимо
1) уменьшить концентрацию ионов цинка
2) увеличить концентрацию ионов водорода
3) уменьшить температуру
4) увеличить концентрацию ионов цинка
Тест 2
1.Катализатор повышает скорость реакции, потому что:
1) увеличивает число столкновений молекул реагентов в единицу времени
2) увеличивает скорость движения молекул реагентов
3)увеличивает энергию активации реакции
4) уменьшает энергию активации реакции
2. Для какой реакции кинетическое уравнение имеет
вид: v= k [O2]?
1) S + О2 → SO2 3) N2 + O2 → 2 NO
2) 2 Н2 + О2 → 2 Н2O 4) 2СО + O2 → 2 СO2
3. Константа скорости химической реакции зависит от:
1) температуры и концентрации реагирующих веществ
2) концентрации и природы реагирующих веществ
3) концентрации и площади поверхности соприкосновения реагирующих веществ
4) температуры и природы реагирующих веществ
4. Во сколько раз увеличится скорость одностадийной реакции А2 + В2 = 2AB при увеличении концентрации вещества A2 в 3 раза?
1) 3 2) 6 3) 9 4) 12
5. При уменьшении концентрации вещества A2 в 3 раза скорость одностадийной реакции 2A 2(г) + B2 (г) = 2A2B(г) :
1) увеличивается в 3 раза
2) уменьшается в 3 раза
3) увеличивается в 9 раз
4) уменьшается в 9 раз
6. Во сколько раз нужно увеличить внешнее давление, чтобы скорость одностадийной реакции А2(г) + 2В = 2AB возросла в 125 раз?
1) 5 2) 25 3) 100 4) 125
7. Как изменится скорость одностадийной реакции А(т) + В(г) = АВ(т) при увеличении давления в 4 раза?
1) не изменится
2) возрастет в 8 раз
3) возрастет в 4 раза
4) возрастет в 16 раз
8. Для какой одностадийной реакции увеличение концентрации вещества А в 2 раза приведет к увеличению скорости в 4 раза?
1) А2(г) + В2(г) = 2АВ(г)
2) А2(г) + В(т) = ВА2(т)
3) 2А2(г) = В(г)
4) 2А2(т) = В(г) + 2 С(г)
9. Увеличить скорость прямой реакции процесса N2(г) + ЗН2  2NH3(г) + Q можно, если повысить:
2NH3(г) + Q можно, если повысить:
1) температуру
2) давление
3) концентрацию водорода
4) концентрацию аммиака
10. Чему равен температурный коэффициент реакции γ, если при повышении температуры на 300C скорость химической реакции возрастает в 64 раза?
1) 2 2) 3 3) 4 4) 5
11. Во сколько раз надо увеличить концентрацию вещества А, чтобы при уменьшении концентрации вещества в два раза скорость одностадийной реакции
А (р-р) + 2В (р-р) = С (р-р) не изменилась?
1) 2 2) 4 3) 6 4) 8
12. При повышении температуры от 20 до 60°С скорость некоторой реакции увеличилась в 81 раз. Температурный коэффициент скорости этой реакции равен
1) 2 2) 3 3) 2,5 4)4
13. При повышении давления в 4 раза скорость реакции С (тв) + 2Сl2(г)=СС14(г) возрастает в . . . раз
1) 4 2)8 3)16 4)64
Тест 3 (Типа В)
1. Скорость химической реакции СН4 (г) + 2O2 (г) = СО2 (г) + 2H2O(г) при повышении концентрации исходных веществ в 3 раза увеличивается в . . . раз.(Ответ запишите цифрами).
2. Скорость синтеза аммиака при повышении концентраций азота и водорода в три раза увеличивается в . . . раз. (Ответ запишите цифрами).
3. Для того, чтобы скорость образования оксида азота (IV) по реакции 2NO2 + О2 = 2 NO2, возросла в1000 раз, давление в системе реакции нужно увеличить в . . . раз. (Ответ запишите цифрами).
4. При увеличении концентрации сероводорода в 5 раз скорость реакции
2 H2S (г) + SO2 (г) = 3 S (тв) + 2 Н2O (г)
возрастает в . . . раз. (Ответ запишите цифрами.)
5. Скорость реакции
Fe2O3 (тв) + 3 СО (г) = 2 Fe (тв) + 3 СО2 (г)
при увеличении концентрации СО в три раза возрастает в ... раз. (Ответ запишите цифрами.)
6. При уменьшении объема реакционного сосуда в 3 раза скорость реакции
2NO (г) + О2 (г) = 2NO2 (г)
возрастает в …. раз. (Ответ запишите цифрами)
7. При повышении температуры 30о скорость реакции, температурный коэффициент которой равен 2, возрастает в …. раз. (Ответ запишите цифрами).
8. Если температурный коэффициент скорости реакции равен 3, то для уменьшения скорости реакции в 27 раз нужно понизить температуру на . . .градусов. (Ответ запишите цифрами.)
9. При повышении температуры на 60°С скорость химической реакции увеличилась в 64 раза. Следовательно, температурный коэффициент этой реакции равен . . . (цифрами).
10. Скорость реакции увеличивается в 4 раза при повышении температуры на 10°С. Следовательно, при повышении температуры от 45°С до 75°С скорость реакции увеличится в ... раз. (Ответ запишите цифрами.)
Химическое равновесие
Тест1
1. В системе 2SO2(г) +O2 (г) « 2SO3 (тв) + Q смещение химического равновесия в сторону исходных веществ будет способствовать:
1) уменьшение давления
2) уменьшение То
3) увеличение [SO2]
4) уменьшение [SO2]
2. При повышении давления равновесие смещается вправо в системе:
1)2СО2(г) « 2СО(г) + О2(г)
2)С2Н4(г) « С2Н2(г)+ Н2(г)
3)PCl3(u) + Cl2(г) « PCl5(г)
4) H2(г) + Cl2(г) « 2HCl(г)
3. Изменение давления оказывает влияние на смещение равновесия в системе:
1)2SO2(г)+ O2(г)«SO3(тв)
2)2HI(г)«H2(г) + I2(г)
3)СО(г)+Н2О(г) «СО2(г)+Н2
4)N2(г)+O2(г)«2NO(г)
4. Обратимой реакции соответствует уравнение:
1)KOH +HCl=KCl+H2O
2) N2 + ЗН2 = 2NН3
3)FeCl3+3NaOH=Fe(OH)3+3NaCl
4) Na2O+2HCl=2NaCl+H2O
5. При одновременном повышении температуры и понижении давления химическое равновесие сместится вправо в системе:
1)H2(г)+S(г)«H2S(г)+Q
2) 2SO2(г)+O2(г)«2SO3(тв)+Q
3) 2NH3(г)«N2(г)+3H2(г)-Q
4) 2HCl(г)«Н2(г)=Cl2(г)-Q
6. При повышении давления равновесие смещается вправо в системе:
1) 2СО(г)«2СО(г)+О2(г)
2)С2Н4(г)«С2Н2(г)+Н2(г)
3)PCl3(г)+Cl2(г)«PCl5(г)
4) ) 2HCl(г)«Н2(г)=Cl2(г)
7.Чтобы химическое равновесие С4Н10(г)«С4Н8(г)+Н2(г)-Q сместить в сторону продуктов реакции надо:
1)повысить То и повысить Р
2)повысить То и понизить Р
3)понизить То и повысить
4) понизить и То, и Р
8. Химическое равновесие в системе 2NO(г)+O2(г)«2NO2(г)+Q смещается в сторону образования продукта реакции при
1) повышении давления 2) повышении То
3) понижении давления 4) применении катализатора
9. На смещение химического равновесия в системе N2+3H2«2NH3+Q не оказывает влияния
1)понижение То 2)повышение Р
3) удаление NН3 4)введение катализатора
10. Химическое равновесие системы СО2(г)+С(тв)«2СО(г)- Q сместится вправо при
1) повышении Р
2) понижении То
3)повышении [CO]
4) повышении То
Тест 2
1. Химическое равновесие - это состояние обратимой реакции, при котором:
1) константы скоростей прямой и обратной реакций равны
2) концентрации реагентов и продуктов реакции равны
3) скорости прямой и обратной реакций равны
4) скорость обратной реакции равна нулю
2. Обратимая реакция, равновесие которой смещается в одном направлении и при повышении температуры и при повышении давления - это:
1) N2 (г) + 3H2 (г) ↔ 2NH3 (г) + 92 кДж
2) 2NO (г) + О2 (г) ↔ 2NO2 (г) + 113 кДж
3) 2NO2 (г) ↔ N2O4 (г) – 9,6 кДж
4) СО (г) + Н2О (г) ↔ СО2 (г) + Н2 + 43 кДж
3.Добавление водорода в систему N2(Г) + ЗН2(Г) ↔2NH3(Г) + Q
1) увеличивает выход продукта реакции
2) смещает положение равновесия в сторону исходных веществ
3) не изменяет положения равновесия
4) ускоряет реакцию разложения аммиака
4.Химическое равновесие сместится вправо при увеличении давления в системе
1) Н2(Г) + Cl2(Г) ↔2HCl(Г)
2) CO2(Г) + C(ТВ) ↔2CO(Г)
3) 2NO(Г) + O2(Г) ↔2NO2(Г)
4) FeO(ТВ) + CO(Г) ↔Fe(ТВ) + СO2(Г)
5.В системе 2SO2 (Г) + O2(Г) 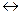 2SO3(Г) + Q химическое равновесие сместится вправо при:
2SO3(Г) + Q химическое равновесие сместится вправо при:
1) добавлении катализатора
2) повышении температуры
3) увеличении концентрации оксида серы (VI)
4) повышении давления
6.Для увеличения выхода продуктов реакции 2Pb(NO3)2(T) ↔ 2РbО(Т) + 4NO2(Г) + O2(Г) - Q
необходимо
1)увеличить температуру 3) увеличить давление
2)ввести катализатор 4) уменьшить температуру
7.Охлаждение системы и увеличение ее объема увеличивают выход продукта реакции
1) 2H2S(Г) + O2(Г) ↔ H2O(Г) + S(T) + Q
2) 4NH3(Г) + 5O2(Г) ↔ 4NO(Г) + 6Н2O(Ж) + Q
3) 2NO(Г) + O2(Г) ↔2NO2(Г) + Q
4) COCl2(Г) ↔ CO(Г) + Cl2(Г) + Q
8.Удаление оксида углерода (IV) при обжиге известняка СаСO3(Т) ↔ СаО(Т) + СO2(Г) - Q
1) уменьшает выход продуктов реакции
2) увеличивает скорость прямой реакции
3) смещает положение равновесия вправо
4) не влияет на положение равновесия
9.Уменьшение объема смещает положение равновесия в сторону образования продуктов реакции
1) СН3СНO (Г) + H2 (Г) ↔ СН3СН2OH (Г)
2) N2O4(Г) ↔ 2NO2(Г)
3) СН3СООCН(Ж) + H2O(Ж) ↔СН3СООН(Ж) + СН3ОН(Ж)
4) H2(Г) + S(T) ↔ H2S(Г)
10.При увеличении давления химическое равновесие не смещается в системе
1) CO(Г) + Сl2(Г) ↔ СОСl2(Г)
2) 2СО(Г) + O2(Г) ↔ 2СO2(Г)
3) СO2(Г) + C ↔ 2СО(Г)
4) С + O2(Г) ↔СО2(Г)
Тест 3
1.Для смещения равновесия в системе MgO(T) + CO2(Г) ↔ MgCO3(T) + Q в сторону продуктов реакции необходимо:
1) понизить давление
2) понизить температуру
3) повысить температуру
4) ввести катализатор
2.Химическое равновесие сместится в сторону образования продуктов как при понижении температуры, так и повышении давления в системе
1) 4NH3(Г) + O2(Г) ↔ 4NO(Г) + 6H2O(Г) + Q
2) 2SO2(Г) + O2(Г) ↔ 2SO3(Г) + Q
3) N2O2(Г) ↔ NO(Г) + NO2(Г) − Q
4) C(TB) + 2N2O(Г) ↔ CO2(Г) + 2N2(Г) + Q
3.При повышении давления равновесие смещается вправо в системе
1)2СO2(Г) ↔ 2СО(Г) + O2(Г) 3) РСl3(Г) + Сl2(Г) ↔РСl5(Г)
2)С2Н4(Г) ↔С2Н2(Г) + Н2(Г) 4) Н2(Г) + Сl2(Г) ↔ 2НСl(Г)
4.Положение равновесия в системе СН4(Г) + Н2O(Г) ↔СО(Г) + ЗН2(Г) − Q смещается вправо при
1) изменении природы катализатора
2) понижении давления
3) понижении температуры
4) уменьшении объема системы
5.Реакция, химическое равновесие которой сместится в сторону образования исходных веществ как при повышении температуры, так и понижении давления:
1) 2NO(Г)+ SO2(Г)↔ N2O(Г)+ SO3(Г)+ Q
2) 2) NO(Г)+ SO3(Г)↔ SO2(Г)+ 2NO(Г)−Q
3) N2(Г)+O2(Г)↔ 2NO(Г)−Q
4) 4) 3Fe2O3(TB) + Н2(Г)↔ 2Fe3O4(TB) + 2 H2O(Г)+ Q
6.He влияет на состояние химического равновесия в системе 2SO2 + O2 ↔2SO3 + Q
1) катализатор
2) изменение концентрации исходных веществ
3) изменение температуры
4) изменение давления
7.Повышение давления будет смещать положение равновесия в том же направлении, что и понижение температуры в системе
1) СO(Г) + H2O(Г) ↔ CO2(Г) + Н2(Г)+ Q
2) N2(Г) + O2(Г) ↔ 2NO(Г) − Q
3) CO(Г) + 2H2(ТВ) ↔CH3OH(Г)−Q
4)2SO2(Г) + O2(Г) ↔2SO3(Г) + Q
8. При одновременном повышении температуры и понижении давления химическое равновесие сместится вправо в реакции
1) Н2 + S(г) ↔H2S + Q
2) 2SO2 + O2 ↔ 2SO3 + Q
3) 2NH3 ↔ N2 + ЗН2 - Q
4) 2НСl ↔Н2 + Cl2 - Q
9.Изменение давления не смешает равновесие в системе
1) Н2(г) + Se(г) ↔H2Se(г) 2) Н2(г) + Вr2(ж) ↔2НВr(г)
3) H2(г) + Cl2(г) ↔2HCl(г) 4) 2NO(г) + O2(г) ↔2NO2(г)
10.Химическое равновесие в системе 2NO(г) + О2(г) ↔ 2NО2(r) + Q смещается в сторону образования продукта реакции при
1) повышении давления
2) повышении темnературы
3) понижении давления
4) применении катализатора
Тест 4
1.На смещение равновесия системы N2(г) + O2(г) ↔2NO(г) –Q не оказывает влияния
1) повышение температуры
2) повышение давления
3) повышение концентрации NO
4) уменьшение концентрации N2
2.Изменение давления оказывает влияние на смещение равновесия в системе
1) 2SО2 (г)+ О2(г) ↔ 2SO3(г)
2) 2НI(г) ↔ H2(г) + I2(г)
3) СО (г)+ Н2O (г) ↔СO2(г) + Н2(г)
4) N2 (г)+ O2 (г)↔ 2NO(г)
3.Состояние химического равновесия характеризуется
1) изменением химической природы продуктов
2) постоянством концентраций веществ
3) повышением температуры
4) понижением давления
4.В гомогенной реакции 4HCl + O2 ↔ 2Cl2 + 2H2O при повышении давления равновесие сместится
1) влево 2) вправо 3) не сместится
5.В гомогенной реакции 2H2S + 3O2 ↔ 2SO2 + 2H2O при понижении давления равновесие сместится
1) влево 2) вправо 3) не сместится
6.При повышении давления равновесие реакции
S(т) + 2HI ↔ I2 + H2S
1) сместится вправо 2) сместится влево 3) не сместится
