Химическая термодинамика. Химическая кинетика и равновесие
МУРМАНСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
Кафедра химии
Контрольная работа №1
ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА.
ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
по курсу «Химия»
Мурманск
Контрольная работа 1
Химическая термодинамика. Химическая кинетика и равновесие
Вариант 1
1. Что называется внутренней энергией, энтальпией?
2. Определите количество теплоты, выделяющееся при гашении 100 кг извести водой при 25 °С, если известны стандартные теплоты образования веществ, участвующих в химической реакции:
ΔfH˚298 (CaO кр) = -635,1 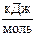 ;
;
ΔfH˚298 (Н2О ж) = -285,84 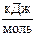 ;
;
ΔfH˚298 (Ca(OН)2 кр) = -982,2 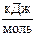 .
.
3. Исходя из ΔfG˚298 соединений, участвующих в реакции, определите, возможна ли реакция:
Al2O3 (кр) + 3SO3 (г) ® Al2(SO4)3 (кр)
4. В какую сторону сместится равновесие реакции:
NiO (кр) « Ni (кр) + 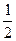 O2 (г) – Q; ΔrH = 262 кДж
O2 (г) – Q; ΔrH = 262 кДж
при понижении температуры, при понижении давления?
5. Во сколько раз изменится константа скорости реакции при увеличении температуры от 500 до 1000 К, если энергия активации равна 95,5 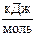 .
.
6. Вычислите константу равновесия химической реакции:
2SO2 (г) + O2 (г) « 2SO3 (г),
протекающей в закрытом сосуде при постоянной температуре. Начальные концентрации веществ равны ( 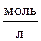 ): С(SO2) = 0,08; C(O2) = 0,06. К моменту наступления равновесия в смеси остаётся 20% первоначального количества SO2.
): С(SO2) = 0,08; C(O2) = 0,06. К моменту наступления равновесия в смеси остаётся 20% первоначального количества SO2.
Контрольная работа 1
Химическая термодинамика. Химическая кинетика и равновесие
Вариант 2
1. Вычислите теплоту образования Fe3O4, исходя из реакции, протекающей по уравнению:
8Al + 3Fe3O4 ® 4Al2O3 + 9Fe + 3349,9 кДж
если теплота образования Al2O3 равна –1675 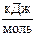 . Сформулируйте закон, на основе которого решаются подобные задачи.
. Сформулируйте закон, на основе которого решаются подобные задачи.
2. Определите ΔrS˚298 системы: H2 (г) + S (ромб) ® H2S (г)
3. Вычислите ΔrG˚298 системы PbO2 + Pb ® 2PbO на основании ΔfH˚298 и S˚298 реагирующих веществ. Определите, возможна ли эта реакция.
4. Укажите факторы, влияющие на скорость химической реакции. Сформулируйте правило Вант-Гоффа.
5. Определите энергию активации реакции, если при увеличении температуры от 500 до 1000 К константа скорости реакции возросла в 100 раз.
6. Константа равновесия химической реакции H2 (г) + I2 (г) ® 2HI (г) при некоторой температуре равна 4. Рассчитайте равновесную концентрацию HI, если исходные концентрации H2 и I2 равны соответственно 0,030 и 0,012 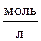 .
.
Контрольная работа 1
Химическая термодинамика. Химическая кинетика и равновесие
Вариант 3
1. В каких случаях возможно самопроизвольное протекание химических реакций при стандартных условиях, если принять ½DH°½>>½TDS°½?
2. Восстановление диоксида свинца водородом протекает по уравнению:
PbO2 (кр) + H2 (г) ® PbO (кр) + H2O (ж); ΔrH˚298 = -182,8 кДж
Определите стандартную теплоту образования PbO2.
3. Рассчитайте ΔrS˚298 реакции разложения бертолетовой соли, если:
S˚298(KClO3) = 142,97 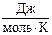 ,
,
S˚298(KCl) = 82,68 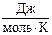 .
.
4. Даны следующие системы:
С (гр) + Н2О (г) « СО (г) + Н2 (г); ΔrH = 131,4 кДж
Н2 (г) + Cl2 (г) « 2HCl (г); ΔrH = -175,7 кДж
РCl5 (г) « PCl3 (г) + Cl2 (г) + Q
CO (г) + Сl2 (г) « СOCl2 (г) – 109,6 кДж
Укажите, какая из систем (1) – (4) является гомогенной? Для каких из реакций (1) – (4) равновесие сместится влево при повышении температуры?
5. Вычислите энергию активации реакции разложения диоксида азота: 2NO2® 2NO + O2,
если константы скорости реакции при 600 и 640 К соответственно равны 83,9 и 407,0 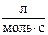 .
.
6. Во сколько раз увеличится скорость реакции, протекающей в газовой фазе, при повышении температуры от 30 до 70 °С, если температурный коэффициент реакции равен 2?
Контрольная работа 1
Химическая термодинамика. Химическая кинетика и равновесие
Вариант 4
1. Почему при низких температурах критерием, определяющим направление самопроизвольного процесса реакций, может служить знак DH , а при достаточно высоких температурах таким критерием является знак DS?
2. При растворении 16 г СаО в воде выделяется 19,3 кДж теплоты. Определите стандартную теплоту образования Са(ОН)2.
3. Вычислите изменение энтропии при стандартных условиях в следующей реакции:
СН4 (г) + 4Cl2 (г) ® ССl4 (ж) + 4HCl (г)
S˚298(СCl4 ж) = 216,19 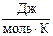 .
.
4. В каких единицах выражается концентрация газообразных и жидких веществ (укажите размерность)?
5. Константа скорости реакции А + 2В ® 3С равна 0,6 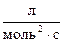 . Начальные концентрации А и В равны соответственно 2,0 и 2,5
. Начальные концентрации А и В равны соответственно 2,0 и 2,5 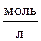 . В результате реакции концентрация вещества В оказалась равной 0,5
. В результате реакции концентрация вещества В оказалась равной 0,5 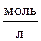 . Вычислите, какова концентрация вещества А и начальная скорость реакции.
. Вычислите, какова концентрация вещества А и начальная скорость реакции.
6. Рассчитайте константу равновесия К химической реакции при 1000 К, если стандартная энергия Гиббса реакции равна при этой температуре –19,1 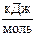 .
.
Контрольная работа 1
