Окислительно-восстановительные реакции. Ионно-электронный метод подбора коэффициентов в окислительно-восстановительных реакциях.
Окислительно-восстановительные процессы связаны с перераспределением электронов между атомами или ионами веществ, участвующих в реакции. Принято считать процесс отдачи веществом электронов окислением, а процесс присоединения электронов – восстановлением. Если одно вещество теряет электроны, то другое вещество, участвующее в реакции, должно их присоединить, при этом общее число электронов, отдаваемых восстановителем, должно быть равно общему числу электронов, присоединяемых окислителем.
Процесс окисления-воостановления с участием кислородсодержащих ионов является сложным процессом, поскольку одновременно с переходом электронов от восстановителя к окислителю происходит разрыв ковалентных связей. Такие реакции протекают с участием молекул или ионов среды. Существует несколько методов составления окислительно-восстановительных реакций, наиболее совершенным среди которых является ионно-электронный метод. Сущность этого метода заключается в следующем:
1. Вначале составляют частные уравнения процесса окисления и процесса восстановления, записывая вещества в той форме, в которой они существуют в растворе: сильные электролиты в ионной форме, слабые – в молекулярной.
2. С участием ионов среды (Н+ в кислой, ОН- в щелочной) или молекул H2O осуществляют материальный баланс, а затем электронный баланс.
3. Составленные частные уравнения суммируют, умножая на соответствующие коэффициенты, подобранные таким образом, чтобы число электронов, теряемых восстановителем, было бы равно числу электронов, приобретаемых окислителем. В результате получают ионное уравнение окислительно-восстановительной реакции.
4. Переносят соответствующие коэффициенты из ионного уравнения в уравнение реакции, написанное в молекулярной форме, и уравнивают количество ионов, не принимавших участие в процессе окисления и восстановления.
Пример:
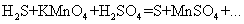
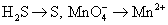
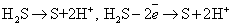
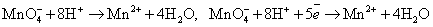
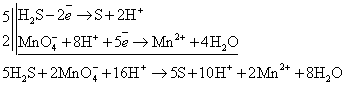
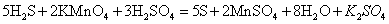
45. Возникновение скачка потенциала на границе раздела «металл-раствор». Равновесный электродный потенциал.
В электрохимии электродом называется проводник первого рода, погруженный в раствор электролита в условиях прохождения через него тока.
В объеме металла имеем подвижное равновесие: 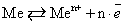
На электроде имеем: 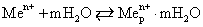
Поверхность электрода заряжается отрицательно за счет оставшихся на нем электроном, вследствие чего перешедшие в раствор гидратированные катионы не могут отойди от электрода и остаются вблизи него, образуя в совокупности с электронами т.н. двойной электрический слой. Пограничный слой жидкости заряжается положительно, металл – отрицательно, получается конденсатор. Возникает скачок электрических потенциалов – электродный потенциал.
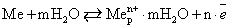
Толщина двойного слоя зависит от концентрации, температуры, заряда металла, колеблясь от нескольких ангстрем до микрона. Переход ионов металла в раствор – окисления, обратный процесс превращения гидратированных ионов металла в атомы – восстановление. Потенциал, отвечающий состоянию равновесию, когда скорость восстановления равна скорости окисления, называют равновесным потенциалом.
При погружении любого металла в воду имеем качественно одно и то же – металл заряжается отрицательно, жидкость вокруг – положительно.
При помещении активного и неактивного металла в растворы их солей активный заряжается отрицательно, а неактивный – положительно.
